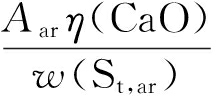电石渣直接湿法碳酸化固定CO2的反应特性
0 引 言
随着人们对气候变化所带来的风险及损害认识的提高,大多数国家承诺将全球温度上升至工业化前2 ℃以下,极具挑战性。碳捕集、利用及封存(CCUS)技术正在全球范围进行广泛研究,常见的CO2封存技术属于燃烧后捕集[1-2],CO2矿化封存是将CO2与含钙、镁量较高的材料反应从而实现CO2固定的技术[3]。SEIFRITZ[4]首先提出加速碳酸化的理念:将碱性物质与CO2在液相条件下反应,反应时间缩短至几分钟或几小时。为进一步提升反应速率,研究人员探究加速碳酸化反应的可能途径。此外,改变其他试验条件如反应温度、液固比、反应时间等也可加速碳酸化[5-8]。多种不同类型反应器用于液相碳酸化,如加压反应釜[9]、旋转填料床[10]和鼓泡床[11]等。电石渣是生产聚氯乙烯(PVC)过程中产生的固体废弃物,主要成分为Ca(OH)2,存在土地占用大、携带二次污染等问题。由于电石渣本身具有强碱性、Ca含量高,具备良好的矿化潜力,常温下即可实现CO2捕集和永久无害的封存[11],因此在直接液相碳酸化研究中有较大价值[12]。
直接碳酸化反应中样品本身所含活性物质总量对碳酸化效率有较大影响,但反应温度、CO2分压力、液固比等因素的影响也极为重要。张亚朋等[13]研究了电石渣、粉煤灰和钢渣干法和湿法直接碳酸化工艺下的CO2封存能力,发现干法条件下电石渣的最终碳化率为38.22%,远低于湿法下62.35%,表明湿法条件下的固碳性能优于干法;任国宏等[14]研究了电石渣、粉煤灰及其配合物在恒温水浴搅拌釜中的碳酸化特性,纯电石渣的最终固碳率约61.3%,与粉煤灰混合后固碳率可提升19.6%。较高的反应温度有利于CaO在水中溶解,对碳酸化反应的反应动力学有促进作用,然而温度超过一定限度,会使CO2在溶液中的吸收量减少。YANG等[15]将电石渣用于高温钙环技术捕获CO2,研究了电石渣在低温甚至是环境温度下的CO2捕集,最终CO2吸附量达18.13%;LIU等[16]将粉煤灰掺杂在电石渣中,并在固定床反应器中进行碳酸化反应。烟气体积分数15%、温度550 ℃、注水量6 kg/h的条件下,碳酸化效率最高达55%。增大CO2压力有利于CO2在水相中溶解,提高最终的碳酸化效率。YUAN等[17]研究发现,增大CO2压力有利于CO2在水中扩散,更有利于其扩散到多孔介质的孔隙中,发生碳酸化反应。在直接液相碳酸化反应中,水是碱性工业固废和CO2之间的反应媒介,液固比是影响碳酸化效率的重要因素。郑鹏等[18]研究了液固比、气速和CO2浓度等操作参数对电石渣在气液固鼓泡床中捕集CO2的影响,发现液固比对碳酸化效率的影响最大,气体流动速度对碳酸化效率的影响最小,增加CO2浓度最初可增加碳酸化效率,但提高到一定程度后,CO2浓度对碳酸化效率的影响较弱。为提升Ca2 和Mg2 在水中的溶解速率,可通过引入添加剂(如NaCl、Na2CO3等)促进碳酸化反应,ALTINER[19]在搅拌釜中提升反应温度、添加油酸钠时,电石渣直接液相碳酸化反应在最佳工况下电石渣碳酸化效率达94.65%。目前关于高压反应釜中电石渣捕集CO2的研究较少,且压力和液固比对碳酸化反应过程中反应速率的影响尚未明确,仍需系统研究。
笔者在高压反应釜中研究了电石渣直接液相碳酸化固定CO2的能力,为优化碳酸化条件,系统研究了不同碳酸化反应过程中不同反应参数对碳酸化反应速率和效率的影响,包括反应时间(0~4 h)、液固比(5~20)和CO2压力(0.1~1.0 MPa)。
1 试 验
1.1 直接液相碳酸化试验
试验所用电石渣购自湖南某工厂,N2(99.9%)与CO2(99.9%)均由南京文达特种气体有限公司提供。加压碳酸化反应装置如图1所示,由CO2气源、反应罐、真空泵和压力数显表等组成:CO2气源由CO2气瓶和气路组成;反应罐容积为2.1 L,最大承受压力为6 MPa,反应釜由1个进气口和2个排气口组成,罐内有1个压力传感接头和1个温控传感接头,位于釜体内部,分别用于测定罐内气体压力以及温度;真空泵为双旋级片真空泵(型号2ZX-4),极限真空压力为6×10-2 MPa,可将反应釜内的压力抽至真空;数显表的压力、温度测量精度分别为0.001 MPa以及0.1 ℃。

图1 碳酸化反应试验系统
Fig.1 Experimental system of carbonation reaction
试验步骤:① 根据工况设定液固比(5~20)称量所需电石渣和水(50 mL),分别加入玻璃皿中,用玻璃棒搅拌30 s以保证充分混合;② 将玻璃皿放入反应釜中,将釜盖盖上旋紧后,关闭进气阀和排气阀,打开真空泵阀门,并打开真空泵开关,至压力表示数降至-0.095 MPa,关闭阀门,最后关闭真空泵。随后悬停静止3 min,观察压力表示数是否发生变化确定气密性;③ 进行直接液相碳酸化反应,打开CO2进气阀,打开气路通入CO2气体直至釜内分压力分别稳定在对应工况下的压力(0.1~1.0 MPa),进行碳酸化试验(4 h);反应结束后,打开排气阀,使容器内气压回到大气压力,打开螺栓;④ 反应结束后打开螺栓将釜内反应完毕的样品取出,收集浆液并通过真空泵抽滤获得固体产物,固体产物在105 ℃下干燥24 h去除水分,最终样品用于后续表征分析。
1.2 数据分析方法
使用热重分析仪(恒久HTG-4)探究样品及其碳酸化反应产物的热分解特性,并通过相关质量平衡公式计算最终碳酸化效率。测试所用电石渣样品质量为20~35 mg,在纯N2气氛下进行加热分解,升温速率控制在10 ℃/min。
样品中主要参与碳酸化反应的成分为Ca(OH)2,反应产物为CaCO3。由式(1)、(2)可知,Ca(OH)2在350~500 ℃分解为CaO和H2O,CaCO3在500~850 ℃分解,分解产物为CaO和CO2,这2个温度区间分别对应分解曲线中2个失重段[20]。第1个失重段是样品Ca(OH)2中H2O的损失,第2个失重段对应CaCO3的分解,因此计算得出2个失重段前后差值可得出Ca(OH)2损失率,并计算得到碳酸化效率。

(1)

(2)
样品原样质量为m1,TG曲线中H2O失重记为X1,CO2失重为Y1,而反应后质量为m2,失重分别记为X2和Y2,根据反应前后钙守恒可得式(3),整理可得式(4)。式中M(Ca(OH)2)、M(H2O)和M(CO2)分别为Ca(OH)2、H2O和CO2的摩尔质量[21]。

(3)

(4)
碳酸化效率Ec可通过参与反应的Ca与Ca总量的比值来计算:

(5)
式中,wc(Ca)为参与反应的Ca含量;w(Ca)为总体Ca含量。
采用日本理学公司的D/max 2500/PC型转靶X射线衍射仪(XRD)测定材料中结晶性物;采用Zetasizer nano粒度分布仪测定样品反应前后的粒度分布;采用荷兰帕森科公司(Panalytical B.V.)的AXIOS-MAX型X射线荧光光谱分析仪(XRF)测定样品元素组成,硼酸做黏合剂。
研究了CO2压力和液固比对电石渣碳酸化反应的影响,一次只改变一个参数。为确定CO2初始分压力带来的影响,由于总压降Ptotal是由于吸附水中CO2和存在于电石渣中的CaO和Ca(OH)2产生的,因此压降仅是由于水中CO2吸附(Pw)引起。由于水的体积和其他影响因素一致,因此由碳酸化反应引起的压降Pc[22]表示为
Pc=Ptotal-Pw。
(6)
考虑到CO2为理想气体,利用理想气体定律可量化矿化封存CO2量n[23]:

(7)
式中,P为CO2压降量;V为反应罐容积;R为气体常数;T为气体温度。
2 结果与讨论
2.1 原样分析
对电石渣原样进行XRD、XRF和粒度分布测试,XRD分析如图2所示,化学成分见表1。粒度分布测试得到电石渣平均粒径为49.5 μm。电石渣主要成分为Ca(OH)2和CaCO3,原样XRD曲线多处显示Ca(OH)2衍射峰,此外在35.4°处也观察到1个强度较弱的CaCO3(方解石)衍射峰,这表明电石渣堆放过程与空气中CO2反应发生部分碳酸化反应,生成CaCO3。

图2 电石渣的XRD图
Fig.2 XRD diagram of carbide slag
表1 材料主要化学成分
Table 1 Main chemical composition of materials

对电石渣原样进行TG/DTG测试,测试分析结果如图3所示。由图3可知,电石渣原样主要有2个失重段,分别对应Ca(OH)2和CaCO3分解,计算得出电石渣中Ca(OH)2占比76%,表明电石渣中活性物质多,具备较好的CO2固定潜力。

图3 电石渣TG/DTG曲线
Fig.3 TG/DTG curves of carbide slag
2.2 CO2压力对碳酸化效率的影响
液固比5、CO2初始分压力0.1~1.0 MPa,电石渣在高压釜中反应4 h时,釜中CO2压降曲线如图4(a)所示,电石渣的吸附量变化如图4(b)所示,以过程中反应釜CO2压力下降量确定初始CO2分压力对碳酸化反应的影响。

图4 不同压力下电石渣液相碳酸化
Fig.4 Liquid phase carbonation of carbide slag at different pressures
反应过程中,固液悬浊液内同时存在水的物理吸附和碳酸化反应2种作用,釜内CO2压力会逐渐降低,直至达到平衡;另一方面CO2初始转移速率受到初始CO2压力影响[22],根据亨利定律[24],在给定温度下,溶入溶液的气体浓度与溶液上方气体的分压力呈正比,因此容器内CO2压力会对液固悬浊液的CO2吸收率有促进作用。由图4(a)可知,由于吸附和碳酸化反应导致的CO2吸收会在CO2气体通入后2~3 h内稳定下来,后续反应速率显著降低。
此外,初始CO2分压力对CO2初始转移到悬浊液中的速度有影响,在更高CO2初始压力下,悬浊液中CO2碳酸化反应速度更快。为确定固存到样品中的实际CO2量,需先去除由于水吸附而导致的压力降低。为此在每种压力下仅用水进行对照试验,并记录釜中压力随时间的变化。根据式(6)、(7)计算得到样品的实际吸附量,并绘制图4(b)。
由图4(b)可知,电石渣碳酸化反应主要发生在前60 min,整体反应速率快,压降明显,反应前120 min内,样品中Ca(OH)2基本都参与反应,后续反应中大部分Ca(OH)2转化为碳酸钙后,液固悬浊液从釜中吸收CO2速率降低,釜中CO2压力下降较缓慢;0.1 MPa下150 min后压力基本饱和,到达平衡所需反应时间较长。而较高压力下,180 min反应仍在发生,且压力在较短时间内迅速下降,表明更高的压力可使碳酸化反应速率提升;这与前人研究结果相似,UKWATTAGE等[22]用粉煤灰在高压反应釜中进行液相碳酸化试验,2~6 MPa初始分压力在2~4 h后趋于稳定,且较高的分压将导致饱和孔隙水中大量溶解CO2,增加反应速率。压力由0.1 MPa升至1.0 MPa时,电石渣的最终吸附量分别为3.58、7.59、8.10和8.17 mmol/g,压力对吸附量的影响较大,但CO2初始分压力超过0.5 MPa后,继续提升压力对吸附量提升并不明显。
2.3 液固比对碳酸化效率的影响
1.0 MPa下,不同液固比电石渣的压力下降和吸附曲线如图5所示。由图5(b)可知,液固比由5增至20,碳酸化反应均能有效进行,但液固比对碳酸化效率的影响逐渐变小。液固比由5升至20,电石渣最终吸附量由8.17 mmol/g提高至9.26 mmol/g。这是由于水体积增加会使单位体积中样品含量下降,因此固液悬浊液中的Ca2 浓度逐渐降低[5,25]。另一方面CO2扩散速率对固体材料碳酸化效果有较大影响。由于碳酸盐沉淀层溶解度低,会堵塞孔隙系统,因此,当孔壁附近Ca(OH)2被碳酸化反应消耗时,Ca2 溶解速度受到影响。孔隙溶液中Ca(OH)2浓度无法保持较高水平,碳酸化反应受Ca2 扩散速率制约。液固比由5提升至20时,电石渣最终吸附量的增长趋势逐渐降低,表明电石渣中Ca2 离子析出速率变缓。上述结果与前人对固废的碳酸化反应一致,CHANG等[25]研究了液固比对转炉渣碳酸化效率的影响,液固比为20时,转炉渣的碳酸化效率最高。

图5 不同液固比下电石渣液相碳酸化
Fig.5 Liquid phase carbonation of carbide slag at different liquid-solid ratios
对比最终CO2吸附量后,将初始分压力1.0 MPa、液固比20工况下的反应产物定为最优样品,初始分压力0.1 MPa、液固比5工况下的反应产物定为最低样品,进行后续测试。
2.4 碳酸化产物表征分析
将各工况下的碳酸化反应产物进行了TG/DTG测试。N2气氛下,升温速率10 ℃/min时电石渣原样及各工况中的碳酸化效率最低工况与最优工况(最低样品、最优样品的碳酸化效率为34.95%、90.35%)的热重曲线如图6所示。由图6(a)可以看出,电石渣原样和最低、最优工况的TG曲线均存在2个明显的失重段,代表加热分解过程有2部分:第1部分是由350 ℃升至500 ℃过程中,样品中未完全反应的Ca(OH)2分解成为CaO和H2O;剩下的CaCO3在500~800 ℃分解,产物为CaO和CO2。

图6 电石渣碳酸化产物的热分解规律
Fig.6 Thermal decomposition law of carbonated products of carbide slag
此外,碳酸化反应后,明显看到固相碳酸化产物的第1个失重段略减小,说明Ca(OH)2在碳酸化反应过程中消耗一小部分。而最优样品的TG曲线第1个失重段较小,表明最优样品中的Ca(OH)2大部分参与反应。图6(b)中2个峰对应TG中2个失重段,进一步验证了上述结论。Ca2 在溶液中的扩散速率是影响CaCO3生成的主要因素,在液固比20、压力1.0 MPa最优工况下,溶液中Ca2 和![]() 含量较高,有利于二者结合生成
含量较高,有利于二者结合生成
根据式(5)计算出反应产物的碳酸化效率,电石渣在不同工况下的最终碳酸化效率如图7所示。液固比不变,压力由0.1 MPa升至1.0 MPa,碳酸化效率由34.95%上升至79.56%;而CO2压力一定时,液固比由5提升至20,电碳酸化效率仅由79.56%提升至90.35%。表明在该反应器中,CO2初始分压力相比液固比对碳酸化效率的影响更重要。

图7 电石渣各工况碳酸化效率
Fig.7 Carbonation efficiency of carbide slag at different conditions
对电石渣液相碳酸化反应后样品进行XRD表征测试,测试结果如图8所示。不完全碳酸化反应的最低样品与图2原样相比,其XRD图谱中21°、29°、49°的2θ角处Ca(OH)2衍射峰明显削弱,而CaCO3(方解石)峰数量增加。表明碳酸化反应消耗了电石渣中Ca(OH)2,最终转化为CaCO3。最优工况下最优样品的XRD图谱中出现了更多CaCO3峰,且无法观察到Ca(OH)2峰。表明电石渣中Ca(OH)2在对应工况下都参与了碳酸化反应,碳酸化效率较高。

图8 电石渣碳酸化产物XRD分析
Fig.8 XRD analysis of carbonation products of carbide slag
电石渣及其碳酸化反应产物的激光粒度分析如图9所示,电石渣原样中粒径小于50.24 μm的颗粒体积分数为50.71%,而最低样品中粒径小于56.5 μm的颗粒体积分数为70.32%,反应较彻底的最优样品固体产物中有85.92%颗粒粒径小于56.54 μm。

图9 电石渣碳酸化产物的粒径分布
Fig.9 Particle size distribution of carbonation products of carbide slag
碳酸化效率越高,固体产物颗粒粒径越小,且粒径最大分布峰变小,此外小于1 μm分布峰逐渐增大,原因可能是碳酸化反应中大尺寸Ca(OH)2逐渐溶解,同时产生了粒径较小的CaCO3沉淀。碳酸化反应不完全的样品可能是由于反应产物CaCO3在反应过程中于样品表面形成了致密的钝化层[27],这将降低产物内部Ca(OH)2的溶解速率,因此反应无法进一步发生。
电石渣碳酸化反应产物的微观形貌如图10所示。通过比较原样和最优样品发现,相比颗粒差距较大的原样,最优样品的颗粒更细致且分散较均匀,这与上述粒径分布分析相符。放大倍率后,最优样品反应产物表面上生成了更多的立方体和菱形形状的方解石,反应生成的CaCO3包裹产物表面且覆盖了内部Ca(OH)2,阻止碳酸化反应的进一步发生,影响最终碳酸化效率。

图10 电石渣及其碳酸化产物的微观形貌
Fig.10 Micro-morphology of carbide slag and its carbonation products
2.5 碳酸化机理分析
碳酸化反应主要包括2部分:① CO2溶于水生成H2CO3,碳酸电离成 和H 三种离子;② 样品中活性物质溶解,Ca2 析出,在孔隙结构中与CO2发生反应并生成碳酸盐沉淀:
和H 三种离子;② 样品中活性物质溶解,Ca2 析出,在孔隙结构中与CO2发生反应并生成碳酸盐沉淀:
CO2 H2O![]() H2CO3,
H2CO3,
(8)

(9)

(10)

(11)
Ca(OH)2![]() Ca2 2OH-,
Ca2 2OH-,
(12)

(13)
碱性固体废物加速碳化反应的机理如图11所示,碳酸化总体速率和碳酸化反应程度由以下机制控制:① Ca2 离子运输到反应部位的速率;② CO2扩散速率;③ Ca(OH)2溶解速率;④ 孔隙堵塞;⑤ 产物沉淀,覆盖表面[28]。一方面CO2初始分压力的提升会促进CO2在水中的扩散速率,有利于碳酸化反应的进行,另一方面液相碳酸化反应中水是加速整体反应的必要条件,YADAV等[29]认为水是碳酸化反应中不可或缺的一部分,在没有任何水分的情况下,会直接发生气相碳酸化,且与液相碳酸化相比反应速率非常低,但CO2扩散速率会被过量水所阻碍。在上述5个机制中,Ca2 的浸出是影响碳酸化反应的关键[6]。液固比会影响钙和其他碱性阳离子从固体中的浸出速率,液固比过低会导致反应过程中孔隙系统堵塞,液固比过高时,过多的水会对Ca2 的浸出造成影响,从而阻碍反应进行[30]。

图11 碱性固体废物加速碳化反应机理
Fig.11 Proposed mechanism of accelerated carbonation reaction of alkaline solid wastes
3 结 论
1)电石渣在高压反应釜中碳酸化效率高,最佳工况下的碳酸化效率达到90.35%,吸附量为9.26 mmol/g。
2)液相碳酸化反应主要发生在前60~120 min,随CO2初始压力、液固比的增大,最终吸附量不断提升,但将液固比由10升至20对吸附量的影响较微弱,CO2初始分压力对吸附量影响最大,将初始分压力由0.1 MPa升至0.5 MPa,电石渣最终吸附量提升了4.01 mmol/g,继续升高压力对吸附量影响较小。
3)SEM和热重分析得出电石渣碳酸化反应后生成大量CaCO3,最优样品中的Ca(OH)2基本完全反应,生成的CaCO3会覆盖在产物表面并覆盖内部Ca(OH)2,且反应后碳酸化完全的最优样品粒径小于最低样品粒径。
[1] 刘嘉, 李永, 刘德顺.碳封存技术的现状及在中国应用的研究意义[J].环境与可持续发展, 2009, 34(2): 33-35.
LIU Jia, LI Yong, LIU Deshun.Current status of carbon sequestration technology and its application in China[J].Environment and sustainable development,2009, 34(2): 33-35.
[2] 邢晨健, 王瑞林, 赵传文.燃煤电站与光伏余热辅助胺法脱碳系统集成[J].洁净煤技术, 2021, 27(2): 170-179.
XING Chenjian, WANG Ruilin, ZHAO Chuanwen.Integration of coal-fired power station and photovoltaic waste heat assisted amine decarbonization system[J].Clean Coal Technology, 2021, 27(2): 170-179.
[3] HO H J, IIZUKA A, SHIBATA E J I, et al.Carbon capture and utilization technology without carbon dioxide purification and pressurization: A review on its necessity and available technologies[J].Industrial &Engineering Chemistry Research, 2019, 58(21): 8941-8954.
[4] SEIFRITZ W.CO2 disposal by means of silicates[J].Nature, 1990, 345: 486-486.
[5] CHANG E E, PAN S Y, CHEN Y H, et al.CO2 sequestration by carbonation of steelmaking slags in an autoclave reactor[J].Journal of Hazardous Materials, 2011, 195: 107-114.
[6] COSTA G, BACIOCCHI R, POLETTINI A, et al.Current status and perspectives of accelerated carbonation processes on municipal waste combustion residues[J].Environmental Monitoring Assessment, 2007, 135(1): 55-75.
[7] LI X, BERTOS M F, HILLS C D, et al.Accelerated carbonation of municipal solid waste incineration fly ashes[J].Waste Management, 2007, 27(9): 1200-1206.
[8] HUIJGEN W J, WITKAMP G J, COMANS R N.Mechanisms of aqueous wollastonite carbonation as a possible CO2 sequestration process[J].Chemical Engineering Science, 2006, 61(13): 4242-4251.
[9] WU W, HAN B, GAO H, et al.Desulfurization of flue gas: SO2 absorption by an ionic liquid[J].Angewandte Chemie International Edition, 2004, 43(18): 2415-2417.
[10] MOTA A, VICENTE A A, TEIXEIRA J.Effect of spent grains on flow regime transition in bubble column[J].Chemical Engineering Science, 2011, 66(14): 3350-3357.
[11] PAN S Y, CHIANG A, CHANG E, et al.An innovative approach to integrated carbon mineralization and waste utilization: A review[J].Aerosol and Air Quality Research, 2015, 15: 1072-1091.
[12] YANG J, LIU S, MA L, et al.Mechanism analysis of carbide slag capture of CO2 via a gas-liquid-solid three-phase fluidization system[J].Journal of Cleaner Production, 2021, 279: 123712.
[13] 张亚朋, 崔龙鹏, 刘艳芳, 等.3种典型工业固废的CO2矿化封存性能[J].环境工程学报, 2021, 15(7): 2344-2355.
ZHANG Yapeng, CUI Longpeng, LIU Yanfang, et al.Comparison of three typical industrial solid wastes on the performance of CO2 mineralization and sequestration[J].Chinese Journal of Environmental Engineering, 2021,15(7): 2344-2355.
[14] 任国宏, 廖洪强, 吴海滨, 等.粉煤灰、电石渣及其配合物碳酸化特性[J].环境工程学报, 2018, 12(8): 2295-2300.
REN Guohong, LIAO Hongqiang, WU Haibin, et al.Carbonation characteristics of fly ash, carbide slag and their mixtures[J].Chinese Journal of Environmental Engineering, 2018, 12(8): 2295-2300.
[15] YANG J, LIU S, MA L, et al.Mechanism analysis of carbide slag capture of CO2 via a gas-liquid-solid three-phase fluidization system[J].Journal of Cleaner Production, 2021, 279: 123712.
[16] LIU R, WANG X, GAO S.CO2 capture and mineralization using carbide slag doped fly ash[J].Greenhouse Gases: Science Technology, 2020, 10(1): 103-115.
[17] YUAN Y, LU W, CHENG W, et al.Method for rapid mineralization of CO2 with carbide slag in the constant-pressure and continuous-feed way and its reaction heat[J].Powder Technology, 2022, 398: 117148.
[18] 郑鹏, 李蔚玲, 郭亚飞, 等.鼓泡床中电石渣加速碳酸化分析与响应面优化[J].化工进展, 2022, 41(3): 1528-1538.
ZHENG Peng, LI Weiling, GUO Yafei, et al.Analysis of carbide slag accelerated carbonation in bubble column and response surface optimization[J].Chemical Industry and Engineering Progress, 2022, 41(3): 1528-1538.
[19] ALTINER M.Use of Taguchi approach for synthesis of calcite particles from calcium carbide slag for CO2 fixation by accelerated mineral carbonation[J].Arabian Journal of Chemistry, 2019, 12(4): 531-540.
[20] NIU S, LIU M, LU C, et al.Thermogravimetric analysis of carbide slag[J].Journal of Thermal Analysis and Calorimetry, 2014, 115(1): 73-79.
[21] 郑鹏, 李蔚玲.鼓泡床中电石渣液相碳酸化反应流动特性表征[J].南京师范大学学报(工程技术版), 2022, 22(2): 1-8.
ZHENG Peng, LI Weiling.Characteristics of carbide slag slurry flow in a bubble column reactor[J].Journal of Nanjing Normal University(Engineeging and Technoloy Edition), 2022, 22(2): 1-8.
[22] UKWATTAGE N L, RANJITH P, WANG S.Investigation of the potential of coal combustion fly ash for mineral sequestration of CO2 by accelerated carbonation[J].Energy, 2013, 52: 230-236.
[23] MALHOTRA V J C I.Making concrete "greener" with fly ash[J].Concrete International, 1999, 21(5): 61-66.
[24] HENRY W.Experiments on the quantity of gases absorbed by water, at different temperatures, and under different pressures[J].Philosophical Transactions of the Royal Society of London, 1803,93:29-42.
[25] CHANG E E, CHIU A C, PAN S Y, et al.Carbonation of basic oxygen furnace slag with metalworking wastewater in a slurry reactor[J].International Journal of Greenhouse Gas Control, 2013, 12: 382-389.
[26] KITAMURA M, KONNO H, YASUI A, et al.Controlling factors and mechanism of reactive crystallization of calcium carbonate polymorphs from calcium hydroxide suspensions[J].Journal of Crystal Growth, 2002, 236(1/3): 323-332.
[27] AIL S S, DASAPPA S.Biomass to liquid transportation fuel via Fischer Tropsch synthesis:Technology review and current scenario[J].Renewable and Sustainable Energy Reviews, 2016, 58: 267-286.
[28] HUNTZINGER D N, GIERKE J S, SUTTER L L, et al.Mineral carbonation for carbon sequestration in cement kiln dust from waste piles[J].Journal of Hazardous Materials, 2009, 168(1): 31-37.
[29] YADAV V S, PRASAD M, KHAN J, et al.Sequestration of carbon dioxide(CO2)using red mud[J].Journal of Hazardous Materials, 2010, 176(1/3): 1044-1050.
[30] JOHANNESSON B, UTGENANNT P.Microstructural changes caused by carbonation of cement mortar[J].Cement Concrete Research, 2001, 31(6): 925-931.
Reaction characteristics of carbon dioxide fixation by direct wet carbonation of carbide slag

KONG Xiao,ZHAO Chuanwen,SUN Jian,et al.Reaction characteristics of carbon dioxide fixation by direct wet carbonation of carbide slag[J].Clean Coal Technology,2023,29(4):129-136.