电催化二氧化碳还原用铜基催化剂设计策略
0 引 言
自工业革命以来,化石燃料消耗不断增加,造成CO2大量排放,在大气中的浓度不断增加。作为一种典型温室气体,过量CO2会阻碍反射的太阳能向外太空消散,引发气候变暖和一系列全球环境危害。为降低大气中CO2浓度,阻止人为碳循环[1],由清洁电力驱动的电催化二氧化碳还原反应(CO2RR)可在温和条件下将CO2有效转化为增值化学品[2-4]。CO2RR技术是在常温常压条件下,利用电能(尤其是可再生能源发电)将CO2与水直接反应生成合成气、甲酸、碳氢化合物、醇类等高附加值的化学品或液态燃料的新技术,是一条实现可再生能源存储与CO2转化利用相耦合的绿色途径,对人类可持续发展具有重要意义。CO2RR技术不需要制氢、加温和加压额外消耗的能量,且所需仪器设备耗费较低,其潜在的经济效益和环境效益引起广泛关注。由于未来电力可能来自风能、太阳能和潮汐能等可持续能源,CO2RR使其能储存在化学品中,克服了利用这些可再生能源期间的地理或时间限制[5-7]。
近年来,学术界和工业界在开发高性能CO2RR电催化剂方面付出巨大努力[8-9]。对于CO2电化学转化,电催化剂在激活稳定的线性CO2分子和推动反应路径发展方面起重要作用[10-11],但仍存在许多问题,如过电势高、电子传递动力学缓慢、产物选择性低、分电流密度低、催化剂稳定性与耐久性欠佳(大多数低于1 000 h)等。上述问题限制了CO2RR技术的实际应用和商业化[12]。电催化剂作为CO2RR技术的关键材料,其性能直接影响CO2转化效率、还原产物选择性及稳定性[13]。因此,开发高性能的电催化剂,提高催化剂的催化活性、选择性和稳定性具有重要意义和应用价值。
笔者综述了近年来电化学催化CO2RR用铜基催化剂优化设计策略方面取得的重要研究进展。首先描述了电催化CO2RR技术的基本原理,特别是利用铜基催化剂催化形成多碳产物的可能反应路径和机理。然后从提高催化剂的催化活性、产物选择性及稳定性2方面讨论了设计策略,并结合代表性研究案例加以分析讨论。最后对电化学催化CO2RR用铜基催化剂的优化设计策略方面取得的重要研究进展进行总结回顾,并对该领域的前景与挑战进行展望。
1 CO2RR技术原理
电化学催化CO2还原反应(CO2RR)是一个复杂的多相反应过程,包含多种反应途径、中间体和产物,并伴随复杂热力学与动力学问题[14-16]。从热力学角度分析,CO2由于其强化学键和线性结构在环境条件下极为稳定,导致其在CO2RR过程中难以活化,反应活性较低[17-18]。在动力学方面,通过各种反应中间体的结合,有多种路径形成最终产物,导致CO2RR产物选择性较低[19],在热力学方面,CO2RR反应物和产物的标准吉布斯自由能决定了反应的进行[20-23]。表1列举了典型的电化学反应方程式,包括CO2RR中的关键半反应、氢气析出反应(HER)、相应的标准氧化还原电位及产物分布组成[24-25]。如活化CO2参与CO2RR所需标准电位为-1.9 V (vs. SHE),远低于生成大多数CO2还原产物所需电位。实际应用中,通常存在较大过电位。为促进CO2RR进行,可设计使用催化剂和电解质进行质子化和水合反应过程,2个过程反应路径、机制及标准氧化还原电位不同。一般来说,质子化过程所需电位远低于水合反应过程,表明质子相关电子转移过程在热力学上更有利于生成C2 产物[26]。
表1 典型的CO2RR半反应
Table 1 Typical CO2RR half-reactions

续表

注:*在1.0 mol/L电解质水溶液中, 101 300 Pa、25 ℃、pH=7的条件下,基于反应物和CO2还原产物的标准吉布斯自由能计算得出的CO2RR标准电极电位,计算时考虑H 和OH-浓度为10-7 mol/L。
在热力学上,生成C2 产物通常比C1产物具有更正的标准电位,表明生成高价值的C2 产物在热力学上可行。然而,由于动力学限制,生成C2 产物通常需更大过电位[27]。因此,在施加电位方面,C2 产物通常在C1产物后产生[28]。在大多数情况下,随着施加电位增加(向更负电位方向),首先生成CO和甲酸(或甲酸根),然后是甲醇和甲烷,最后生成类似于乙烯、乙烷和乙醇等C2 产物[29]。由于大多数CO2RR半反应的标准电位接近氢气析出反应(HER)的标准电位,氢气成为水溶液中CO2RR的主要副产物[30]。
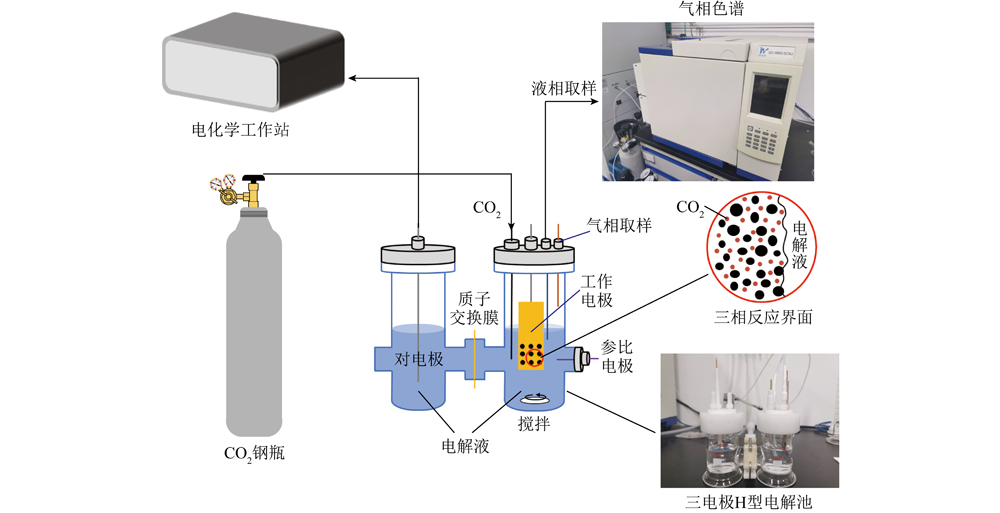
电化学CO2RR主要包括扩散、吸附、活化、裂解和二聚化及产物脱附等步骤,易受反应环境和催化剂的影响[31-32]。以在流动式电解槽(Flow cell)中进行的CO2RR为例,CO2首先穿过气体扩散层,在催化剂与电解液形成的气-液-固三相界面以吸附形式被目标催化剂的活性位点捕获。吸附的CO2通过获得一个电子被活化,并通过相邻的H 和H /e-对进一步被质子化,形成CO2RR不同中间体和产物。最终产物从活性中心脱附,通过逆向扩散离开催化剂表面,最终进入电解质或扩散回到气相中[33-36]。
CO2RR由CO2吸附开始,在催化剂表面形成*CO2,其吸附状态受到*CO2与催化剂之间结合能影响,造成后续反应路径不同[22,37-38]。以线性吸附模式为例,CO2分子倾向于被活性位点吸引,并形成*CO2,此中间体将捕获一个电子(e-)并将其转移到中心碳原子上,使C原子远离或吸引靠近活性位点[15,22](图1(a),箭头表示协调的质子或电子转移步骤),导致CO2线性结构被弯曲和拉伸,从而削弱C—O键,在催化剂表面上形成CO2和活性位点之间的新化学键,生成CO2RR的重要中间体 此步骤(表1第1个半反应)需-1.9 V vs. SHE电位驱动转化,是CO2RR的第1个决速步骤,也是形成不同CO2还原产物的第1个分岔口。
此步骤(表1第1个半反应)需-1.9 V vs. SHE电位驱动转化,是CO2RR的第1个决速步骤,也是形成不同CO2还原产物的第1个分岔口。![]() 中间体将通过逐步耦合H 和/或e-,形成不同C1产物或C2 产物中间体,反应途径主要由吸附状态、结合强度和涉及中间体的相互关系决定[40]。如果新生成的C原子和催化剂活性位点之间的键合作用太弱,则在质子耦合电子转移过程中易断裂,导致生成甲酸根(图1(a))[41]。如果键合作用很强,
中间体将通过逐步耦合H 和/或e-,形成不同C1产物或C2 产物中间体,反应途径主要由吸附状态、结合强度和涉及中间体的相互关系决定[40]。如果新生成的C原子和催化剂活性位点之间的键合作用太弱,则在质子耦合电子转移过程中易断裂,导致生成甲酸根(图1(a))[41]。如果键合作用很强,![]() 将首先转换为*COOH,转化为另一个重要中间体*CO(图1(b)),这是生成C1和C2 产物又一个反应路线分岔口[42]。如果*CO直接从催化剂表面脱附,将产生CO气体[43-44],反之,*CO可触发一系列电子转移和质子化过程(图1(b)),发生C—O键断裂和C—H键生成,进而形成新的C1中间体,如*CHO和*COH,并最终转化为不同产物,如通过*CO加氢产生的*CHO和*COH是生成CH4和CH3OH的关键中间体(图1(c))。
将首先转换为*COOH,转化为另一个重要中间体*CO(图1(b)),这是生成C1和C2 产物又一个反应路线分岔口[42]。如果*CO直接从催化剂表面脱附,将产生CO气体[43-44],反之,*CO可触发一系列电子转移和质子化过程(图1(b)),发生C—O键断裂和C—H键生成,进而形成新的C1中间体,如*CHO和*COH,并最终转化为不同产物,如通过*CO加氢产生的*CHO和*COH是生成CH4和CH3OH的关键中间体(图1(c))。

图1 电催化CO2RR中C1~C3产物的反应途径[3]
Fig.1 Reaction pathways for C1-C3 products in electrocatalytic CO2RR[3]
考虑到C2 产物通过*CO、*CHO和*COH等关键中间体的非常复杂的质子耦合电子转移过程形成,以下仅列举一些代表性产物的形成途径(图1(c))[45]。*CO、*CHO和/或*COH中间体的二聚化
形成生成C2 产物的关键中间体,如*COCO、*COCHO和*COCOH。其中,*COCO中间体通过2个*CO耦合生成,是生成C2 产物的又一个决速步骤,*COCHO和*COCOH可通过*COCO获得一个H /e-对或*CO与*CHO和*COH的直接反应得到[46-47]。虽然典型的C2 产物可从相同C2 中间体生成,如乙烯、乙醇和丙醇等,但通常具有不同的能垒和优选形成途径[48]。如乙烯通常通过以下途径形成:*COCHO→*CCHO→*CHCHO→*CH2CHO→C2H4,这条途径与其他产物相比步骤较少,使乙烯成为水溶液中主要C2 产物[49-50]。而*COCOH途径更有利于乙醇的产生,反应路径为*COC→*CCOH→*CHCOH→*CHCH2OH→*CH2CH2OH→C2H5OH[51]。同时,乙醇也可通过以下途径获得,即*CH2CHO→ *CH3CHO→C2H5OH。如果*CO和*COCOH直接相互反应形成*COCOHCO中间体,则可后续生成丙醇。
2 提高铜基催化剂催化活性和选择性的设计策略
铜(Cu)是一种用于CO2RR的异相催化剂,是唯一能选择性催化CO2RR生成烃类/含氧化合物的纯金属催化剂,受到广泛关注。相比之下,过渡金属如铂(Pt)、镍(Ni)、铁(Fe)和钛(Ti),具有较低的氢过电势和较高的CO吸附能力。被CO中毒时,主要选择性进行析氢反应。P区块金属(即汞(Hg)、铅(Pb)、铊(Tl)、铟(In)、镉(Cd)和锡(Sn))具有较高的氢过电势和独特的嗜氧特性,对形成甲酸盐的关键中间体*OHCO有强烈的吸附作用,因此倾向于产生甲酸盐。其他金属,如金(Au)、银(Ag)和锌(Zn),主要通过CO2还原生成CO。与这些金属不同,Cu的独特之处在于允许以高产量形成甲烷和其他C—C耦合产物。合理设计低过电位、高电流密度、高法拉第效率、长期稳定的催化剂是提高CO2RR能量效率的中心任务。目前,铜基催化剂优化设计代表性策略,如晶面工程、合金化处理、铜氧化态调节、催化剂表面功能化和缺陷工程,已被应用于通过调节活性和选择性来调节CO2还原和提高能量效率。
2.1 晶面工程
纳米结构工程被广泛应用于调整反应路径和催化性能,可追溯到一些基本原理,特别是电子结构的调制和中间吸附。通过调节成核速率或在合成中使用配体,可合理控制纳米晶体的暴露面,使其具有特定的原子排列、表面能和中间亲和力[52-53]。研究发现,(100)面封闭的铜立方体有利于CO2转化为乙烯,(111)面封闭的铜八面体有利于甲烷生成,而混合面封闭的铜纳米球体不具有完全选择性(图2(a)、2(b))[54]。

图2 铜催化剂的典型结构及CO2还原过程中电位对法拉第效率的影响
Fig.2 Typical structures of Cu catalysts and the effect of potential on Faradaic efficiency during the CO2RR process
值得注意的是,制备高指数面催化剂可为CO2分子吸附和活化提供丰富活性位点。具有(711)和(911)面和高密度原子台阶面的铜催化剂倾向于生成乙烯,而在低过电位下抑制甲烷。通过使用金属离子电池循环策略,WANG Haotian课题组选择性地暴露铜(100)面,密度泛函理论(DFT)计算证实这有利于初始C—C耦合步骤。100次循环后,与原始抛光铜箔(111)表面相比,铜纳米立方催化剂的C2 /C1产物比率提高6倍,为提高C2 产物的能量效率提供可行性策略[55]。
2.2 合金化处理
开发高效的CO2RR电催化剂通常采用合金化处理方式。这种方式通过结合至少2种类型金属来调控CO2RR表面吸附亲和力和反应性,其中杂原子与主金属的相互作用带来几何效应和电子效应[56]。通过改变化学成分、形态、元素分布和晶体结构,合金化处理导致CO2RR电催化剂独特的催化表现[57-58]。以不同成分PdCu合金纳米颗粒为例,介孔Pd7Cu3的CO生成效率达80%以上,其中Cu调节相邻Pd的电子结构,增强活性Pd中心对CO2/*COOH的吸附和CO的脱附(图2(c)、2(d))[59]。Roy课题组的研究报告指出,Cu催化剂上CO的选择性随着客体金属Au含量的增加而增加[60]。这可能是由于CO与基质金属之间的结合较弱,无法使CO从基质金属表面脱附。某些情况下,铜基双金属合金颗粒具有过电位低、选择性好等特点,有利于C2 产物的生成[61]。ZHONG等[62]开发的去合金化的Cu-Al催化剂在1.5 V vs. RHE条件下对乙烯的选择性大于80%,在150 mA/cm2条件下阴极能量效率为55%。Al作为调制剂可以诱导Cu催化剂的活性位点,促进催化剂表面高度纳米化,并产生与OH-或K 离子相关的电解质效应,从而使得Cu-Al催化剂获得较高的选择性和能量效率[62]。
2.3 铜氧化态调节
由于铜的氧化衍生物在生成C2 产物方面的催化性能优异,铜基催化剂中铜的氧化态调控是CO2RR中被广泛讨论的课题。考虑到催化剂制备和应用过程中面临的复杂多变条件,包括合成过程、暴露于空气或电解质及外加电压,铜的氧化态通常是动态的[63]。因此,利用动态现场原位技术(如原位X射线吸收光谱(XAS))实时监测铜的氧化态对于揭示铜的氧化态与催化性能之间的相关性具有重要意义。
原则上,铜的氧化态对CO2RR性能的影响涉及活性位点和电子结构(如能带、功函数和自旋态)的调控,从而决定了CO2分子的活化和关键中间体的吸附[64]。值得注意的是,在铜氧化态演化过程中,铜基催化剂的纳米结构和形貌发生变化,从而产生有利于CO2RR的缺陷或晶界[65]。
对于铜基催化剂来说,等离子体处理的铜箔上的动态现场原位XAS研究表明,在阴极反应条件下,初始Cu 可以存活,有助于乙烯的高选择性生成(图3(a)、3(b))[66]。通过使用脉冲电解策略,CUENYA课题组观察到乙醇选择性提高是由于利用周期性阳极电压变化在催化剂表面原位连续产生缺陷和Cu 基团,并协同促进C—C偶联途径(图3(c)、3(d))[67]。Cu0和Cu 的共存通常会降低CO2分子的活化能和C—C偶联步骤,从而提高C2 产物产量和相应的能量效率。除Cu外,铜的氧化态对其他金属也有影响,包括Ag、Zn、In、Sn等各类型金属,这些金属的化学状态及铜基催化剂纳米结构的演变共同决定产物选择性[68]。

图3 原位X射线吸收光谱和脉冲电解技术对C2产物选择性的探究
Fig.3 Investigation of C2 product selectivity using in situ X-ray absorption spectroscopy and pulse electrolysis techniques
2.4 催化剂表面功能化
有机分子的表面功能化是控制催化剂活性/选择性和特定产物能量效率的简单有力策略,提供了分子催化和多相催化之间的桥梁,在多相催化中,表面分子重塑核心催化剂的能态,并改变催化剂附近的反应微环境。功能分子的影响取决于配体的组成、覆盖密度、空间排列及配体与活性物质之间的相互作用强度。表面功能化调节催化行为的潜在机制可能与立体效应、电子效应和溶解效应有关[69]。WANG Xin课题组报道了与未修饰的铜纳米线相比,氨基酸修饰铜纳米线的乙烷和乙烯产量增加[70],密度泛函理论计算表明,氨基酸的—NH2和—COOH基团可促进中间体*CHO的稳定和转化,从而提高C2 产物的选择性。
具有疏水化学结构的硫醇可改善金属材料的表面润湿性能,从而提高其电催化CO2RR性能。WAKERLEY等[71]研究了用具有长疏水烃链的1-十八烷硫醇(ODT)修饰的分层结构Cu枝晶的CO2RR性能(图4(a))。经ODT改性后,铜枝晶表面变得疏水,水接触角由17°增至153°。在铜枝晶的ODT改性后,H2选择性由71%急剧降至10%,表明竞争性HER过程被显著抑制(图4(b))。同时,在ODT修饰后,Cu枝晶上大多数C1(如CO和CH4)和C2(如CH3COOH、C2H4和C2H5OH)产物的法拉第效率(EF)得以显著改善(图4(c)、4(d))。疏水性Cu枝晶增强的CO2RR性能归因于固液气(即Cu电非水电解质捕获的CO2气体)三相边界的产生。三相边界的存在使得H 只能来自本体溶液,然而CO2可以从各个方向输送到Cu表面,导致区域CO2浓度显著增加。因此,CO2RR中间体如*COOH和*CO的表面浓度显著增加,有助于C1和C2产物的形成。

图4 表面疏水及晶体缺陷对CO2还原反应的影响
Fig.4 Effect of surface hydrophobicity and crystal defects on the CO2RR
2.5 缺陷工程
晶体缺陷(Crystal Defects)是指晶体内部结构完整性受到破坏的所在位置。按其延展程度主要分为点缺陷、线缺陷、平面缺陷和体缺陷[72]。晶体缺陷可在催化剂合成和后处理过程中生成,甚至在电化学操作条件下就地生成。缺陷工程已被证明可有效调整电催化剂的表面组成、电荷分布、电子结构和活性位点,从而为影响反应途径和CO2RR的活性或选择性提供机会[73]。对于C2 产物,在含铜催化剂上引入缺陷有利于关键中间体的吸附。由于丰富的纳米缺陷有利于中间体的吸附和限制以及C—C偶联步骤,合成的多孔Cu纳米片对乙烯的法拉第效率高达83.2%(图4(e)~4(g))[74]。PARK等[75]利用氧等离子体辅助氮掺杂CuO,使CO2RR催化剂具有较高的C2 产物选择性和稳定的催化性能,在22 h内保持77%的多碳选择性。CuO表面的N2等离子体自由基产生了丰富的氧空位和晶界等缺陷,增加了N掺杂CuO中的催化位点,降低了*CO结合能。此外,原位X射线吸收近边结构分析表明,ON-CuO中的缺陷有利于C—C耦合产生C2 产物。
部分研究中,边缘和缺陷位置没有明确的表征(如精确的小面方向、配位数等)。相反,理论模拟常被用来建立简化的纳米晶模型和理解结构-性能关系。虽然其随机和混合的结构可能部分阻止更详细的表征,但仍有必要进一步了解这些参数对催化剂性能的影响及作用机理。优异的催化CO2RR性能主要归因于所含的晶界和缺陷打破了局部空间对称,调整了关键中间体的结合能。这些发现显著深化纳米催化剂中缺陷工程与CO2RR性能之间的关系,为提高整体能量效率提供解决方案。
3 提高铜基催化剂催化稳定性的设计策略
电催化剂在工作条件下的降解基本可体现在结构变化(或演化、转变、重构)上,破坏其固有活性或使某一活性位点的选择性发生移位,或使活性位点数量减少。原则上,重构行为主要通过2种方式发生:原子迁移和化学演化。原子迁移是指原子从一个位置转移到另一个位置,而化学演化可改变(电)化学反应中原子中心的氧化态或配位环境[76-77]。为解决这些问题,本节将重点讨论提高CO2RR铜基催化剂稳定性的设计策略。
3.1 掺杂和合金化处理
在催化剂基体中引入掺杂剂已被证明是重塑活性位点电子态和相关活性/选择性的有效方法[78]。在稳定性方面,元素掺杂可通过电荷转移或轨道重叠增强催化剂内部原子相互作用,以抑制特定元素的原子迁移。同时,掺杂剂可进一步改变金属中心的电子密度,以增加其抗开路电压氧化或负电压下的还原能力[79]。卤素元素(如氟、氯、溴)具有相对较强的电负性。因此,在金属材料表面掺杂卤素通常会改变其平均化学状态,从而改变其催化活性。LI Minhan课题组通过简单的水热过程合成了含卤素的前体Cu4(OH)6FCl纳米片(CuOHFCl NSs),然后在CO2RR条件下将其电化学活化为Cl掺杂的多孔Cu催化剂。催化剂在240 h以上的长期电催化中表现出优异的稳定性,主要归因于氯离子抑制了正价铜离子的还原,稳定了阳离子Cu0/Cu 活性位点(图5)[80]。此外,通过掺杂和合金化大幅提高活性位点的稳定性,还可以通过微调化学成分和元素分布提高催化剂内部的晶格强度。由于Cu 物种在加速C—C偶联反应方面具有重要作用,将Pd引入Cu2O纳米立方体以稳定Cu ,从而提高生成乙烯的选择性和稳定性,如在-1.1 V (vs. RHE)条件下,35 h内,EF最高达63.8%[81]。

图5 CuOHFCl-NSs的表征及其长时间的催化稳定性
Fig.5 Characterization of CuOHFCl-NSs and their long-term catalytic stability
除掺杂稳定催化剂活性位点的化学态外,催化剂在CO2RR过程中结构的稳定性也尤为重要。最近,OKATENKO课题组进行系统研究,揭示了CO2RR过程中合金对铜纳米催化剂结构演变和稳定性的影响[82]。采用种子生长法制备CuGa17纳米颗粒,首先在铜纳米颗粒表面沉积镓层,然后通过热汞化法制备CuGa17合金纳米催化剂。电化学测量表明,与铜纳米颗粒相比,CuGa17在产甲烷方面具有更高的稳定性(图6(a)~6(c))。然后,通过一系列基于非原位和原位技术的成分和结构表征,分析了稳定性增强的机制。原始铜纳米颗粒的重建由开路电压下生成的表面铜氧化物的溶解和CO2RR过程中可溶性瞬态铜物质的溶解/沉淀驱动,导致铜纳米颗粒形态显著变化和降解。对于合金纳米颗粒,由于镓的亲氧性较高,在CuGa17表面形成了较薄氧化镓层,从而阻止铜组分在开路电压下的氧化和相应铜元素在CO2RR中的溶解。另一方面,镓和铜之间的电子相互作用使晶格内原子键合更强,降低系统能量,抑制CuGa17纳米颗粒上原子的迁移和降解。

图6 表面合金化对铜催化剂稳定性的影响及N,N′-乙烯二溴菲对晶体形貌的影响
Fig.6 Effect of surface alloying on the stability of Cu catalysts and the effect of N,N′-ethylene-phenanthrolinium dibromide on crystal morphology
3.2 配体保护策略
在纳米颗粒合成过程中,利用配体调节纳米颗粒大小、形状和形态是可行方法[83]。在电催化中,配体通过电子效应或改变反应物/生成物的传质,在改变反应途径方面起重要作用[84]。其对稳定性也有重要影响,配体分子层可接受或提供电子,改变金属表面的形态,稳定CO2RR中间产物,防止金属催化剂聚集或降解,起到延长催化剂寿命的作用。聚多巴胺(PDA)作为一种常见配体,被广泛应用于稳定催化金属表面和调节界面性质[85]。如LIU Hui课题组最近合成了一种稳定的聚多巴胺修饰铜纳米线CuNWs@PDA,在CO2还原为CH4的过程中表现出显著的稳定性。由于PDA的保护,CuNWs@PDA在14 h内保持约30%的稳定甲烷选择性,而裸CuNWs只能稳定3 h。通过XPS分析,CuNWs@PDA的稳定性可归因于CuNWs和PDA之间的化学强结合,从而阻碍其形态演变并保持催化稳定性[86-87]。THEODOR等[88]报道了一种以N,N′-乙烯二溴菲为分子添加剂的纳米铜电极结构的新方法,C2 选择性最高达70%,稳定性超过40 h且催化剂表面形态没有显著变化。研究发现N,N′-乙烯二溴菲可发挥多种功能,包括促进生成立方体状的铜纳米结构、CO2RR中碳-碳偶联产品的形成,尤其是通过溴离子和胺与铜表面的配位作用实现了长达40 h电催化过程中催化剂形态的稳定(图6(d))。
但配体利用在提高CO2RR稳定性方面的作用不及其提高活性/选择性方面的表现。这可能是由于小分子配体本身在长期工作中不稳定所致。在这种情况下,使用更稳定的聚合物配体,如聚吡咯和有机COF,可更好地实现稳定任务[86,89]。
3.3 界面工程
具有丰富界面的杂化催化剂通过调节电子结构和产生协同活性位点来调节催化性能。通过原子连接或电荷转移效应产生的强界面相互作用也有助于活性位点的稳定,从而提高长期稳定性[90]。在串联催化设计中,具有良好界面连接的Cu-Au异质结能稳定工作90 h以生产乙醇[91]。通过设计Cu-CuAlO2-Al2O3催化剂,用原位生成的CuAlO2物质稳定乙烯电合成的高活性位点(图7(a)~7(c)),在H型电解池测试中获得了优良的稳定性[92]。在-61.1 mA/cm2条件下电解300 h后,乙烯的法拉第效率未明显下降(图7(d))。非原位结构分析表明,长期操作后CuAlO2界面保持不变。利用从头算DFT分子动力学(AIMD)模拟,通过在300 K下加入一个电子合理化模型的稳定性机制。理论计算结果证明Cu(100)/CuAlO2(001)和重组Cu(411)/CuAlO2(001)杂化结构中Cu(100)面的热力学稳定性高于裸Cu(100)模型。在非晶CuSiOx纳米管上实现了界面策略,并通过Cu—O—Si键建立了Cu与二氧化硅之间的强界面相互作用。由于强界面的存在,CuSiOx纳米管在工作条件下具有较高的抗重构性,因此具有良好的产甲烷稳定性。计算结果进一步证实了CuSiO3中的Cu—O键比CuGeO3和CuO模型中的Cu—O键更强,这与试验中CuSiOx纳米管的电化学稳定性相吻合。未来,在CO2RR铜基催化剂中实现强金属-载体相互作用,可进一步形成坚固界面,稳定活性位点[93]。

图7 Cu-CuAlO2-Al2O3样品的表征及性能测试
Fig.7 Characterizations and CO2RR Performance of Cu-CuAlO2-Al2O3 Samples
3.4 包覆和封装策略
为平衡多相催化活性和稳定性,用薄保护层包裹催化剂,如铠甲催化剂[94-95],已被证明是一种有效的方法。界面处的电荷转移和物质通过薄层的选择性渗透性使活性位点电子态重塑和质量输运条件发生改变[96]。同时,包覆可明显抑制纳米颗粒内部的原子扩散和烧结行为,从而减轻催化剂在工作条件下的降解。在某些情况下,阻碍杂质进入催化剂层也导致抗毒性更高。对于CO2RR,典型的保护层包括碳基材料(石墨烯、纳米管、多孔碳等)、六方氮化硼(h-BN)、金属氧化物和金属有机框架材料(MOF)。通过聚丙烯腈与铜前驱体的共解和随后的气固反应,准石墨碳壳外延生长在由非晶碳管支撑的铜纳米颗粒上(图8(a))[97]。在结构稳定性方面,无约束铜纳米颗粒经过CO2RR处理数小时后出现了严重的表面重构(图8(b)),同时乙烯的活性和选择性迅速下降。而受准石墨碳壳约束的铜纳米颗粒未出现表面粗糙或团聚等明显降解现象(图8(c))。通过进一步掺杂p-嵌段元素优化关键中间体在活性位点上的结合亲和力,受限的铜催化剂在膜电极中的乙烯选择性大于60%,寿命长达180 h(图8(d))。采用类似策略,用氧化石墨烯包裹五重孪晶铜纳米线,以保持其表面形态和产物中甲烷的选择性[98]。通过“瓶中两船”的架构设计,三元锌-银-氧纳米颗粒催化剂被限制在超高表面积碳球的纳米孔中[99]。由于抑制了纳米颗粒的分离和聚集,该催化剂在150 h内提供了CO生成的长期稳定性。

图8 包覆准石墨碳壳对铜纳米颗粒在CO2RR中结构稳定性的影响
Fig.8 Effect of encapsulating quasi-graphitic carbon shells on the structural stability of copper nanoparticles in CO2RR
此外,用2D h-BN纳米片封装可稳定Cu2O上的Cu 物质,这是由于亲电的h-BN能够降低Cu2O中电子密度,从而保护Cu—O键免受负电位下的电子攻击[100]。在连续运行过程中,Cu 态的持续存在和纳米约束效应使CO2RR稳定14 h,产物中乙烯/CO比例较高。
考虑到铜的(100)晶面和(111)晶面选择性差异明显,Drisdell课题组采用面选择性原子层沉积方法控制铜纳米晶体的表面暴露(图9(a))[101]。CO化学吸附的漫反射红外傅里叶变换光谱证实了Al2O3对铜(111)晶面的选择性包覆和(100)晶面面积/(111)晶面面积的比值增加(图9(b)),而诸多研究表明铜催化剂(100)晶面面积/(111)晶面面积的比值增加能显著促进乙烯的生成(图9(c))。从另一方面来说,Al2O3包覆有利于降低铜原子表面迁移率和纳米催化剂降解,使包覆后铜纳米晶体的结构稳定性和产物中乙烯的选择性均高于裸铜纳米晶体(图9(d))。此外,在Al-MOF基体中嵌入银纳米晶体可阻止长期CO2RR的烧结行为和活性损失[102]。包覆策略中,应当谨慎控制保护层的厚度、孔隙率等特征,避免过度阻断活性位点和限制活性物质的转移。

图9 铜纳米晶体面选择性原子层沉积过程及封装前后的性能比较
Fig.9 Facet-selective atomic layer deposition process for copper nanocrystals with a comparison of performance before and after encapsulation
4 结语及展望
1)综述了近年来在CO2RR用铜基催化剂优化设计策略方面取得的重要研究进展。从调控催化活性、选择性以及稳定性2方面,分别讨论了晶面工程、合金化处理、铜氧化态调节、催化剂表面功能化和缺陷工程等代表性调控策略的研究进展,探讨了电催化剂的核心参数(组成、微观结构、形貌、尺寸等)对催化剂性能的协同效应。
2)CO2还原反应(CO2RR)电催化剂在激活CO2分子和调整还原路径方面具有核心作用,从而获得高能量效率的理想产物。与CO和甲酸相比,通常在含铜催化剂上,CO2转化为烃类和C2 产物效率不理想,需通过提高法拉第效率和降低过电位进一步优化。通过将试验研究与理论计算相结合,揭示C2 深层催化机理和实时结构性能关系,为设计先进的CO2RR铜基催化剂提供科学指导。此外,对于工业电解,催化剂稳定性十分重要,应达到数千小时,同时具有理想的产物选择性和能量效率。然而目前CO2RR催化剂的最大持续时间仅限于数百小时。为解决这一问题,特别是在铜基催化剂上,对催化剂降解机理的理解非常迫切,其中通过动态现场原位技术对工作条件下动态演变的系统研究尤为重要。加强催化剂内部原子相互作用、引入保护层、增强催化剂-载体相互作用等措施的实施有助于提高催化剂稳定性[103]。利用独特的技术,如微流控合成,以低成本大规模生产工业应用催化剂的新方法也具有重要意义。在含金属催化剂的基础上,进一步探索开发廉价、环保、高性能的无金属催化剂(如碳纳米材料、有机催化剂等)。
3)为稳定二氧化碳还原反应(CO2RR)的活性位点,需削弱催化剂的结构转变。为实现这一目标,必须在原子迁移过程中增加更多热力学和动力学难题,如通过加强晶格内原子间的结合力,或表面包裹以物理方式减缓原子扩散。这可通过如掺杂/合金化、配体保护、界面构建和封装等策略实现。其中,界面构建和封装可能是延长催化剂寿命最有前景的方法。作为参考,在工业热催化(如费托合成)中,负载型催化剂已被广泛应用。底物相与活性相之间的强烈界面相互作用使这些催化剂对恶劣的反应条件具有很高的形变抵抗强度。将这一理念应用于设计CO2RR电催化剂时,由于其选择性对化学成分敏感,面临挑战。在封装/限制策略中,碳基材料通常用作保护层。对碳层结构的调节可能性,包括厚度、孔隙率、渗透性和表面特性,为平衡CO2RR催化剂的活性/选择性和稳定性带来机会。直接在催化剂-电极顶部沉积保护层也有积极作用。此外,需进一步稳定用于C2 生产的含铜催化剂。
[1] GRIM R Gary, HUANG Zhe, GUARNIERI Michael T, et al. Tra-nsforming the carbon economy:Challenges and opportunities in the convergence of low-cost electricity and reductive CO2 utilization [J]. Energy &Environmental Science, 2020, 13(2): 472-494.
[2] WANG Liming, CHEN Wenlong, ZHANG Doudou, et al. Surface strategies for catalytic CO2 reduction: From two-dimensional materials to nanoclusters to single atoms [J]. Chemical Society Reviews, 2019, 48(21): 5310-5349.
[3] BIRDJA Yuvraj Y, PéREZ-GALLENT Elena, FIGUEIREDO Marta C, et al. Advances and challenges in understanding the electrocatalytic conversion of carbon dioxide to fuels [J]. Nature Energy, 2019, 4(9): 732-745.
[4] HAN Na, DING Pan, HE Le, et al. Promises of main group met-al-based nanostructured materials for electrochemical CO2 reduction to formate [J]. Advanced Energy Materials, 2020, 10(11): 1902338.
[5] HUANG Zhe, GRIM R Gary, SCHAIDLE Joshua A, et al. The economic outlook for converting CO2 and electrons to molecules[J]. Energy &Environmental Science, 2021, 14(7): 3664-3678.
[6] SPURGEON Joshua M, KUMAR Bijandra. A comparative technoeconomicanalysis of pathways for commercial electrochemical CO2 reduction to liquid products [J]. Energy &Environmental Science, 2018, 11(6): 1536-1551.
[7] ZHANG Jiawei, SEWELL Christopher D, HUANG Hongwen, et al. Closing the anthropogenic chemical carbon cycle toward a sustainable future via CO2 valorization [J]. Advanced Energy Materials, 2021, 11(47): 2102767.
[8] JIN S, HAO Z, ZHANG K, et al. Advances andchallenges for the electrochemical reduction of CO2 to CO: From fundamentals to industrialization [J]. Angewandte Chemie-international Edition, 2021, 60(38): 20627-20648.
[9] LIANG Feng, ZHANG Kaiwen, ZHANG Lei, et al. Recent development of electrocatalytic CO2 reduction application to energy conversion [J]. Small, 2021, 17(44): 2100323.
[10] NITOPI S, BERTHEUSSEN E, SCOTT S B, et al. Progress and perspectives of electrochemical CO2 reduction on copper in aqueous electrolyte [J]. Chemical Reviews, 2019, 119(12): 7610-7672.
[11] ZHU Shangqian, DELMO Ernest Pahuyo, LI Tiehuai, et al. Recent advances in catalyst structure and composition engineering strategies for regulating CO2 electrochemical reduction [J]. Advanced Materials, 2021, 33(50): 2005484.
[12] ZHONG Y, WANG S, LI M, et al. Rational design of copper-based electrocatalysts and electrochemical systems for CO2 reduction: From active sites engineering to mass transfer dynamics [J]. Materials Today Physics, 2021, 18:100354.
[13] LI K, WANG W, ZHENG H, et al. Visualizing highly selective electrochemical CO2 reduction on a molecularly dispersed catalyst [J]. Materials Today Physics, 2021, 19:100427.
[14] PAN Fuping, YANG Yang. Designing CO2 reduction electrode materials by morphology and interface engineering [J]. Energy &Environmental Science, 2020, 13(8): 2275-2309.
[15] LI Fengwang, LI Yuguang, WANG Ziyun,et al. Cooperative CO2-to-ethanol conversion via enriched intermediates at molecule-metal catalyst interfaces [J]. Nature Catalysis, 2020, 3(1): 75-82.
[16] PETER Sebastian C. Reduction of CO2 to chemicals and fuels: A solution to global warming and energy crisis [J]. ACS Energy Letters, 2018, 3(7): 1557-1561.
[17] LI Kan, PENG Bosi, PENG Tianyou. Recent advances in heterogeneous photocatalytic CO2 conversion to solar fuels [J]. ACS Catalysis, 2016, 6(11): 7485-7527.
[18] BENSON E E, KUBIAK C P, SATHRUM AJ, et al. Electrocatalytic and homogeneous approaches to conversion of CO2 to liquid fuels [J]. Chemical Society Reviews, 2009, 38(1): 89-99.
[19] ZHENG Y, VASILEFF A, ZHOU X, et al. Understanding the-roadmap for electrochemical reduction of CO2 to multi-carbon oxygenates and hydrocarbons on copper-based catalysts [J]. Journal of the American Chemical Society, 2019, 141(19): 7646-7659.
[20] ZHANG Qiyan, ZHAO Qinfu, LIANG Ximin, et al. Computational studies of electrochemical CO2 reduction on chalcogen doped Cu4 cluster [J]. International Journal Of Hydrogen Energy, 2018, 43(21): 9935-9942.
[21] LIU Min, LIU Mengxia, WANG Xiaoming, et al. Quantum-dot-derived catalysts for CO2 reduction reaction [J]. Joule, 2019, 3(7): 1703-1718.
[22] NITOPI S, BERTHEUSSEN E, SCOTT S B, et al. Progress andperspectives of electrochemical CO2 reduction on copper in aqueous electrolyte [J]. Chemical Reviews, 2019, 119(12): 7610-7672.
[23] ZHANG L, ZHAO Z J, GONG J. Nanostructured materials for heterogeneous electrocatalytic CO2 reduction and their related reaction mechanisms [J]. Angewandte Chemie-international Edition, 2017, 56(38): 11326-11353.
[24] SUN Zhenyu, MA Tao, TAO Hengcong, et al. Fundamentals andchallenges of electrochemical CO2 reduction using two-dimensional materials [J]. Chem, 2017, 3(4): 560-587.
[25] ZHU D D, LIU J L, QIAO S Z. Recent advances in inorganic heterogeneous electrocatalysts for reduction of carbon dioxide [J]. Advanced Materials, 2016, 28(18): 3423-3452.
[26] JIN H Y, GUO C X, LIU X, et al. Emerging two-dimensional nanomaterials for electrocatalysis [J]. Chemical Reviews, 2018, 118(13): 6337-6408.
[27] WANG Yifei, HAN Peng, LV Ximeng, et al. Defect and inter-face engineering for aqueous electrocatalytic CO2 reduction [J]. Joule, 2018, 2(12): 2551-2582.
[28] DURST J, RUDNEV A, DUTTA A, et al. Electrochemical CO2 reduction:A critical view on fundamentals, materials and applications [J]. Chimia, 2015, 69(12): 769-776.
[29] FAN L, XIA C, YANG F, et al. Strategies in catalysts and electrolyzer design for electrochemical CO2 reduction toward C2 products [J]. Science Advances, 2020, 6(8): eaay3111.
[30] OOKA H, FIGUEIREDO M C, KOPER M T M. Competition between hydrogen evolution and carbon dioxide reduction on copper electrodes in mildly acidic media [J]. Langmuir, 2017, 33(37): 9307-9313.
[31] NIE X, ESOPI M R, JANIK M J, et al. Selectivity of CO2 reduction on copper electrodes:The role of the kinetics of elementary steps [J]. Angewandte Chemie-international Edition, 2013, 52(9): 2459-2462.
[32] PETERSON Andrew A, ABILD-PEDERSEN Frank, STUDT Felix, et al. How copper catalyzes the electroreduction of carbon dioxide into hydrocarbon fuels [J]. Energy &Environmental Science, 2010, 3(9): 1311-1315.
[33] MELCHAEVA O, VOYAME P, BASSETTO V C, et al. Electrochemical reduction of protic supercritical CO2 on copper electrodes [J]. ChemSusChem, 2017, 10(18): 3660-3670.
[34] LEE Seunghwa, OCON Joey D, SON Youngil, et al. Alkaline CO2 electrolysis toward selective and continuous HCOO-production over SnO2 nanocatalysts [J]. Journal of Physical Chemistry C, 2015, 119(9): 4884-4890.
[35] MA Sichao, SADAKIYO Masaaki, LUO Raymond, et al. One-step electrosynthesis of ethylene and ethanol from CO2 in an alkaline electrolyzer [J]. Journal of Power Sources, 2016, 301: 219-228.
[36] YANG K, KAS R, SMITH W A. Insitu infrared spectroscopy reveals persistent alkalinity near electrode surfaces during CO2 electroreduction [J]. Journal of the American Chemical Society, 2019, 141(40): 15891-15900.
[37] LIU L, FAN W, ZHAO X, et al. Surface dependence of CO2 adsorption on Zn2GeO4[J]. Langmuir, 2012, 28(28): 10415-10424.
[38] HANDOKO Albertus D, WEI Fengxia,JENNDY, et al. Understanding heterogeneous electrocatalytic carbon dioxide reduction through operando techniques [J]. Nature Catalysis, 2018, 1(12): 922-934.
[39] HORI Yoshio, MURATA Akira, TAKAHASHI Ryutaro. Forma-tion of hydrocarbons in the electrochemical reduction of carbon dioxide at a copper electrode in aqueous solution [J]. Journal of the Chemical Society, 1989, 85(8): 2309-2326.
[40] LI Yawei, SUN Qiang. Recent advances in breaking scaling relations for effective electrochemical conversion of CO2 [J]. Advanced Energy Materials, 2016, 6(17):1600463.
[41] FEASTER Jeremy T, SHI Chuan, CAVE Etosha R, et al. Understanding selectivity for the electrochemical reduction of carbon dioxide to formic acid and carbon monoxide on metal electrodes [J]. ACS Catalysis, 2017, 7(7): 4822-4827.
[42] KORTLEVER R, SHEN J, SCHOUTEN K J, et al. Catalysts andreaction pathways for the electrochemical reduction of carbon dioxide [J]. Journal of Physical Chemistry Letters, 2015, 6(20): 4073-4082.
[43] LIU X, XIAO J, PENG H, et al. Understanding trends in electrochemical carbon dioxide reduction rates [J]. Nature Communications, 2017, 8: 15438.
[44] VASILEFF Anthony, XU Chaochen, JIAO Yan, et al. Surface andinterface engineering in copper-based bimetallic materials for selective CO2 electroreduction [J]. Chem, 2018, 4(8): 1809-1831.
[45] MONTOYA J H, SHI C, CHAN K, et al. Theoretical insights into a CO dimerization mechanism in CO2 electroreduction [J]. Journal of Physical Chemistry Letters, 2015, 6(11): 2032-2037.
[46] PÉREZ-GALLENT Elena, FIGUEIREDO Marta C, CALLE-VALLEJO Federico, et al. Spectroscopic observation of a hydrogenated CO dimer intermediate during CO2 reduction on Cu(100) electrodes [J]. Angewandte Chemie-international Edition, 2017, 56(13): 3621-3624.
[47] TING Louisa Rui Lin, YEO Boon Siang. Recent advances in understanding mechanisms forthe electrochemical reduction of carbon dioxide [J]. Current Opinion in Electrochemistry, 2018, 8: 126-134.
[48] LEDEZMA YANEZ Isis, GALLENT Elena Pérez, KOPER Marc T M, et al. Structure-sensitive electroreduction of acetaldehyde to ethanol on copper and its mechanistic implications for CO and CO2 reduction [J]. Catalysis Today, 2016, 262: 90-94.
[49] GARZA Alejandro J, BELL Alexis T, HEAD-GORDON Mart-in. Mechanism of CO2 reduction at copper surfaces: Pathways to C2 products [J]. ACS Catalysis, 2018, 8(2): 1490-1499.
[50] TODOROVA Tanya K, SCHREIBER Moritz W, FONTECA-VE Ma-rc. Mechanistic understanding of CO2 reduction reaction(CO2RR) toward multicarbon products by heterogeneous copper-based catalysts [J]. ACS Catalysis, 2020, 10(3): 1754-1768.
[51] KIBRIA Md Golam, EDWARDS Jonathan P, GABARDO Christine M, et al. Electrochemical CO2 reduction into chemical feedstocks: From mechanistic electrocatalysis models to system design [J]. Advanced Materials, 2019, 31(31): 1807166.
[52] YANG Tung Han, SHI Yifeng, JANSSEN Annemieke, et al. Su-rface capping agents and their roles in shape-controlled synthesis of colloidal metal nanocrystals [J]. Angewandte Chemie-international Edition, 2020, 59(36): 15378-15401.
[53] SHI Y, LYU Z, ZHAOM, et al. Noble-metal nanocrystals wi-th controlled shapes for catalytic and electrocatalytic applications [J]. Chemical Reviews, 2021, 121(2): 649-735.
[54] DE GREGORIO Gian Luca, BURDYNY Thomas, LOIUDICE An- na, et al. Facet-dependent selectivity of Cu catalysts in electrochemical CO2 reduction at commercially viable current densities [J]. ACS Catalysis, 2020, 10(9): 4854-4862.
[55] JIANG Kun, SANDBERG Robert B, AKEY Austin J, et al. Me-tal ion cycling of Cu foil for selective C—C coupling in electrochemical CO2 reduction [J]. Nature Catalysis, 2018, 1(2): 111-119.
[56] LEE C W, YANG K D, NAM D H, et al. Defining amaterials database for the design of copper binary alloy catalysts for electrochemical CO2 conversion[J]. Advanced Materials, 2018, 30(42): e1704717.
[57] SANKAR Meenakshisundaram, DIMITRATOS Nikolaos, MIEDZIAK Peter J, et al. Designing bimetallic catalysts for a green and sustainable future [J]. Chemical Society Reviews, 2012, 41(24): 8099-8139.
[58] YU D, GAO L, SUN T, et al. Strain-stabilized metastable face-centered tetragonal gold overlayer for efficient CO2 electroreduction [J]. Nano Letters, 2021, 21(2): 1003-1010.
[59] LI Mu, WANG Junjie, LI Peng, et al. Mesoporous palladi-um-copper bimetallic electrodes for selective electrocatalyticreduction of aqueous CO2 to CO [J]. Journal of Materials Chemistry A, 2016, 4(13): 4776-4782.
[60] ROY C, GALIPAUD J, FRÉCHETTE-VIENS L, et al. CO2 electroreduction at AuxCu1-x obtained by pulsed laser deposition in O2 atmosphere [J]. Electrochim Acta, 2017, 246: 115-122.
[61] MA S, SADAKIYO M, HEIMA M, et al. Electroreduction ofcarbon dioxide to hydrocarbons using bimetallic Cu-Pd catalysts with different mixing patterns [J]. Journal of the American Chemical Society, 2017, 139(1): 47-50.
[62] ZHONG M, TRAN K, MIN Y, et al. Accelerated discovery of CO2 electrocatalysts using active machine learning [J]. Nature, 2020, 581(7807): 178-183.
[63] WANG Jiali, TAN Huiying, ZHUyanping, et al. Linking thedynamic chemical state of catalysts with the product profile of electrocatalytic CO2 reduction [J]. Angewandte Chemie-International Edition, 2021, 60(32): 17254-17267.
[64] WU Zhizheng, GAO Feiyue, GAO Minrui. Regulating the oxidation state of nanomaterials for electrocatalytic CO2 reduction [J]. Energy &Environmental Science, 2021, 14(3): 1121-1139.
[65] POPOVIC S, SMILJANIC M, JOVANOVIC P, et al. Stability anddegradation mechanisms of copper-based catalysts for electrochemical CO2 reduction [J]. Angewandte Chemie-international Edition, 2020, 59(35): 14736-14746.
[66] MISTRY Hemma, VARELA Ana Sofia, BONIFACIO Cecile S, et al. Highly selective plasma-activated copper catalysts for carbon dioxide reduction to ethylene [J]. Nature Communications, 2016, 7(1): 12123.
[67] AR N-AIS Rosa M, SCHOLTEN Fabian, KUNZE Sebastian, et al. The role of in situ generated morphological motifs and Cu(I) species in C2 product selectivity during CO2 pulsed electroreduction [J]. Nature Energy, 2020, 5(4): 317-325.
N-AIS Rosa M, SCHOLTEN Fabian, KUNZE Sebastian, et al. The role of in situ generated morphological motifs and Cu(I) species in C2 product selectivity during CO2 pulsed electroreduction [J]. Nature Energy, 2020, 5(4): 317-325.
[68] CHEN Jiayi, WANG Lei. Effects of thecatalyst dynamic changes and influence of the reaction environment on the performance of electrochemical CO2 reduction [J]. Advanced Materials, 2021, 34(25): e2103900.
[69] LU Linfang, ZOU Shihui, FANG Baizeng. The Criticalimpacts of ligands on heterogeneous nanocatalysis: A review [J]. ACS Catalysis, 2021, 11(10): 6020-6058.
[70] XIE Mingshi, XIA Baoyu, LI Yawei, et al. Amino acid modified copper electrodes for the enhanced selective electroreduction of carbon dioxide towards hydrocarbons [J]. Energy &Environmental Science, 2016, 9(5): 1687-1695.
[71] WAKERLEY David, LAMAISON Sarah, OZANAM François, et al. Bio-inspired hydrophobicity promotes CO2 reduction on a Cu surface [J]. Nature Materials, 2019, 18(11): 1222-1227.
[72] JIAO Shilong, FU Xianwei, ZHANG Li, et al. Point-defect-optimized electron distribution for enhanced electrocatalysis: Towards the perfection of the imperfections [J]. Nano Today, 2020, 31: 100833.
[73] JIAO Shilong, FU Xianwei, WANG Shuangyin, et al. Perfecting electrocatalysts via imperfections: Towards the large-scale deployment of water electrolysis technology [J]. Energy &Environmental Science, 2021, 14(4): 1722-1770.
[74] ZHANG B, ZHANG J, HUA M, et al. Highly electrocatalytic ethylene production from CO2 on nanodefective Cu nanosheets [J]. Journal of the American Chemical Society, 2020, 142(31): 13606-13613.
[75] PARK Dong Gyu, CHOI Jae Won, CHUN Hoje, et al. Incr-easing CO binding energy and defects by preserving Cu oxidation state via O2-plasma-assisted N doping on CuO enables high C2 selectivity and long-term stability in electrochemical CO2 reduction[J]. ACS Catalysisysis, 2023, 13(13): 9222-9233.
[76] WANG W, DUAN J, LIU Y, et al. Structural reconstruction of catalysts in electroreduction reaction: Identifying, understanding, and manipulating [J]. Advanced Materials, 2022, 34(52): e2110699.
[77] ZHANG Wenbiao, YANG Yang, TANG Yi, et al. In-situ reconstruction of catalysts in cathodic electrocatalysis: New insights into active-site structures and working mechanisms [J]. Journal of Energy Chemistry, 2022, 70: 414-436.
[78] ZHOU Y, CHE F, LIU M, et al. Dopant-induced electron localization drives CO2 reduction to C2 hydrocarbons [J]. Nature Chemistry, 2018, 10(9): 974-980.
[79] JIANG Yunling, SHAN Jieqiong, WANG Pengtang, et al. Stabilizing oxidation state of SnO2 for highly selective CO2 electroreduction to formate at large current densities [J]. ACS Catalysis, 2023, 13(5): 3101-3108.
[80] LI Minhan, MA Yuanyuan, CHEN Jun,et al. Residual chlorine induced cationic active species on a porous copper electrocatalyst for highly stable electrochemical CO2 reduction to C2 [J]. Angewandte Chemie-international Edition, 2021, 60(20): 11487-11493.
[81] XIAO Difei, BAO Xiaolei, ZHANGMinghui, et al. Stabilizing Cu2O for enhancing selectivity of CO2 electroreduction to C2H4 with the modification of Pd nanoparticles [J]. Chemical Engineering Journal, 2023, 452: 139358.
[82] OKATENKO V, LOIUDICE A, NEWTON M A, et al. Alloying as astrategy to boost the stability of copper nanocatalysts during the electrochemical CO2 reduction reaction [J]. Journal of the American Chemical Society, 2023, 145(9): 5370-5383.
[83] BHATTACHARJEE Kaustav, PRASAD Bhagavatula L V. Surface functionalization of inorganic nanoparticles with ligands: A necessary step for their utility [J]. Chemical Society Reviews, 2023, 52(8): 2573-2595.
[84] ZHU Q, MURPHY C J, BAKER L R. Opportunities for electrocatalytic CO2 reduction enabled by surface ligands [J]. Journal of the American Chemical Society, 2022, 144(7): 2829-2840.
[85] MISHRA Biswajit, GHOSH Dibyajyoti, TRIPATHI Bijay P. Finely dispersed AgPd bimetallic nanoparticles on a polydopamine modified metal organic framework for diverse catalytic applications [J]. Journal of Catalysis, 2022, 411: 1-14.
[86] LIU Hui, XIANG Kaisong, LIU Yucheng, et al. Polydopaminefunctionalized Cu nanowires for enhanced CO2 electroreduction towards methane [J]. ChemElectroChem, 2018, 5(24): 3991-3999.
[87] HUANG J, HORMANN N, OVEISI E, et al. Potential-induced nanoclustering of metallic catalysts during electrochemical CO2 reduction [J]. Nature Communications, 2018, 9(1): 3117.
[88] THEVENON Arnaud, ROSAS-HERN NDEZ Alonso, PETE-RS Jonas C, et al. In-situ nanostructuring and stabilization of polycrystalline copper by an organic salt additive promotes electrocatalytic CO2 reduction to ethylene [J]. Angewandte Chemie-international Edition, 2019, 58(47): 16952-16958.
NDEZ Alonso, PETE-RS Jonas C, et al. In-situ nanostructuring and stabilization of polycrystalline copper by an organic salt additive promotes electrocatalytic CO2 reduction to ethylene [J]. Angewandte Chemie-international Edition, 2019, 58(47): 16952-16958.
[89] PERIASAMY A P, RAVINDRANATH R, SENTHIL KUMAR S
M, et al. Facet- and structure-dependent catalytic activity of cuprous oxide/polypyrrole particles towards the efficient reduction of carbon dioxide to methanol [J]. Nanoscale, 2018, 10(25): 11869-11880.
[90] DAI L, QIN Q, WANG P, et al. Ultrastable atomic copper nanosheets for selective electrochemical reduction of carbon dioxide [J]. Science Advances, 2017, 3(9): e1701069.
[91] KUANG S, SU Y, LI M, et al. Asymmetrical electrohydrogena-tion of CO2 to ethanol with copper-gold heterojunctions [J]. Proceedings of the National Academy of Sciences of the United States of America 2023, 120(4): e2214175120.
[92] LIU Fei, REN Xixi, ZHAO Jun, et al. Inhibiting sulfur dissolution and enhancing activity of SnS for CO2 electroreduction via electronic state modulation[J]. ACS Catalysis, 2022, 12(21): 13533-13541.
[93] LI Zhao, WU Rui, ZHAO Lei, et al. Metal-support interactions in designing noble metal-based catalysts for electrochemical CO2 reduction: Recent advances and future perspectives [J]. Nano Research, 2021, 14(11): 3795-3809.
[94] WANG Bin, SRINIVAS Katam, LIU Yanfang, et al. N-doped CNTs capped with carbon layer armored CoFe alloy as highly stable bifunctional catalyst for oxygen electrocatalysis [J]. Nano Research, 2022, 15(5): 3971-3979.
[95] QIAO Li, WANG Xingkun, XU Ren, et al. Nitrogen-doped carbon shell armored ′Janus′ Co/Co9S8 heterojunction as robust bi-functional oxygen reduction reaction/oxygen evolution reaction catalysts in seawater-based rechargeable Zn-air batteries [J]. Materials Today Energy, 2023, 37: 101398.
[96] GAWANDE Manoj B, GOSWAMI Anandarup, ASEFA Tewo-dros, et al. Core-shell nanoparticles: Synthesis and applications in catalysis and electrocatalysis [J]. Chemical Society Reviews, 2015, 44(21): 7540-7590.
[97] KIM J Y, HONG D, LEE J C, et al. Quasi-graphitic carbon shell-induced Cu confinement promotes electrocatalytic CO2 reduction toward C2 products[J]. Nature Communications, 2021, 12(1): 3765.
[98] PELZ P M, GROSCHNER C, BRUEFACH A, et al. Simultaneoussuccessive twinning captured by atomic electron tomography [J]. ACS Nano, 2022, 16(1): 588-596.
[99] ZHANG Z, WEN G, LUO D, et al. "Twoships in a bottle" design for Zn-Ag-O catalyst enabling selective and long-lasting CO2 electroreduction [J]. Journal of the American Chemical Society, 2021, 143(18): 6855-6864.
[100] ZHOU Yixiang, YAO Yebo, ZHAO Rui, et al. Stabilization of Cu via strong electronic interaction for selective and stable CO2 electroreduction [J]. Angewandte Chemie-international Edition, 2022, 61(31): e202205832.
[101] O′BRIEN Colin P, MIAO Rui Kai, LIU Shijie, et al. Single pass CO2 conversion exceeding 85% in the electrosynthesis of multicarbon products via local CO2 regeneration [J]. ACS Energy Letters, 2021, 6(8): 2952-2959.
[102] GUNTERN Y T, PANKHURST J R, VAVRA J, et al. Nanocrystal/metal-organic framework hybrids as electrocatalytic platforms for CO2 conversion [J]. Angewandte Chemie-international Edition, 2019, 58(36): 12632-12639.
[103] ZHANG Jiawei, YUAN Yuliang, GAO Lei, et al. Stabilizing Pt-based electrocatalysts for oxygen reduction reaction: Fundamental understanding and design strategies [J]. Advanced Materials, 2021, 33(20): 2006494.
Design strategies for copper-based catalysts in electrochemical reduction of carbon dioxide

移动阅读