卤族元素对湿法脱硫系统汞释放影响
0 引 言
据联合国环境保护署数据显示,2015年全球汞排放量超过7 000 t,人为活动是重要的汞排放源,造成汞排放量占全球汞排放量的30%[1],其来源主要包括手工和小规模金矿开采、有色金属生产、燃煤火电站等工业活动。我国能源消耗结构中煤炭消费占比较高,尤其是发电行业。2021年全球范围燃煤发电平均占全途径发电量比例的35%,而我国这一比例达63%,同期发电量达4.9万亿kWh,远超世界平均值[2]。我国煤炭汞含量偏高,平均含汞质量分数约为0.22 mg/kg,超世界煤炭汞平均含量2倍以上[3-4],煤炭的高位消耗导致燃煤成为最重要的大气汞排放源之一。LIANG等[5]利用EE-MRIO(Environmentally Extended Multiregional Input-Output)模型构建虚拟大气汞排放网络,对国内大气汞排放情况进行全方位立体分析,得出2007年我国人为汞排放量达794.9 t,其中以火力发电为排放源引起的汞排放量为357.7 t,占比超47% 。
燃煤电站通常有选择性催化还原脱硝(Selective Catalytic Reduction,SCR)、静电除尘器(Electrostatic Precipitators,ESP)、湿法脱硫(Wet Flue Gas Desulfurization,WFGD)等常规污染物排放控制设备(Air Pollution Control Devices,APCDs)用于脱除燃煤产生的常规污染物[6],如氮氧化物(NOx)、二氧化硫(SO2)、颗粒物(PM)。烟气中汞以3种形式存在,包括元素态(Hg0)、氧化态(Hg2 )和颗粒态(HgP)。燃煤烟气经APCDs处理后除满足超低排放要求外,对控制烟气汞排放也有一定作用[7-12]。
近几年,为满足更严格的大气排放控制标准,加装湿式静电除尘器(Wet Electrostatic Precipitators,WESP),控制燃煤超细颗粒物的排放,如PM2.5和PM10,截至2020年底,全国范围内达到超低排放限制的煤电机组约9.5亿kW,约占全国煤电总装机容量88%[13]。WESP在脱除PM2.5和PM10的过程中对包括汞在内的重金属具有协同脱除作用[6,14-16],对国内较普遍的单机容量300 MW机组超低排放改造前后汞的排放特性进行对比,发现经超低排放改造后烟气汞排放明显降低,燃煤电厂烟气综合脱汞效率提高1.5倍[17]。除燃煤烟气Hg0被APCDs直接脱除外,氧化态汞较易被WFGD系统高效脱除,脱除效率超90%[18]。然而,WFGD系统浆液内大量水溶态的Hg2 会与浆液中的还原性物质反应,被还原的Hg0可能再次释放到烟气中。研究表明,经WFGD系统脱硫塔内浆液洗涤后,烟气中的汞浓度不降反升[9,14,19-21],个别机组烟气中Hg0质量浓度经WFGD系统后大幅提高,由0.13 μg/m3 升至0.62 μg/m3。关于WFGD系统引起汞再释放的行为已有较多报道,研究认为脱硫浆液内部存在未氧化的S(Ⅳ)组分具有较强的还原性,是导致Hg2 还原为Hg0再次释放到烟气中的主要因素[22]。同时,系统反应温度、pH和![]() 浓度等多种因素影响Hg0再释放的机理和强度[23-27]。此外,对于WFGD系统实际运行,脱硫塔塔内使用浆液循环易造成水溶性组分(如Cl)堆积,这些组分无法随石膏生产过程脱除,积累在脱硫浆液中的Cl会显著影响汞的释放浓度[25,28]。关于卤族元素对WFGD系统内汞释放的深入研究相对较少,因此,系统研究包含Cl在内的卤族元素对WFGD系统浆液汞释放行为的影响具有重要意义。
浓度等多种因素影响Hg0再释放的机理和强度[23-27]。此外,对于WFGD系统实际运行,脱硫塔塔内使用浆液循环易造成水溶性组分(如Cl)堆积,这些组分无法随石膏生产过程脱除,积累在脱硫浆液中的Cl会显著影响汞的释放浓度[25,28]。关于卤族元素对WFGD系统内汞释放的深入研究相对较少,因此,系统研究包含Cl在内的卤族元素对WFGD系统浆液汞释放行为的影响具有重要意义。
1 试验仪器及方法
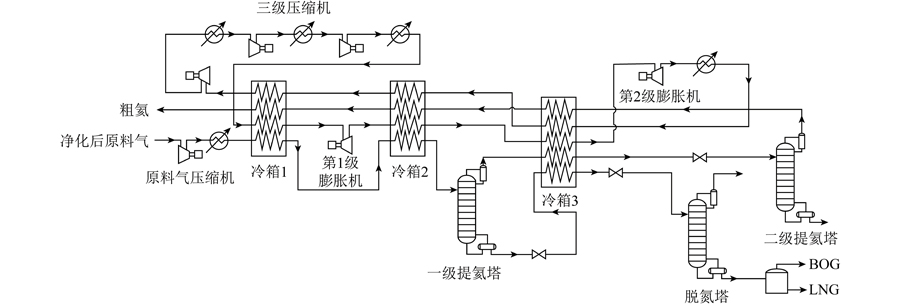
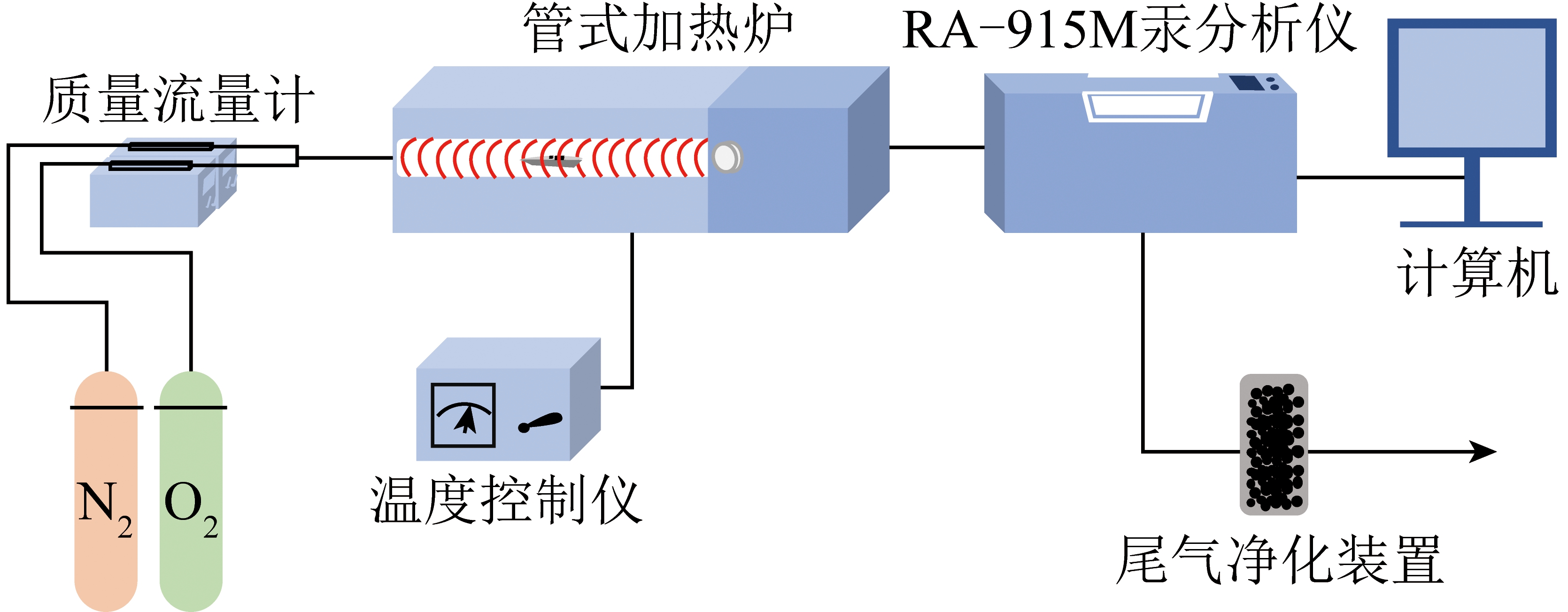
实验室搭建WFGD系统卤族元素汞释放影响评价试验系统,如图1所示。系统主要包括核心反应模块、测试模块和辅助模块,其中辅助模块包含供气、尾气处理过程。单组试验前配置模拟脱硫液,由于![]() 受氧气影响较大,为更好评价卤族元素对汞释放的影响,核心反应模块内采用磨砂口分散进气、底部旋转搅拌等措施,增强进气分散性,确保气液充分混合。同时,模拟脱硫液配制加入NaAC-HAC缓冲剂控制反应过程中浆液pH,减少反应过程中浆液pH变化对汞释放行为的影响[23,29],在整个反应过程中对浆液pH进行在线监测。此外,基于弱酸性的反应环境,试验中卤族元素仅包含Cl、Br和I元素,并未考虑F元素的影响,这主要是由于在酸性条件下,F离子与H离子结合生成具有强腐蚀性的HF,会对整个试验系统造成较大损坏。采用高纯N2作为载气(流量为1 L/min),将释放的汞输送到测试模块内。测试模块采用原子吸收法测量气相汞浓度,该方法利用气相Hg0对波长253.7 nm紫外光的吸收特性,对气相Hg0浓度进行测量,由于此方法受水蒸气影响较大,在进入汞蒸气在线检测仪(Mercury Vapor Monitor VM3000,德国Mercury Instrument公司)前需经硅胶干燥除水过程。试验系统管路均缠绕加热带,避免水蒸气凝结,加热温度保持在120 ℃。尾气处理依次通过质量分数5%的KMnO4溶液和活性炭,用于脱除尾气中的Hg0,避免造成环境污染。
受氧气影响较大,为更好评价卤族元素对汞释放的影响,核心反应模块内采用磨砂口分散进气、底部旋转搅拌等措施,增强进气分散性,确保气液充分混合。同时,模拟脱硫液配制加入NaAC-HAC缓冲剂控制反应过程中浆液pH,减少反应过程中浆液pH变化对汞释放行为的影响[23,29],在整个反应过程中对浆液pH进行在线监测。此外,基于弱酸性的反应环境,试验中卤族元素仅包含Cl、Br和I元素,并未考虑F元素的影响,这主要是由于在酸性条件下,F离子与H离子结合生成具有强腐蚀性的HF,会对整个试验系统造成较大损坏。采用高纯N2作为载气(流量为1 L/min),将释放的汞输送到测试模块内。测试模块采用原子吸收法测量气相汞浓度,该方法利用气相Hg0对波长253.7 nm紫外光的吸收特性,对气相Hg0浓度进行测量,由于此方法受水蒸气影响较大,在进入汞蒸气在线检测仪(Mercury Vapor Monitor VM3000,德国Mercury Instrument公司)前需经硅胶干燥除水过程。试验系统管路均缠绕加热带,避免水蒸气凝结,加热温度保持在120 ℃。尾气处理依次通过质量分数5%的KMnO4溶液和活性炭,用于脱除尾气中的Hg0,避免造成环境污染。

图1 卤族元素影响汞释放试验系统
Fig.1 Experiment system of halogen elements influence on Hg emission
为考察单一影响因素下卤族元素对汞释放的影响,试验所用模拟脱硫浆液仅添加S(Ⅳ)、卤族元素阴离子和汞,其中还原性S(Ⅳ)和卤族元素阴离子分别通过溶解![]() 和卤族元素钠盐方式添加,浆液中的汞源采用汞标准溶剂(主要成分为Hg(NO3)2)利用微量注射器定量添加到三口烧瓶内,汞质量浓度为100 μg/L。
和卤族元素钠盐方式添加,浆液中的汞源采用汞标准溶剂(主要成分为Hg(NO3)2)利用微量注射器定量添加到三口烧瓶内,汞质量浓度为100 μg/L。
2 结果与讨论
2.1 卤族元素种类对汞释放影响
WFGD系统中的还原性S(Ⅳ)是造成脱硫浆液内部Hg2 释放的主要原因[30-32],如![]() 和
和 会与Hg2 发生氧化还原反应,导致已被捕获的烟气和保留在脱硫浆液内部的可溶态Hg2 被还原为不可溶的Hg0,重新释放到烟气中,进而随烟气排放进入大气,主要反应途径见式(1)。在反应温度50 ℃、pH为5、卤族元素物质的量浓度为20 mmol/L条件下,考察Cl、Br和I元素对汞释放影响,结果如图2所示。经90 min反应后,可以看到Cl、Br和I三种卤族元素中,添加I元素后的模拟浆液汞释放量最低,仅为0.33 μg,添加Br-的模拟浆液中汞的释放量与I-接近,为0.45 μg,添加Cl-的浆液中汞的释放量最高,为0.95 μg。WANG等[33]向含有Hg2 的体系内添加KF、KCl和KBr考察汞的释放行为时发现,添加KF后,体系内Hg2 与F-结合后随即发生分解,生成HgO,反应途径见式(2)、(3),而添加HCl和HBr的体系中生成较稳定的Hg-Cl和Hg-Br配合物,且Hg-Br配合物的热力学稳定性高于Hg-Cl 配合物,反应生成速率更快,汞释放量也更低,可以认为3种卤族元素对汞释放抑制的能力按Cl<Br<I顺序逐渐增大。
会与Hg2 发生氧化还原反应,导致已被捕获的烟气和保留在脱硫浆液内部的可溶态Hg2 被还原为不可溶的Hg0,重新释放到烟气中,进而随烟气排放进入大气,主要反应途径见式(1)。在反应温度50 ℃、pH为5、卤族元素物质的量浓度为20 mmol/L条件下,考察Cl、Br和I元素对汞释放影响,结果如图2所示。经90 min反应后,可以看到Cl、Br和I三种卤族元素中,添加I元素后的模拟浆液汞释放量最低,仅为0.33 μg,添加Br-的模拟浆液中汞的释放量与I-接近,为0.45 μg,添加Cl-的浆液中汞的释放量最高,为0.95 μg。WANG等[33]向含有Hg2 的体系内添加KF、KCl和KBr考察汞的释放行为时发现,添加KF后,体系内Hg2 与F-结合后随即发生分解,生成HgO,反应途径见式(2)、(3),而添加HCl和HBr的体系中生成较稳定的Hg-Cl和Hg-Br配合物,且Hg-Br配合物的热力学稳定性高于Hg-Cl 配合物,反应生成速率更快,汞释放量也更低,可以认为3种卤族元素对汞释放抑制的能力按Cl<Br<I顺序逐渐增大。

图2 卤族元素种类对汞释放影响
Fig.2 Effect of halogen species on Hg emission

(1)
Hg2 F-![]() HgF,
HgF,
(2)
HgF2 H2O![]() HgO 2HF。
HgO 2HF。
(3)
2.2 卤族元素含量对汞释放影响
WFGD系统内的脱硫浆液单次循环后脱硫剂往往无法完全反应,通常需要多次循环使用。烟气中的卤族元素易溶于水,尤其是Cl-,多次循环易导致系统浆液内卤族元素含量堆积过高,向系统内补水后对卤族元素有一定稀释作用,研究卤族元素浓度对汞释放的影响同样重要。设定反应温度50 ℃,pH为5,调整Cl、Br和I物质的量浓度分别为5、20和50 mmol/L,考察卤族元素对汞释放的影响,结果如图3所示。由图3可知,随卤族元素浓度增大,汞释放强度有所降低,当3种卤族元素物质的量浓度由5 mmol/L升至50 mmol/L后,汞释放量分别降低了23.5%、53.8%和62.8%。研究表明,在Hg2 与![]() 共存的系统内增加Cl-浓度会显著降低汞的释放,当向反应系统内加入质量分数0.4%的Cl-后,汞释放浓度相比加入Cl-前降低70%[34],这主要是由于卤族元素浓度增大后,虽然单位体积内活化分子比例不变,但活化分子数量的绝对值升高,在Hg含量一定的情况下,增强卤族元素与汞的有效结合,从而降低了汞的释放强度。此外,体系内大量Cl-会与反应(1)的中间产物HgSO3结合,生成
共存的系统内增加Cl-浓度会显著降低汞的释放,当向反应系统内加入质量分数0.4%的Cl-后,汞释放浓度相比加入Cl-前降低70%[34],这主要是由于卤族元素浓度增大后,虽然单位体积内活化分子比例不变,但活化分子数量的绝对值升高,在Hg含量一定的情况下,增强卤族元素与汞的有效结合,从而降低了汞的释放强度。此外,体系内大量Cl-会与反应(1)的中间产物HgSO3结合,生成 和
和 这2种配合物的稳定性较高[34],可将Hg2 束缚在配合物结构内,有效减少体系中的游离态Hg2 ,有助于减少汞的释放。
这2种配合物的稳定性较高[34],可将Hg2 束缚在配合物结构内,有效减少体系中的游离态Hg2 ,有助于减少汞的释放。

图3 卤族元素浓度对汞释放的影响
Fig.3 Effect of halogen concentrations on Hg emission
2.3 温度对汞释放影响
反应温度对化学反应速度影响较大,WFGD系统运行浆液温度通常在50 ℃左右,选取温度40、50和60 ℃,卤族元素物质的量浓度为20 mmol/L,pH为5的条件下,考察卤族元素对汞释放的影响,结果如图4所示。温度升高后汞释放强度均有所降低,当浆液温度由40 ℃升至60 ℃时,汞释放量分别降低了24.9%、21.9%和24.0%。由阿伦尼乌斯方程,有:

图4 温度对汞释放的影响
Fig.4 Effect of temperature on Hg emission
k=Ae-Ea/RT,
(4)
式中,k为反应速率常数;A为指前因子;Ea为反应表观活化能;R为摩尔气体常数;T为反应温度。
Hg和卤族元素X(代表Cl、Br和I)在模拟浆液体系内涉及一系列配合反应,见式(5)~(8)。以Cl为例,体系内生成的![]() (n取1~4)类型配合物的稳定性随配位数增加而增强[35],升高反应温度后会加快Hg与卤族元素生成深层配合物进程,使Hg以配合物的形式稳定在液相中,减少了Hg与
(n取1~4)类型配合物的稳定性随配位数增加而增强[35],升高反应温度后会加快Hg与卤族元素生成深层配合物进程,使Hg以配合物的形式稳定在液相中,减少了Hg与![]() 接触,即抑制了反应(1)的进行,进而降低汞的释放强度。此外,有研究表明相比Cl-而言,Br-与Hg2 的反应活性更高[28,33],生成配合物的反应速率常数更大,对体系内Hg2 束缚性也更强,整体对汞排放抑制效果也相对较好。
接触,即抑制了反应(1)的进行,进而降低汞的释放强度。此外,有研究表明相比Cl-而言,Br-与Hg2 的反应活性更高[28,33],生成配合物的反应速率常数更大,对体系内Hg2 束缚性也更强,整体对汞排放抑制效果也相对较好。
Hg2 X-![]() HgX ,
HgX ,
(5)
Hg2 2X-![]() HgX2,
HgX2,
(6)

(7)

(8)
2.4 pH对汞释放影响
为保证SO2脱除效率更高,WFGD系统运行过程中要确保脱硫塔内循环为弱酸性环境,可使脱硫剂中的Ca组分充分溶出并与S组分结合。然而在塔内脱硫剂与烟气逆流反应过程中,随脱硫浆液SO2吸收量逐渐增大,浆液pH逐渐降低,进而导致汞大量释放,为此考察不同pH条件下卤族元素对汞释放的影响至关重要。在温度50 ℃,卤族元素物质的量浓度为20 mmol/L条件下,pH选取4、5和6考察卤族元素对汞释放强度的影响,结果如图5所示。由图5可知,pH增大,汞的释放强度显著降低。当pH由4增至6时,汞释放量分别降低了45.8%、50.1%和37.1%。这主要是由于pH降低后,体系内的还原电势增大,导致Hg2 还原反应增强,促进了汞的释放。WO等[28]考察了pH影响汞释放行为,发现当pH从3升至4、5和6时,反应2 h后,Hg2 的还原释放率从84.4%分别降至63.1%、51.1% 和23.3%。

图5 pH对汞释放影响
Fig.5 Effect of pH on Hg emission
此外,降低反应pH,将导致体系内H 浓度显著增大,这会造成反应(1)中间产物HgSO3质子化,生成HgSO3H ,进而导致汞释放进一步增强。因此,在保证较高SO2脱除效率的前提下,在一定范围内提高环境pH将有利于减少汞的释放。
2.5 卤族元素对汞释放影响的机理分析
前文提到体系内存在卤族元素时会与汞生成多级![]() 配合物,以Cl-为例,Hg2 与Cl-在体系内生成的一系列配合物空间构型见表1。生成的Hg-Cl配合物避免了Hg2 与
配合物,以Cl-为例,Hg2 与Cl-在体系内生成的一系列配合物空间构型见表1。生成的Hg-Cl配合物避免了Hg2 与![]() 直接接触,改变了Hg2 的反应路径,降低汞的释放强度。配合物的稳定性越强,中心原子的束缚性越强,对汞释放的抑制效果也越明显。Hg与卤族元素生成的配合物稳定性主要受配体类型和数量等多种因素影响。本文作为配体的3种卤族元素为周期表同族元素,化学性质相似,PEARSON[36]基于路易斯酸碱理论对酸碱的软硬进行分类时指出,Cl-属于硬碱类离子,I-属于软碱类离子,Br-处在过渡交界处,软碱类离子半径较大,携带电荷量较低,易提供电子而引起空间变形,与Hg2 的配位能力强弱规律遵循F-<Cl-<Br-<I-,这为不同卤族元素对汞释放强度抑制的差异性提供理论支撑。此外,平衡常数
直接接触,改变了Hg2 的反应路径,降低汞的释放强度。配合物的稳定性越强,中心原子的束缚性越强,对汞释放的抑制效果也越明显。Hg与卤族元素生成的配合物稳定性主要受配体类型和数量等多种因素影响。本文作为配体的3种卤族元素为周期表同族元素,化学性质相似,PEARSON[36]基于路易斯酸碱理论对酸碱的软硬进行分类时指出,Cl-属于硬碱类离子,I-属于软碱类离子,Br-处在过渡交界处,软碱类离子半径较大,携带电荷量较低,易提供电子而引起空间变形,与Hg2 的配位能力强弱规律遵循F-<Cl-<Br-<I-,这为不同卤族元素对汞释放强度抑制的差异性提供理论支撑。此外,平衡常数![]() 通常用于评价配合物的稳定性,通常平衡常数
通常用于评价配合物的稳定性,通常平衡常数![]() 的数值越大,对应配合物的稳定性越强。对于一般反应(9)来说,
的数值越大,对应配合物的稳定性越强。对于一般反应(9)来说,![]() 计算方法见式(10),对于存在多级反应的配合物,反应级数i的平衡常数
计算方法见式(10),对于存在多级反应的配合物,反应级数i的平衡常数![]() 计算方法见式(11):
计算方法见式(11):
表1 Hg2 与Cl-生成配合物构型
Table 1 Construct of coordination compounds between Hg2 and Cl-

R1 R2![]() P,
P,
(9)

(10)

(11)
式中,R为反应物;P为生成物;i为产物反应级数。
PETRUCCI等[37]测量了常温(25 ℃)条件下 和
和![]() 的平衡常数,得出三者的
的平衡常数,得出三者的![]() 分别为1.2×1015、1.0×1021和6.8×1029,这说明3种配合物中
分别为1.2×1015、1.0×1021和6.8×1029,这说明3种配合物中![]() 配合物的稳定性最高,对游离态Hg2 的结合能力也更强,进一步说明在Cl、Br和I三种卤族元素中,在添加I元素后汞的释放强度最弱,添加Br次之,添加Cl元素对汞的结合能力最低,汞排放强度也最大。
配合物的稳定性最高,对游离态Hg2 的结合能力也更强,进一步说明在Cl、Br和I三种卤族元素中,在添加I元素后汞的释放强度最弱,添加Br次之,添加Cl元素对汞的结合能力最低,汞排放强度也最大。
![]() 配合物的配位体数量同样会影响配合物稳定性,随配体数量增加,Hg2 与卤族元素(如Cl)在体系内依次生成直线型、平面正三角形和正四面体形的配合物,见表1。从空间结构来看,
配合物的配位体数量同样会影响配合物稳定性,随配体数量增加,Hg2 与卤族元素(如Cl)在体系内依次生成直线型、平面正三角形和正四面体形的配合物,见表1。从空间结构来看,![]() 和
和![]() 配合物中心原子Hg被配位原子包围,对中心原子束缚性相对较好,从而影响体系汞释放强度。
配合物中心原子Hg被配位原子包围,对中心原子束缚性相对较好,从而影响体系汞释放强度。
从动力学角度对卤族元素影响汞释放机理进行分析,忽略Hg2 还原生成气相Hg0后由液相转移到气相的传质过程,默认生成的Hg0均不溶于体系,同时假设反应体系为理想液体并在体系内均匀混合,反应模型抽象为匀速搅拌的封闭体系,描述体系反应物在等温条件下的动力学反应进程。利用Comsol软件内部Chemical Engineering模块对脱硫浆液汞释放行为进行模拟分析,主要考察汞释放主要反应和卤族元素间相互作用对汞释放机理的影响(以Cl为例),涵盖反应(1)和(5)~(8)。反应体系包含Hg2 、Cl-和![]() 离子,反应初始各离子物质的量浓度分别设置为0.5×10-3、5.0和2.0 mol/L,Cl-对汞释放强度影响如图6所示(HgCl 与
离子,反应初始各离子物质的量浓度分别设置为0.5×10-3、5.0和2.0 mol/L,Cl-对汞释放强度影响如图6所示(HgCl 与![]() 变化趋势一致,HgCl2与
变化趋势一致,HgCl2与![]() 变化趋势一致)。由图6可知,在
变化趋势一致)。由图6可知,在![]() 和Cl-体系内引入Cl-后,体系内游离的Hg2 浓度迅速降低,并与Cl-结合生成
和Cl-体系内引入Cl-后,体系内游离的Hg2 浓度迅速降低,并与Cl-结合生成![]() 的多级配合物,最终主要以
的多级配合物,最终主要以![]() 和
和![]() 形式存在。研究指出,针对某一特定体系Hg与卤族元素在生成各配合物的含量分布上并非随配位数增大而增加,而是受体系内卤族元素总浓度影响[38]。值得注意的是,相比多种Hg与Cl生成的配合物含量而言,汞释放强度(Hg0浓度)始终保持在较低水平,表明体系内添加Cl-对汞释放强度的抑制效果明显,可迅速与Hg2 结合,减少Hg2 与
形式存在。研究指出,针对某一特定体系Hg与卤族元素在生成各配合物的含量分布上并非随配位数增大而增加,而是受体系内卤族元素总浓度影响[38]。值得注意的是,相比多种Hg与Cl生成的配合物含量而言,汞释放强度(Hg0浓度)始终保持在较低水平,表明体系内添加Cl-对汞释放强度的抑制效果明显,可迅速与Hg2 结合,减少Hg2 与![]() 结合,从而有效降低汞释放强度。
结合,从而有效降低汞释放强度。

图6 Cl-对汞释放强度影响
Fig.6 Influence of Cl- on Hg emission
3 结 论
1)卤族元素(Cl、Br和I)可明显降低WFGD浆液中汞的释放,不同种类卤族元素对汞释放抑制的能力按Cl<Br<I顺序依次增强。
2)提高系统反应温度、增加卤族元素浓度以及增大反应pH均有利于降低WFGD浆液中汞的释放。
3)WFGD浆液加入卤族元素后会与汞生成一系列较稳定配合物![]() (X为Cl、Br和I,n取1~4),其中,I元素表现出更强的Hg2 结合能力,生成的配合物稳定性更强,对汞释放的抑制效果最好。
(X为Cl、Br和I,n取1~4),其中,I元素表现出更强的Hg2 结合能力,生成的配合物稳定性更强,对汞释放的抑制效果最好。
4)WFGD体系内的汞通过与卤族元素生成配合物的方式,减少了与![]() 的接触,汞的还原反应路径发生改变,使汞释放行为受到抑制。
的接触,汞的还原反应路径发生改变,使汞释放行为受到抑制。
[1] UN Environment.Global mercury assessment 2018[R]. Switzerland:UN Environment Programme. Chemicals and Health Branch Geneva,2019.
[2] British Petroleum. Statistical review of world energy 70th edition [EB/OL].(2021-10-28)[2022-05-09].http://www.bp.com.
[3] 王起超,沈文国,麻壮伟. 中国燃煤汞排放量估算[J]. 中国环境科学,1999,19(4):318-321.
WANG Qichao,SHEN Wenguo,MA Zhuangwei. The estimation of mercury emission from coal combustion in China[J]. China Environmental Science,1999,19(4):318-321.
[4] ZHAO S,PUDASAINEE D,DUAN Y,et al. A review on mercury in coal combustion process:Content and occurrence forms in coal,transformation,sampling methods,emission and control technologies[J]. Progress in Energy and Combustion Science,2019,73:26-64.
[5] LIANG S,ZHANG C,WANG Y,et al. Virtual atmospheric mercury emission network in China[J]. Environmental Science & Technology,2014,48(5):2807-2815.
[6] ZHAO Y,YANG J,MA S,et al. Emission controls of mercury and other trace elements during coal combustion in China:A review[J]. International Geology Review,2018,60(5/6):638-670.
[7] 王树民,白孝轩,宋畅,等. 燃煤电厂大气汞及其他痕量元素排放标准研究[J]. 中国环境科学,2021,41(4):1949-1958.
WANG Shumin,BAI Xiaoxuan,SONG Chang,et al. Study of atmospheric trace elements emission standards for coal-fired power plants in China[J]. China Environmental Science,2021,41(4):1949-1958.
[8] ZHANG Y,YANG J,YU X,et al. Migration and emission characteristics of Hg in coal-fired power plant of China with ultra low emission air pollution control devices[J]. Fuel Processing Technology,2017,158:272-280.
[9] WANG S,ZHANG L,LI G,et al. Mercury emission and speciation of coal-fired power plants in China[J]. Atmospheric Chemistry and Physics,2010,10(3):1183-1192.
[10] CAO Y,CHEN B,WU J,et al. Study of mercury oxidation by a selective catalytic reduction catalyst in a pilot-scale slipstream reactor at a utility boiler burning bituminous coal[J]. Energy & Fuels,2007,21(1):145-156.
[11] LEE C W,SERRE S D,ZHAO Y,et al. Mercury oxidation promoted by a selective catalytic reduction catalyst under simulated powder river basin coal combustion conditions[J]. Journal of the Air & Waste Management Association,2012,58(4):484-493.
[12] 曹晓满,刘亚文,张军梅,等. 超低排放燃煤电厂污染控制设备协同脱汞研究进展[J]. 洁净煤技术,2021,27(5):98-105.
CAO Xiaoman,LIU Yawen,ZHANG Junmei,et al. Research progress on collaborative mercury removal of pollution control equipment in ultra-low emission coal-fired power plants[J]. Coal Clean Coal Technology,2021,27(5):98-105.
[13] 中国电力企业联合会. 中国电力行业年度发展报告[EB/OL].(2021-07-08)[2022-05-09].https://cec.org.cn/index.html.
[14] ZHAO S,DUAN Y,YAO T,et al. Study on the mercury emission and transformation in an ultra-low emission coal-fired power plant[J]. Fuel,2017,199:653-661.
[15] CHANG L,YANG J,ZHAO Y,et al. Behavior and fate of As,Se and Cd in an ultra-low emission coal-fired power plant[J]. Journal of Cleaner Production,2019,209:722-730.
[16] 陈崇明,党志国,车凯,等. 660 MW燃煤机组汞迁移转化特性研究[J]. 洁净煤技术,2021,27(4):157-163.
CHEN Chongming,DANG Zhiguo,CHE Kai,et al. Research on migration and transformation characteristics of mercury in 660 MW coal-fired unit[J]. Clean Coal Technology,2021,27(4):157-163.
[17] 宋畅,张翼,郝剑,等. 燃煤电厂超低排放改造前后汞污染排放特征[J]. 环境科学研究,2017,30(5):1-9.
SONG Chang,ZHANG Yi,HAO Jian,et al. Mercury emission characteristics from coal-fired power plant before and after ultra-low emission retrofitting[J]. Research of Environmental Sciences,2017,30(5):1-9.
[18] STEPHEN N,FUJIWARA N. The impact of wet flue gas desulfurization scrubbing on mercury emissions from coal-fired power stations[J]. Journal of the Air & Waste Management Association,2005,55(7):970-977.
[19] RAVI K S,NICK H,BLAIR M,et al. Control of mercury emi-ssions from coal-fired electric utility boilers[J]. Environmental Science & Technology,2006,40(5):1385-1393.
[20] PUDASAINEE D,KIM J H,YOON Y S,et al. Oxidation,reemission and mass distribution of mercury in bituminous coal-fired power plants with SCR,CS-ESP and wet FGD[J]. Fuel,2012,93:312-318.
[21] NOLAN P S,REDINGER K E,AMRHEIN G T,et al. Demonstration of additive use for enhanced mercury emissions control in wet FGD systems[J]. Fuel Processing Technology,2004,85(6/7):587-600.
[22] WU C,CAO Y,DONG Z,et al. Impacting factors of elemental mercury reemission across a lab-scale simulated scrubber[J]. Chinese Journal of Chemical Engineering,2010,18(3):523-528.
[23] CHANG L,ZHAO Y,LI H,et al. Effect of sulfite on divalent mercury reduction and re-emission in a simulated desulfurization aqueous solution[J]. Fuel Processing Technology,2017,165:138-144.
[24] TANG T,XU J,LU R,et al. Enhanced Hg2 removal and Hg0 re-emission control from wet fuel gas desulfurization liquors with additives[J]. Fuel,2010,89(12):3613-3617.
[25] LIU Y,WANG Y,WU Z,et al. A mechanism study of chloride and sulfate effects on Hg2 reduction in sulfite solution[J]. Fuel,2011,90(7):2501-2507.
[26] WANG Y,LIU Y,WU Z,et al. Experimental study on the absorption behaviors of gas phase bivalent mercury in Ca-based wet flue gas desulfurization slurry system[J]. Journal of Hazardous Materials,2010,183(1/3):902-907.
[27] WANG Q,LIU Y,WANG H,et al. Mercury re-emission behav-iors in magnesium-based wet flue gas desulfurization process:The effects of oxidation inhibitors[J]. Energy & Fuels,2015,29(4):2610-2615.
[28] WO J,ZHANG M,CHENG X,et al. Hg2 reduction and re-emission from simulated wet flue gas desulfurization liquors[J]. Journal of Hazardous Materials,2009,172(2/3):1106-1110.
[29] WU C L,CAO Y,HE C C,et al. Study of elemental mercury re-emission through a lab-scale simulated scrubber[J].Fuel,2010,89(8):2072-2080.
[30] CHANG John C S,GHORISHI S Behrooz. Simulation and evaluation of elemental mercury concentration increase in flue gas across a wet scrubber[J]. Environmental Science & Technology,2003,37(24):5763-5766.
[31] SOLIS K L B,NAM G U,HONG Y. Mercury(II) reduction and sulfite oxidation in aqueous systems:Kinetics study and speciation modeling[J]. Environmental Chemistry,2017,14(3):151-159.
[32] CHEN C,LIU S,GAO Y,et al. Investigation on mercury reemi-ssion from limestone-gypsum wet flue gas desulfurization slurry[J]. The Scientific World Journal,2014,2014:1-6.
[33] OCHOA-GONZ LEZ R,D
LEZ R,D AZ-SOMOANO M,MART
AZ-SOMOANO M,MART NEZ-TARAZONA M R. Effect of anion concentrations on Hg2 reduction from simulated desulphurization aqueous solutions[J]. Chemical Engineering Journal,2013,214:165-171.
NEZ-TARAZONA M R. Effect of anion concentrations on Hg2 reduction from simulated desulphurization aqueous solutions[J]. Chemical Engineering Journal,2013,214:165-171.
[34] OMINE N,ROMERO C. E,KIKKAWA H,et al. Study of elemental mercury re-emission in a simulated wet scrubber[J]. Fuel,2012,91(1):93-101.
[35] ACU A-CARO C,BRECHTEL K,SCHEFFKNECHT G,et al. The effect of chlorine and oxygen concentrations on the removal of mercury at an FGD-batch reactor[J]. Fuel,2009,88(12):2489-2494.
A-CARO C,BRECHTEL K,SCHEFFKNECHT G,et al. The effect of chlorine and oxygen concentrations on the removal of mercury at an FGD-batch reactor[J]. Fuel,2009,88(12):2489-2494.
[36] PEARSON R G. Hard and soft acids and bases[J]. Journal of the American Chemical Society,1963,85(22):3533-3539.
[37] PETRUCCI R H,HARWOOD W S,HERRING F G. General chemistry:Principles and modern application & Basic Media Pack[M].Upper Saddle River:Prentice Hall,2002.
[38] SILLEN L G. Electrometric investigation of equilibria between mercury and halogen ions. VIII. Survey and Conclusions[J]. Acta Chemica Scandinavica,1949,3:539-553.
Effect of halogen elements on the mercury emission from wet flue gas desulfurization system

移动阅读
CHANG Lin,ZHANG Yi,LIU Yi,et al.Effect of halogen elements on the mercury emission from wet flue gas desulfurization system[J].Clean Coal Technology,2022,28(8):126-132.