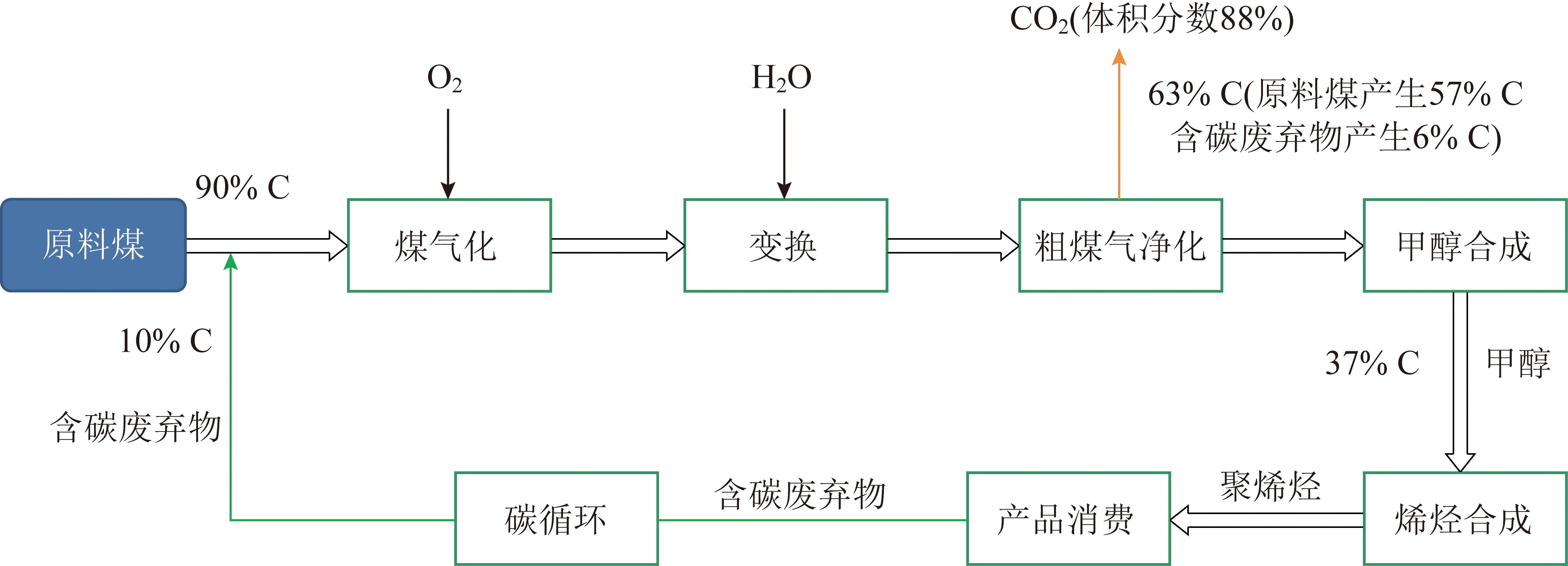
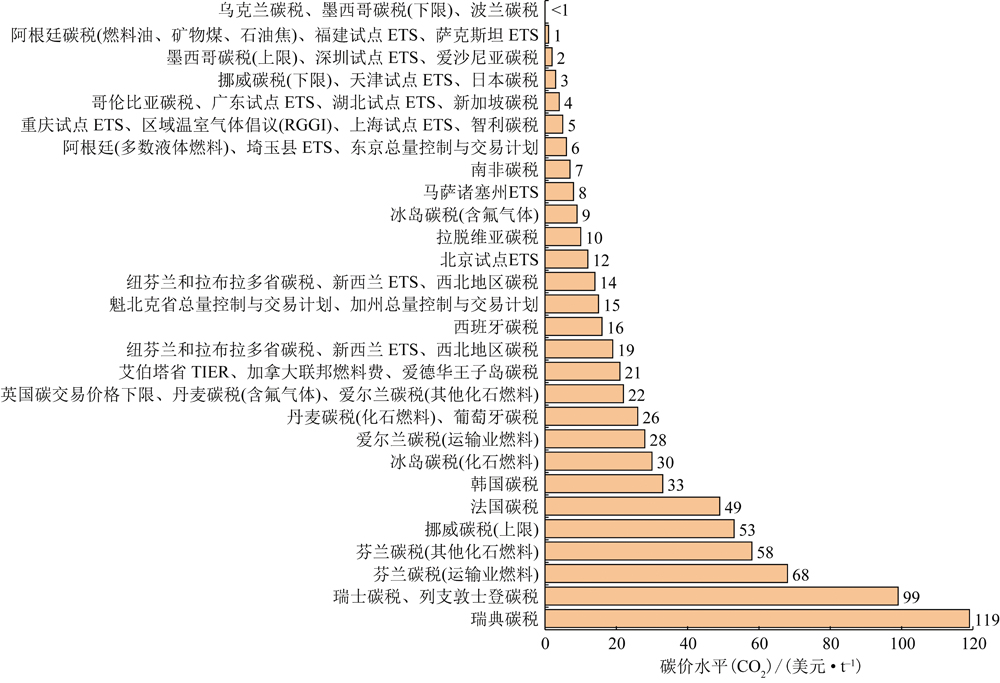
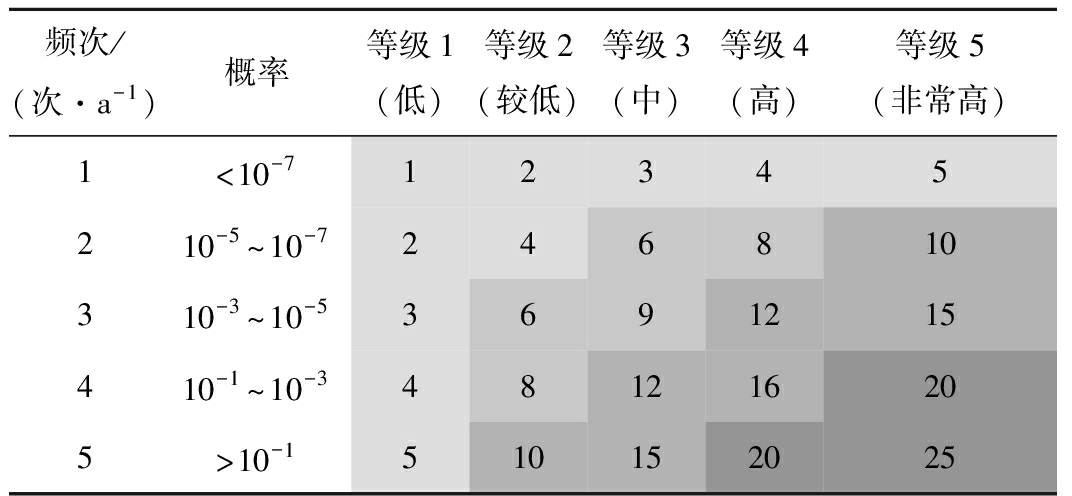
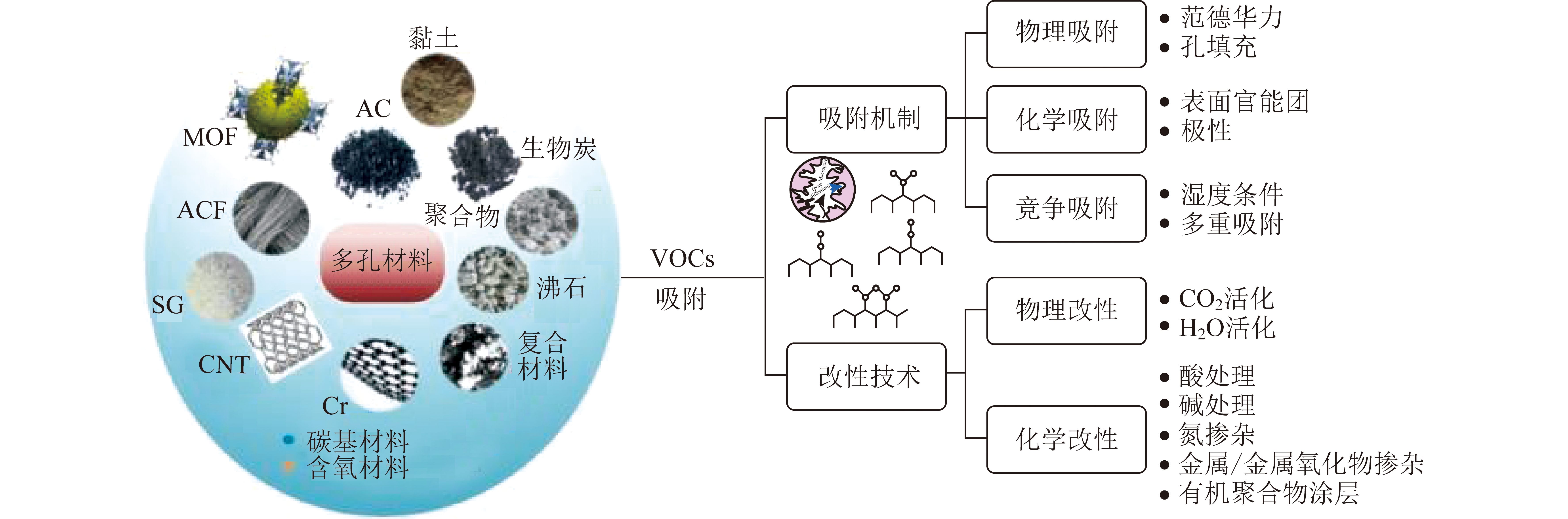
ACF电吸附过程动力学特性和脱盐影响因素试验研究
0 引 言
近年来,国家对于水污染治理愈加重视,出台了《水污染防治行动计划》等,强化了对各类污水的治理力度和排放标准[1]。工业领域的水系统具有较大的节水与回用潜能,工业废水含盐量高、排量大等是处理难点[2],因此急需研发新型的节能环保、减少浓水排放的技术,以实现其高效低成本脱盐。目前电吸附技术处于试验研究和中试阶段,其电耗低,仅需在水的电解电压以下运行;绿色环保,无需添加药剂,无二次污染[3];除盐效率高,出水水质好,是水处理技术研究的热点方向。
利用电吸附技术实现废水快速脱盐的核心包括提高脱盐速度和实现高通量,因此探究影响电吸附过程动力学特性和脱盐影响因素是关键。动力学因素决定了离子在溶液及吸附剂内部的运动行为,即吸附速率[4]。吸附容量与电极施加的电压、溶液内离子所带电荷数、溶液浓度、温度等相关[5]。因此,对电吸附动力学特性及电极材料吸附容量的研究是未来电吸附技术提高的关键。现有关于电吸附的研究集中在操作参数的选择和材料的改进[6-8],但缺少对特定材料动力学特性和电极材料吸附机理的探究。基于此,本文选择易取得的活性炭纤维为电极材料,在自制的板式电吸附装置进行多组电吸附试验,研究进样浓度、外加电压、进样液pH值和温度对其除盐效率和饱和吸附容量的影响,对不同电压、不同浓度下的电吸附动力学结果进行拟合,以期为活性炭纤维(ACF)电吸附在污水脱盐处理及电吸附材料的发展方向提供理论依据。
1 试 验
1.1 试验系统
采用按一定浓度配制的NaCl溶液模拟含盐废水进行电吸附脱盐试验,试验系统如图1所示,其核心装置为自制电吸附模堆,电极对数为1,模堆内部结构如图2所示,1~6依次为:有机玻璃作为端板(固定模堆内部各组件,并预留外接端口作为水流出入口)、厚1 mm橡胶垫(密封作用)、橡胶圈(固定ACF电极,并密封电极四周)、316L不锈钢板(集流体)、ACF(盐溶液中阴阳离子的吸附载体)、绝缘隔膜(聚乙烯纤维网,作为水流通道)。

图1 ACF电吸附试验系统
Fig.1 System diagram of ACF electro-sorption experiment

图2 电吸附装置内部结构
Fig.2 Internal structure diagram of electric adsorption device
1.2 试验方法
选择NaCl溶液作为目标样液,利用自制ACF电吸附装置进行不同浓度、不同电压下的电吸附试验。经前期预试验,调节进样流量恒定为最佳流速40 mL/min,采用循环进样方式,将电导率仪置于进样液中,每隔30 s记录电导率、电流等的变化。
电导率能反映溶液中的含盐量、溶液浓度与电导率间存在良好的线性关系[9],本文以电导率的去除率判定电吸附的脱盐率,计算公式为

(1)
式中, η为平均脱盐率,%;t为时间间隔,取30 s;当t取出口电导率与入口电导率相等时,对应的时刻即为电极吸附饱和时刻;C0为入口电导率(进样液的电导率),为常数,μs/cm;C为出口电导率,μs/cm。
2 试验结果与讨论
2.1 ACF表面形态和孔径
ACF的电镜扫描如图3所示。可以看出,ACF呈规则分布的纤维状,说明其接触电阻比颗粒状的活性炭更小,更适合做电极材料。ACF由大量形状不规则、尺寸不等的纤维沿轴向排列,形成少量深浅不一的纵向纹理沟槽和不连续、不规则的空隙及楔形的轴向裂纹,局部存在少量外来的杂质。纤维本身有裂缝和细微的斑点,其表面由细纤状的片状结构组成,片状结构之间可认为是孔,数量级在几个微米级,形状为狭缝形。该结构促使ACF相比于传统炭材料有更大的比表面积、更强的可塑性以及更优的吸附效果。

图3 ACF的SEM图
Fig.3 Scanning electron microscopy of ACF
ACF电极材料的N2吸附等温线如图4(a)所示,可以看出,该吸附等温线属于IUPAC定义的I型等温线,比表面积为13 81.497 m2/g,微孔比体积为0.507 cm3/g,微孔比表面积为1 293 m2/g,剩余比表面积为88.194 m2/g。图4(b)为孔径分布,可以看出,孔径主要集中在1~2 nm,说明ACF属于微孔材料。

图4 ACF的N2等温吸附脱附曲线及孔径分布曲线
Fig.4 N2 isotherm adsorption-desorption curve and pore size distribution of ACF
2.2 电吸附等温吸附模型
吸附等温线表示在特定温度下,吸附剂的吸附量与溶液中剩余吸附质数量的关系[10],表示电吸附过程的热力学性能,并预测未研究的试验条件下吸附质在吸附剂与溶液的量的关系[11]。Langmuir吸附理论(单分子层吸附理论)假设:活性位点数与吸附数对应,仅进行单层吸附;吸附材料表面各点的吸附力一致,且被吸附的吸附质之间相互作用可忽略不计[12];整个吸附剂表面存在动态的吸附平衡。Langmuir吸附等温方程为

(2)
式中,qe为吸附平衡时的吸附量,mmol/g;qm为单分子层吸附质的吸附量,mmol/g;KL为吸附过程的平衡常数,L/mmol,;Ce为吸附平衡时的浓度,mmol/L。
若吸附剂表面不均匀,吸附在吸附剂表面的分子间存在不可忽略的相互作用,此时Langmuir吸附等温方程预测结果与实际情况相差较大。Freundlich吸附理论提出含有2个常数项KF和n吸附经验方程,其线性表达式为

(3)
式中,KF为Freundlich吸附系数,为温度的函数;n为吸附强度相关的特征常数。
等温模型的研究重点是优化吸附并了解控制吸附剂和被吸附物间相互作用的驱动力。试验考查了25 ℃,电压0.4、0.8、1.2 V时平衡浓度与吸附容量的关系,图5为Langmuir吸附等温模型拟合结果。可以看出,在一定电压下,随着浓度增加,吸附容量逐渐增加,说明进样浓度越小,双电层重叠效应越明显,部分孔道未得到充分利用,浓差极化较弱,离子迁移速度慢;随着离子浓度提高,浓差极化增强,离子迁移速度变快,吸附材料的截止孔径变小,双电层重叠效应减弱,使孔道得到充分利用,比表面积和孔隙率均增大。

图5 Langmuir吸附等温模型拟合结果
Fig.5 Fitting results of Langmuir adsorption isotherm model
表1为Langmuir和Freundlich拟合参数。随着电压增大,饱和吸附量增大。特别是电压由0.8 V增至1.2 V后,电吸附装置的饱和吸附量增幅明显。在保证无水电解的前提下,1.2 V为电吸附最佳电压。外加电压越大,Langmuir吸附常数KL越大,电吸附脱盐能力越强。由双电层模型可知,紧密层内实现离子的单分子层吸附,扩散层实现离子的多分子层吸附。ACF主要以紧密层吸附离子为主导,电吸附过程更符合单分子层吸附。
表1 Langmuir和Freundlich拟合参数
Table 1 Fitting parameters of Langmuir and Freundlich formula

图6为Freundlich吸附等温线的拟合结果,可以看出,电压越大,n越大,说明电压越大,极板的平衡吸附量越大,极板吸附能力越强。根据2种模型的R2(表1)可得出,ACF电吸附脱盐过程更符合Langmuir等温吸附模型。

图6 Freundlich吸附等温模型拟合结果
Fig.6 Fitting results of Freundlich adsorption isotherm model
不同浓度下电压与平衡吸附容量的关系结果如图7所示,施加电压低于水解电压时,电压与吸附容量成正比,说明电压越高,产生的吸附点位越多,吸附量越大。但随着浓度增加,吸附容量增加幅度减小,是因为浓度增大、电压升高使截止孔径减小。反之,双电层厚度增加,重叠效应明显,截止孔径增大。同时中平层电势的升高使扩散层电压降低,若不计电极上的特性吸附离子吸附,按照GCS 模型,双电层的电容量也随之减少[13]。

图7 不同浓度下电压与平衡吸附容量的关系
Fig.7 Changes between voltage and equilibrium adsorption capacity at different concentrations
2.3 电吸附动力学
吸附动力学模型可表征吸附速率、吸附容量、吸附平衡时间等[14]。吸附过程动力学主要由吸附质从溶液主体向吸附材料表面的外扩散速度、吸附平衡时间以及在吸附材料表面和内部孔道的内扩散速率等决定[15]。吸附过程一般可分为:① 外部传质过程,吸附质从主体溶液向吸附材料表面的外扩散;② 与吸附质表面活性位点作用;③ 内部传质过程,吸附质由外表面向孔道内迁移,受吸附剂孔道尺寸影响明显;④ 吸附质与吸附质孔道内活性位点作用[16],吸附过程是多个步骤同时影响吸附速率[17]。
Lagergren又称为准一级动力学模型,适于描述固液两相界面上吸附反应的快慢,不适于描述整个吸附反应的速率[18],可表示为
q=q′e(1-e-k1),
(4)
式中,q为任意t的吸附量,mg/g;q′e为达到饱和吸附时的吸附容量,mg/g;k1为Lagergren准一级动力学吸附常数,h-1。
准二级动力学模型[19]是在固相吸附容量的基础上推导的(式(5))。
q(1 q′ek2t)=q′e2k2t,
(5)
式中,k2为准二级动力学吸附常数,h-1。
2.3.1 不同电压下的电吸附动力学
图8为5种电压下电导率随时间的变化(500 mg/L,20 mL/min)。可以看出,0~0.4 V有一个明显的电导率差值,约为53 μS/cm,说明在微弱的电压下形成的电场和双电层对离子去除率的贡献很大。电压为1.2 V时,除盐效率最高,此时电场力最强,双电层的厚度最小,电荷密度最大,对离子的迁移提供的推动力最大。电压升到1.6 V时,电压高于水的电解电压,部分能量用于水的电解,使产生的电场力和双电层储能性能不足,导致1.6 V的脱盐效果比1.2 V时差。因此,1.2 V为最佳的外加电压。

图8 不同电压下电导率的变化
Fig.8 Changes in conductivity at different voltages
图9为不同电压下电吸附装置吸附容量随时间的变化(500 mg/L,20 mL/min),Lagergren准一级吸附动力学速率方程拟合和准二级吸附动力学速率方程拟合结果见表2。可以看出,未施加电压与施加电压后饱和吸附容量相差较大,随着电压等距升高,饱和吸附容量等距上升,但1.2 V时平衡吸附容量高于1.6 V。随着电吸附时间的延长,吸附容量的增加速率下降,这与电导率下降减缓一致。整体上,随着电压的增大,吸附量逐渐增大,但其吸附速率逐渐减小。这是因为吸附初始时刻吸附材料的活性位点数量多、双电层和电场作用力强,随着吸附过程的进行,吸附位点越来越少,且未被吸附的离子受到已被吸附的相同电荷离子的静电斥力,使吸附速率减缓至0,即达到吸附饱和。

图9 不同电压下的电吸附容量随时间的变化
Fig.9 Changes of electrosorption capacity with time at different voltages
表2 不同电压下溶液的准一级、二级动力学拟合结果
Table 2 Quasi-first-order and quasi-second-order kinetics fitting results of the solution at different voltages

由图9可知,准一级和准二级动力方程的拟合度均较高。由表2可得出,施加电压较低时,准二级动力学方程拟合度相对较高,说明低电压下离子迁移主要依靠浓度差,但实际上离子吸附是电吸附和物理吸附的综合作用结果。随着电压的升高,准一级动力学拟合度逐渐优于准二级方程。同时,在准一级动力学拟合下,饱和吸附量的理论值与试验值间的误差更小。扩散作用主要取决于吸附质本身的属性,吸附质所带电荷量越高,扩散速度越快;电迁移作用主要取决于所加极板电压和离子的离子迁移率,在固液界面形成双电层,对离子产生进一步的抓捕作用,将其储存在双电层中。但外加电压不能高于水解电压,防止水解副产物的生成。
2.3.2 不同浓度下的电吸附动力学
图10为不同浓度下吸附容量随时间的变化(12 V,20 mL/min)。可以看出,样液浓度越高,吸附量越大。由于溶液主体与固液界面间浓度梯度增加,促进了离子向固液界面的迁移;而且离子浓度升高使截止孔径缩小,稀溶液中未利用的孔道也吸附了部分离子,削弱了双电层重叠效应。表3为Lagergren准一级、二级吸附动力学速率方程的拟合参数。随着初始浓度增加,吸附容量上升速率加快,平衡吸附容量不断增加。这是因为溶液主体离子浓度增加,减少了外部传质阻力,加快了外扩散步骤,从而提高了电吸附速率。准一级动力学模型的拟合回归常数优于二级动力学模型,因此一级动力学模型更适合描述试验过程。一级动力学拟合结果中,动力学吸附常数随浓度增加逐渐增大,是因为浓度增大,使离子的外扩散作用增强,内扩散的抑制作用被削弱,从而电吸附速率提高。

图10 不同浓度下电吸附容量随时间的变化
Fig.10 Changes of electro-sorption capacity with time under different concentrations
表3 Lagergren准一级、二级吸附动力学速率方程拟合参数
Table 3 Fitting results of Lagergren quasi-first and second-order adsorption kinetic rate parameters

2.4 pH值对电吸附装置除盐性能的影响
图11为不同pH下电吸附容量随时间变化(500 mg/L,1.2 V,20 mL/min)。酸性条件的吸附容量优于碱性条件,是因为酸性条件下,电吸附材料表面和孔道中的结垢物质被溶解,比表面积和孔隙率增大,吸附性能增强;碱性条件下,OH-可能与溶液中的易成垢离子(如钙离子、镁离子等)在表面结垢,堵塞孔道,导致吸附离子能力下降。pH=6.5时,平衡吸附容量大于pH=5.5时,这是因为强酸条件下引入更多的H ,与溶液中待去除离子形成竞争吸附,占用部分吸附位点,导致对溶液中离子的吸附量减少。因此,弱酸性条件更有利于电吸附除盐性能的提高。

图11 不同pH值下吸附容量随时间变化
Fig.11 Changes of adsorption capacity with time at different pH
2.5 温度对电吸附除盐性能的影响
图12为进样液为500 mg/L的NaCl溶液、电压为1.2 V条件下,温度分别为25、35、45 ℃时平衡浓度与吸附容量间的关系。25 ℃下,吸附容量最大,随着温度升高,吸附容量下降。表4为不同温度下Langmuir等温模型的拟合系数,可以看到,不同温度下均有很高的拟合度,但随着进样温度的升高,平衡吸附容量呈明显现下降趋势,即平衡吸附容量在25 ℃时最大,在45 ℃时最小。这是由于温度升高会影响溶液的介电常数、离子迁移速度、双电层的厚度等,溶液温度降低,使分散层的有效厚度变小,分散层电容增加,使吸附容量增加。因此,25 ℃为最佳试验温度。

图12 不同温度下平衡浓度与吸附容量的关系
Fig.12 Changes of adsorption capacity with equilibrium concentration at different temperatures
表4 不同温度下Langmuir等温模型的拟合系数
Table 4 Fitting parameters of Langmuir isothermal model at different temperatures

3 结 论
1)对不同电压、不同浓度下的电吸附动力学结果进行拟合发现,施加低电压时(<0.8 V),吸附过程适于准二级动力学方程;高电压时(>0.8 V)适于一级动力学模型。电压越大,吸附速率越快,电吸附脱盐过程更符合Langmuir等温吸附模型,电压和浓度增大,吸附容量增加。
2)5种不同pH值样液进行电吸附试验发现,弱酸性条件脱盐性能最佳,中性一般,碱性最差,弱酸性条件更有利于电吸附除盐性能的提高。
3)温度升高会影响溶液的介电常数,溶液温度升高,使分散层的有效厚度变大,分散层电容降低,使吸附容量减小,脱盐效果变差,25 ℃为最佳进样温度。
[1] 石效卷,李璐,张涛.水十条 水实条——对《水污染防治行动计划》的解读[J].环境保护科学,2015,41(3):1-3.
SHI Xiaojuan ,LI Lu,ZHANG Tao. Water pollution control action plan,a realistic and pragmatic plan:An Interpretation of Water Pollution Control Action Plan[J]. Environmental Protection Science,2015,41(3):1-3.
[2] 吴晓迪,陈志强. 电化学法处理工业废水的现状与发展研究[J]. 环境科学与管理,2014,39(8):30-33.
WU Xiaodi ,CHEN Zhiqiang. Research progress and development trend in wastewater treatment with electrochemical methods[J].Environmental Science and Management,2014,39(8):30-33.
[3] 马双忱,马岚,刘畅,等. 电厂循环冷却水处理技术研究与应用进展[J]. 化学工业与工程,2019,36(1):38-47.
MA Shuangchen,MA Lan,LIU Chang,et al. Progress in research and application of circulating cooling water treatment technologies in power plants[J]. Chemical Industry and Engineering,2019,36(1):38-47
[4] MANEERUNG T ,LIEW J ,DAI Y,et al. Activated carbon derived from carbon residue from biomass gasification and its application for dye adsorption:Kinetics,isotherms and thermodynamic studies[J]. Bioresource Technology,2016,25:350-359.
[5] LEE J J. Adsorption thermodynamics,kinetics and isosteric heat of adsorption of rhodamin-B onto granular activated carbon[J]. Journal of the Korean Industrial & Engineering Chemistry,2016,27(2):199-204.
[6] 李娜,张国珍,杨仕超,等. 活性炭纤维电吸附处理含盐溶液吸附特性研究[J]. 工业水处理,2013,33(8):48-51.
LI Na,ZHANG Guozhen,YANG Shichao,et al. Research on the adsorption capability of active carbon fiber electroadsorption for treating salt-containing solution[J].Industrial Water Treatment,2013,33(8):48-51.
[7] 高湘,林小辉.活性炭纤维对于离子的电吸附选择性能研究[J].工业安全与环保,2015,41(4):41-44.
GAO Xiang,LIN Xiaohui. Study of electrosorption selectivity of ions by activated carbon fiber[J]. Industrial Safety and Environmental Protection,2015,41(4):41-44.
[8] 毕慧芝,田秉晖. 电吸附活性炭电极制备及电吸附特性[J]. 环境工程学报,2015,9(4):1606-1612.
BI Huizhi,TIAN Binghui. Preparation of activated carbon electrodes and their electrosorption performances[J]. Chinese Journal of Environmental Engineering,2015,9(4):1606-1612.
[9] DAI Q ,SHAN H ,JIA Y ,et al. Laboratory study on the relationships between suspended sediment concentration and electrical conductivity[C]//ASME International Conference on Ocean. 2009.
[10] FOO K Y ,HAMEED B H . Insights into the modeling of adsorption isotherm systems[J]. Chemical Engineering Journal,2010,156(1):2-10.
[11] GUNARY D . A new adsorption isotherm for phosphate in soil[J]. European Journal of Soil Science,2010,21(1):72-77.
[12] CHEN Xunjun. Modeling of experimental adsorption isotherm data[J]. Information(Switzerland),2015,6(1):14-22.
[13] OLDHAM K B . A Gouy-Chapman-Stern model of the double layer at a(metal)/(ionic liquid)interface[J]. Journal of Electroanalytical Chemistry,2008,613(2):131-138.
[14] 李兵,蒋海涛,张立强,等. SO2在活性炭表面的吸附平衡和吸附动力学[J]. 煤炭学报,2012(10):1737-1742.
LI Bing ,JIANG Haitao ,ZHANG Liqiang ,et al. Adsorption equilibrium and kinetics of SO2 on activated carbon[J]. Journal of China Coal Society,2012,37(10):1737-1742.
[15] DOGAN M,ALKAN M. Adsorption kinetics of methyl violet onto perlite[J]. Chemosphere,2003,50(4):517-528.
[16] HAN Y ,CAO X ,OUYANG X,et al. Adsorption kinetics of magnetic biochar derived from peanut hull on removal of Cr(VI)from aqueous solution:Effects of production conditions and particle size[J]. Chemosphere,2016,145:336-341.
[17] CONWAY E A E . Adsorption and electrosorption at high-area carbon-felt electrodes for waste-water purification:Systems evaluation with inorganic,S-containing anions[J]. Journal of Applied Electrochemistry,2001,31:257-266.
[18] LIN S H,CHEN Y W. Liquid-phase adsorption of 1,1-dichloro-1-fluoroethane by various adsorbents[J]. Industrial & Engineering Chemistry Research,1997,36(10):4347-4352.
[19] MATHIALAGANT ,VIRARAGHAVAN T . Adsorption of cadmium from aqueous solutions by perlite[J]. Journal of Hazardous Materials,2003,38(1):57-76.
Experimental study on kinetic characteristics of ACF electro-sorption process and influencing factors of desalination
MA Lan,HUANG Luyue,XU Yongyi,et al.Experimental study on kinetic characteristics of ACF electro-sorption process and influencing factors of desalination[J].Clean Coal Technology,2021,27(1):316-322.