焦炉煤气制氢技术研究进展
0 引 言
近10 a,我国粗钢和焦炭产量整体小幅上升,在全球产能中占比均超过50%。2021年焦炭产量为4.64亿t,生产1 t焦炭可产生430 m3左右焦炉煤气。焦炉煤气中H2体积分数超过50%,若以55%计算,可从2021年焦炉煤气中分离出的H2量超1 000亿m3。由于一些中小型焦化企业“只焦不化”,以行业20%焦炉煤气放散或燃烧量计算,被丢弃的H2量可达200亿m3。此外,燃烧过程产生的大量温室气体(如CH4、CO2)被直接排放到大气中,严重污染环境。焦炉煤气综合利用意义重大,特别是H2的分离与利用,一方面是国家环保战略和冶金企业转型升级的需要,另一方面是高纯H2、合成气等化工原料市场的迫切需求。在冶金领域,焦炉煤气主要应用于高炉炼铁、冷轧热处理炉和钢管光亮退火炉保护气[1-2]。随着氢冶金技术的发展,与未喷吹焦炉煤气相比,其焦比可降低14.43%,碳减排8.61%[3-4]。宝钢、本钢等大型钢铁联合企业大力发展该工艺,H2需求量急剧增长。在能源化工领域,H2主要用作甲醇、乙醇、乙醚合成以及苯加氢的原料。在新能源汽车领域,H2作为燃料,是汽车的核心动力来源。
我国H2生产较成熟的路线[5-6]有:① 煤、天然气等化石能源重整制氢,占比约64%,世界上96%以上的氢原料来自该方法;② 工业副产气制氢,约32%;其余为电解水等方式制氢。化石能源重整制氢以煤炭、天然气为代表,其中天然气蒸汽重整是主流技术,制氢成本主要来自原料天然气,占比超过70%。工业副产气制氢原料以焦炉煤气、氯碱尾气等富氢尾气为代表,根据气体组分的沸点、吸附特性、分子尺寸等物理特性,利用变压吸附(PSA)、深冷法、膜分离等物理技术将H2分离出来,其纯度可达99.5%以上。我国炼焦和制碱工业基础雄厚,分离技术成熟,制氢成本较低(0.5~1.0元/m3),利用工业副产气制H2是一条符合我国现阶段能源国情的技术路线[7]。电解水制氢技术绿色环保、产氢纯度高,可达99.999%,但设备占地面积大,耗电严重,只有极少数水电丰盈的省份适合大范围开展,如四川省。然而H2运输是阻碍其大范围开展的难点。目前世界先进的碱水电解(AWE)电解水制氢技术效率在70%~80%,质子交换膜(PEM)电解水制氢技术制氢成本较低,约3.7美元/kg[8],还存在较大技术提升空间。
基于双碳目标和H2需求增长的现实意义,焦炉煤气的深度开发与利用尤为重要。物理法分离H2可获得高纯度H2,产生的解吸气主要用于供热、发电及液化天然气生产,部分被放空燃烧,焦油、苯等焦炉煤气成分高值化程度较低。针对焦炉煤气高效利用这一难题,一方面对传统物理分离技术进行工艺优化和能效提升,另一方面围绕非催化和催化重整、氧传输膜重整、化学链重整等化学法焦炉煤气制氢技术进行探索,开发更高效、节能的工业副产气制氢技术。相比成熟的物理法分离技术,化学法焦炉煤气制氢技术还存在诸多亟需解决的科学问题,其关键在于促进工业副产气中CH4、CO2等含碳气体选择性地转化为H2和CO。目前,非催化和催化重整焦炉煤气制氢技术及氧传输膜重整焦炉煤气制氢技术已实现小范围工业化应用,而化学链重整技术还停留在实验室阶段。
笔者围绕焦炉煤气物理分离技术与化学重整技术的技术原理和难点进行阐述,给出相应的应用实例与解决思路,以期推动焦炉煤气的高效清洁利用。
1 物理方法制氢
1.1 变压吸附制氢
PSA技术由美国联合碳化物公司(UCC)于20世纪60年代开发,广泛应用于气体混合物的分离[9]。其原理是利用吸附剂对不同气体组分的吸附能力随压力变化的特性,升压时吸附剂吸附杂质组分,降压时杂质组分被脱附,吸附剂再生,整个过程中H2几乎不会被吸附,从而实现连续分离H2的目的。
变压吸附制氢工艺流程如图1所示,主要分为4个工序。第1阶段为压缩,压缩炼焦厂产生的焦炉煤气,压力由5~12 kPa提升至变压吸附所需压力0.6~1.8 MPa[10]。第2阶段为预处理与净化,焦炉煤气经冷却进入预净化装置,预脱除有机物、H2S、NH3等杂质。再通过变温吸附(TSA)工艺进一步脱除易使吸附剂中毒的组分,如焦油、萘、硫化物。第3阶段为变压吸附,被认为是整个工艺的核心,用于除去H2以外的绝大部分杂质组分。第4阶段为H2精制,前一道工序获得的H2一般含有少量O2和水分,为获得纯度达99.999%的高纯氢还需严格控制O2含量(低于2×10-6)。

图1 变压吸附制氢工艺流程
Fig.1 Process flow diagram of pressure swing adsorption hydrogen production
根据目标气体组分特性,变压吸附工艺须采用具有不同吸附选择性和吸附容量的吸附剂。根据焦炉煤气的成分特点,吸附剂一般选用氧化铝、分子筛、活性炭[11-12]。氧化铝物理性质表现为高孔隙率的球状颗粒,具有机械强度高、无毒等特点,对水亲和力较强,可以深度吸附微量的水,主要填装于吸附塔底部。活性炭为毛细孔结构,对有机物亲和力强,主要填装于吸附塔中部,用于吸附分离萘和各类烃。SHAMSUDIN等[13]以棕榈壳活性炭为吸附剂,用于H2/CO2分离,该活性炭具有几乎100%的H2分离纯度,H2回收率为88.43%。分子筛为立方体骨架结构,具有比表面积大、孔隙均匀等特点,主要填装于吸附塔上层,用于吸附脱除CH4、N2、CO2。最上层选用沸石,净化H2中CO等杂质[14]。5A沸石、BPL活性炭、SSF碳膜、MOF UTSA-16等吸附剂对CH4和CO2具有良好的选择性吸附性能[14-18],结合双变压吸附工艺可有效分离CH4和CO2,获得纯净的CO2流;净化H2或合成气,使H2纯度达99.99%以上,回收率达93%~96%;实现超过90%的干重整制合成气纯度和回收率,几乎完全转化CH4和CO2。
随着行业发展,对变压吸附工艺的焦炉煤气处理能力和H2纯度提出更高要求。早期,宝钢采用三塔一均工艺,其H2纯度达99.99%。随着新能源汽车、工业制甲醇等行业快速发展,对H2的供应量以及纯度要求更高,五塔三均工艺逐渐成为主流。五塔三均工艺采用5台吸附塔、1台顺放气缓冲罐和1台H2缓冲罐,运行过程中确保2台吸附塔始终处于吸附状态,另外3个吸附塔则处于不同再生阶段[19]。该工艺在一定程度上降低了工况波动,实现H2连续生产。同时,降低了高压气体对吸附剂的冲刷与破坏,降低生产运行成本。此外,H2纯度突破99.999%。有效降低变压吸附解吸气中H2含量,热值提升63.2%,达29 093 kJ/m3,可用于电力生产[20]。焦炉煤气变压吸附制氢技术的氢回收率普遍不高,在65%~70%,大量CH4未得到有效利用,只有少部分返回炼焦炉中作为燃料供热。三源制氢公司采用两段法吸附技术[21],将H2回收率成功提高至95%以上。
该工艺运行过程中可能存在以下问题:产品H2中氧含量较高,H2纯度降低,产氢量下降。对于氧含量超标,由于吸附剂对O2的吸附能力有限,要求原料气中O2含量控制在设计标准内。对于产氢量低这一问题,关键在于控制原料气温度。温度不宜高于40 ℃,高于设计温度会导致预净化效果不理想,造成后续吸附脱除工序中的吸附剂中毒失活,进而引起H2精制工序气体杂质成分含量超标,超出吸附剂最大处理能力。控制原料气温度的关键在于前端冷却装置,确保原料气温度在40 ℃以下[21]。另外,压缩机后端冷却装置出口处易结垢,须定期清理。三源制氢公司在此处增加了备用冷却装置,确保其中一台装置始终处于工作状态。原料气中N2浓度对制氢影响很大,N2体积分数降低2%,H2回收率由47%增至55%,能耗降低50%[22]。H2产量低也可能与变压吸附塔中吸附剂的使用比例有关,CH4含量决定了吸附时间,而分子筛对CH4的吸附能力固定。适当增加吸附塔中分子筛比例有利于增强CH4吸附,提高H2产量。当吸附塔前后压差≥0.1 MPa时,表明吸附剂已经接近失活[19],导致H2产量下降,需及时更换催化剂。
采用多种技术手段耦合可获得更高的H2回收率和纯度。BANG等[23]将设计的Pd-Cu催化膜反应器与四塔变压吸附装置联用,获得99.999 1%高纯氢和91.37% H2回收率,H2中CO体积分数降至8.67×10-6。传统氢气PSA使用70%活性炭和30%的5A沸石,CO去除效果不明显。VAN ACHT等[24-25]采用双床真空变压吸附(VPSA)和电化学H2净化压缩(EHP/C)技术偶联,对焦炉煤气中H2进行净化与压缩,如图2所示。其中,VPSA柱分别用活性炭和CuCl(7.0)-活性炭填充,选择性地吸附CO2和CO;EHP/C的堆叠电流为37~52 A。VPSA-EHP/C工艺的H2回收率和纯度分别达90.00%、99.99%,适用于焦炉煤气、氯碱工业尾气等副产气的净化、压缩。MOF UTSA-16因其较高的CO2吸附选择性用于CO2脱除,测定H2、N2、CO、CH4和CO2在UTSA-16挤出物上的吸附亨利定律常数和相互扩散时间常数[14]。该净化工艺可使产品H2纯度达99.99%以上,H2回收率和产率分别达93%~96%、2.0~2.8 mol/(kg·h)。BREA等[26]比较了MOF UTSA-16和BPL活性炭净化甲烷蒸汽重整(SMR)H2的能力,试验和模拟结果均表明BPL活性炭在氢纯度和回收率方面均优于UTSA-16。

图2 VPSA-EHP/C H2分离压缩工艺流程
Fig.2 Illustration of VPSA-EHP/C hydrogen separation and compression method
沸石常被用作变压吸附剂。两阶段双床八步工艺吸附剂选用改性活性炭AC5-KS和沸石13X-Ca,H2-PSA阶段可获得99.98%的H2`纯度和79%的H2回收率,CO2-PSA阶段可获得92%的CO2纯度和98%的 CO2回收率,实现H2和CO2共回收[27]。利用模拟工具PSASIM模拟CaX沸石和5A沸石从焦炉煤气中分离H2的差异性,结果表明,在相同产品纯度(99.7%以上)下,进料压力为3×105 Pa时,CaX沸石的H2回收率高于5A沸石[28]。CaX对氮的去除效果优于5A沸石,但对CO和CH4的去除效果不及5A沸石。另外,加入清洗步骤可显著提高H2纯度和回收率,回收率由65%提升至90%。DELGADO等[29]通过试验获取BPL活性炭对气体分子的亲和力,顺序为H2<CO<CH4<CO2,13X沸石的亲和力顺序为H2<CH4<CO<CO2,CO与沸石中Na 的静电相互作用是造成CO和CH4在13X沸石中吸附顺序存在差异的原因。四塔两吸附工艺在处理炼油厂尾气时相比聚合物膜分离、液体溶剂吸附净化H2更具经济性,但H2纯度不高,仅99.4%,无法满足燃料电池需要[30]。
采用变压吸附获得的H2纯度可达99.99%以上,甚至99.999 9%,满足新能源汽车、氢冶金、甲醇生产等需求。其次,自动化程度高,对原料适应性好,富氢气体(H2体积分数>20%)提纯效果明显。但设备繁琐、占地大、工艺复杂、维护量大、投资成本高,对操作人员技术水平要求严苛。变压吸附技术在有效利用焦油、CH4等杂质方面还存在不足,造成一定资源浪费,单一的PSA工艺还无法高效利用焦炉煤气。
1.2 膜分离制氢
膜分离技术原理如图3所示(绿色球代表氢分子,蓝色球代表杂质分子),该技术借助膜两侧压差迫使氢分子选择性穿过膜,在另一侧产品区富集,杂质气体则滞留在初始侧,从而达到分离H2的目的。膜分离气体过程可概括为气体的溶解、扩散、(产品侧)解析。膜分离效果与3个参数有关:膜两侧各气体组分的分压差、膜面积、膜选择性。理论上压差越大,H2分离纯度越高,最终达到上限值,但压力增加会导致相应能耗大幅提升。气体的相对渗透速度[31]为:H2O>H2>He>H2S>CO2>O2>Ar>CO>CH4>N2。经过冷凝除水后焦炉煤气中的H2优先穿过膜,在低压侧形成富氢。与变压吸附相比,膜分离技术获得的H2纯度较低,在80%~90%,H2收率为50%~85%,且原料气中H2体积分数高于30%才能获得一定经济效益。与变压吸附法、深冷法相比,其制氢成本低、操作简单,适用于对H2纯度要求不高的生产部门。

图3 膜法H2分离技术分离原理
Fig.3 Separation principle of hydrogen separation technology by membrane
根据制备材料的差异性可将回收H2的气体分离膜分为有机膜、无机膜、复合基质膜。针对H2分离的有机膜主要有聚醚酰亚胺(PEI)、聚苯并咪唑(PBI)、聚醚砜(PES)、醋酸纤维等,无机膜有金属靶及其合金膜、分子筛膜、质子电子混合导体膜等[32]。Y
 EZ等[33]评价了商用PEI、PES和PBI聚合物膜分离氨合成、钢铁厂、甲醇生产工业富氢尾气中H2的性能,其中PEI膜处理上述3种尾气获得的H2纯度分别为99.7%、98.8%、95.4%,仍无法满足质子交换膜燃料电池等清洁燃料系统的需求。TANAKA等[34]制备了不同结构的聚酰亚胺聚合物膜,并测试了其气体渗透率和选择性,认为六氟丙烷会导致膜对H2/CO和H2/CH4的选择性降低。19种测试膜中6FDA-APAP和6FDA-mp′ODA膜具有优异的H2/CH4选择系数,是理想的H2分离膜材料。Pd膜具有高H2回收率和选择性,田文中等[35]利用化学镀法制备了钯银合金无机复合膜,对经冷冻处理净化后的焦炉煤气进行膜分离H2试验,最终获得纯度99.99%的纯氢。中国科学院大连化学物理研究所李慧团队[36-38]研制的不锈钢钯复合膜超纯H2纯化器的产氢量达到30 m3/h(标况下),H2纯度为99.999 999%。将聚砜负载在40%沸石上得到混合基质膜[39],相比纯聚砜,其H2/CO2分离选择性由1.53提升至3.57。
EZ等[33]评价了商用PEI、PES和PBI聚合物膜分离氨合成、钢铁厂、甲醇生产工业富氢尾气中H2的性能,其中PEI膜处理上述3种尾气获得的H2纯度分别为99.7%、98.8%、95.4%,仍无法满足质子交换膜燃料电池等清洁燃料系统的需求。TANAKA等[34]制备了不同结构的聚酰亚胺聚合物膜,并测试了其气体渗透率和选择性,认为六氟丙烷会导致膜对H2/CO和H2/CH4的选择性降低。19种测试膜中6FDA-APAP和6FDA-mp′ODA膜具有优异的H2/CH4选择系数,是理想的H2分离膜材料。Pd膜具有高H2回收率和选择性,田文中等[35]利用化学镀法制备了钯银合金无机复合膜,对经冷冻处理净化后的焦炉煤气进行膜分离H2试验,最终获得纯度99.99%的纯氢。中国科学院大连化学物理研究所李慧团队[36-38]研制的不锈钢钯复合膜超纯H2纯化器的产氢量达到30 m3/h(标况下),H2纯度为99.999 999%。将聚砜负载在40%沸石上得到混合基质膜[39],相比纯聚砜,其H2/CO2分离选择性由1.53提升至3.57。
张健青设计了一种耦合甲烷蒸汽重整、水煤气变换制氢和分离的膜增强制氢工艺,可通过膜渗透和变温吸附分离出不同纯度的H2[40]。模拟结果表明,H2回收率达83.3%,最终的驰放气成分主要为CO2和N2。利用膜分离H2时应注意,水会损坏中空纤维膜,导致膜分离效果降低[41]。混合气体进入膜分离器前需要经过换热器加热处理,热源为0.7 MPa饱和蒸汽。膜两侧压差对膜寿命影响很大,为防止破坏,要求操作时膜两侧压差小于10 MPa。
1.3 深冷法分离产氢
深冷法又称低温精馏法,其原理是利用不同气体的沸点差异,通过降温使除目标气体外其他组分液化,从而达到分离目的[42]。焦炉煤气各气体组分沸点如图4所示,焦炉煤气中H2沸点为-252.6 ℃,远低于杂质沸点[43-47]。经过逐级降温,杂质气体组分在不同阶段被冷凝,实现逐级分离。深冷法的操作压力在2.0~4.0 MPa,随操作压力提升,温度降低。而压力越高,相应能耗越高,H2损失随之增加。该方法得到的H2纯度不高,在83%~88%,常与变压吸附联用进行深度提纯[48-49]。深冷法是最早用于分离焦炉煤气制氢的方法,也适用于CH4、CO等气体的综合分离、回收。深冷制氮装置由空气压缩与输送系统、空气预冷系统、空气净化系统、空气分馏塔、低温液体贮存系统、仪表空气压缩贮存系统组成,存在预冷启动、大修解冻过程,耗费时间长,不宜常开常停[50]。

图4 焦炉煤气各气体组分沸点
Fig.4 Boiling point of different gas components in coke oven gas
深冷法已被广泛应用于N2、CO2、CO、CH4等气体的分离。深冷法制氮的N2纯度可达99.999%以上,变压吸附纯度较低,在95.0%~99.9%[51]。ATSONIOS等[52]提出一套利用深冷法从富CO2气体中分离H2并捕集CO2的模型,模拟结果表明该模型可实现可燃气体分离,并获得纯度高于99%的CO2流。深冷法分离CO技术又分为甲烷洗和部分冷凝2道工艺[31]。甲烷洗工艺利用低温下液态甲烷对CO的强溶解能力,实现CO和H2分离。产品气CO纯度>99%,H2纯度>98%,且为中高压。部分冷凝工艺利用气体各组分冷凝点差异进行CO分离,CO纯度大于99%且为低压。焦炉煤气经除杂、甲烷化、干燥净化等工序后进行深冷液化,可获得液化天然气[53-54]。该工艺投资成本大,技术较复杂,可获得较高的液化天然气产量,适用于大型钢铁联合企业。内蒙古恒坤化工借鉴Davy公司甲烷化技术建成国内首套焦炉煤气制液化天然气装置,并成功投产。其采用的冷箱可将原料气温度降至-180 ℃,从而产出-162 ℃的液态天然气[55]。
然而,由于深冷设备复杂,操作难度系数大,H2分离难度高,预冷时间长,需专人实时监控,投资成本高,回报周期长,因而限制了深冷法在焦炉煤气制氢领域的发展。
2 化学方法重整制氢
2.1 传统催化和非催化重整制氢
焦炉煤气催化重整和非催化重整以水蒸气、CO2、O2或空气为气化氧化剂,选择性氧化CH4,产生富氢合成气,再通过PSA等物理方法净化、分离、提纯,从而获得纯氢。焦炉煤气非催化重整制氢是在一定压力下通过高温增强作用促进反应气转化,而催化重整制氢是借助催化剂对焦炉煤气中的气体分子进行活化,实现不同气体分子在催化剂活性位点上的重整,反应一般在常压下进行。主要反应如下:
水气重整:CH4 H2O![]() CO 3H2,
CO 3H2,
(1)
部分氧化:CH4 0.5O2![]() CO 2H2,
CO 2H2,
(2)
干重整:CH4 CO2![]() 2CO 2H2,
2CO 2H2,
(3)
水气变换:CO H2O![]() CO2 H2,
CO2 H2,
(4)
逆水气变换:CO2 H2![]() CO H2O。
CO H2O。
(5)
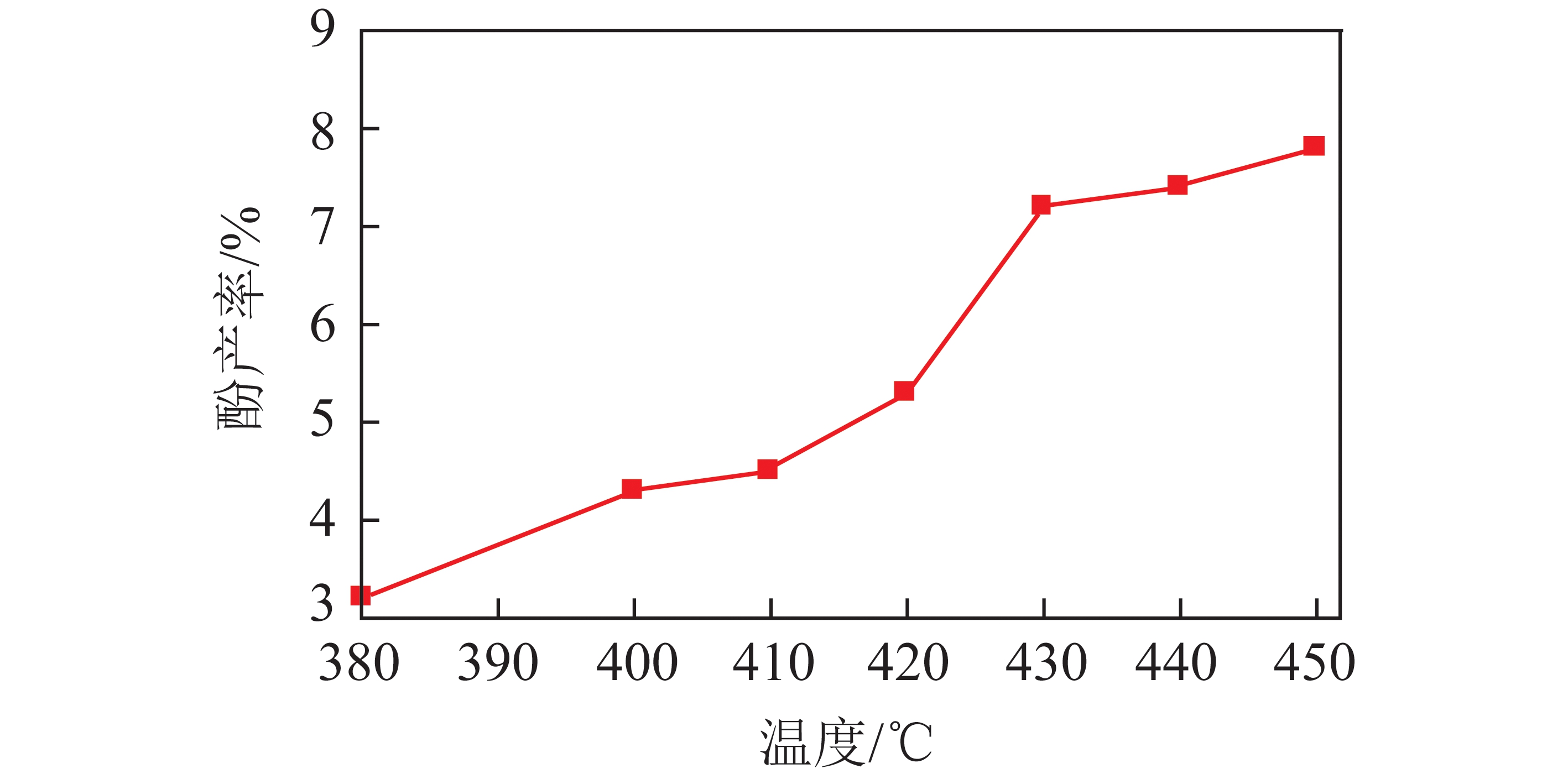
Ni是焦炉煤气干重整制氢的主要活性金属。ZHU等[56]发现对La0.6Sr0.4CoO3的Co位进行Ni掺杂可有效提高CH4和CO2的转化率以及H2选择性,其中800 ℃焙烧的La0.6Sr0.4NiO3表现出最佳的催化活性和抗积碳性,中间相La2O2CO3的存在可促进CH4选择性生成合成气。在蒸汽重整和干重整耦合反应中,Sm元素的修饰使Ni/M-Al2O3具有高的电负性和碱度[57],镍纳米颗粒与Al2O3表面碱性位点表现出强相互作用。通过比较Ni-MgO-Al2O3催化剂的不同制备方法发现,共沉淀法具有最佳的反应活性,特别是pH为12时,在600 000 h-1大空速下运行50 h,CH4和CO2转化率可平稳维持在90%[58]。SHEN等[59]探究了CO2、O2、焦炉煤气非催化重整、催化重整、两步法重整的重整性能,其中两步法重整的焦炉煤气重整性能更佳,第1阶段H2燃烧供热,驱动第2阶段具有吸热特性的CH4重整反应和逆水气变换反应,H2/CO体积比为2.10时,CH4和CO2转化率分别为98.96%、62.32%。在O2参与下,CO2作为重整的碳源可在0.52~3.83内调整H2/CO。采用溶胶凝胶法 浸渍法制备了系列Ni/La2O3-ZrO2催化剂,10% Ni负载量的催化剂在800 ℃ 具有超过95%的CH4和CO2转化率[60-61]。在此基础上探究少量贵金属(Ru、Pd、Ag)添加的影响,贵金属的添加对晶须型碳物种起到一定抑制作用,同时还可提高焦炉煤气重整活性[62]。
相比单金属负载,由于形成Ni-Co固溶体,双金属负载具有更高的干重整性能和抗积碳性[63]。催化剂的制备方法、浸渍顺序、pH是影响催化性能的重要参数,JING等[64]探究了Ni和Co前驱体在MgO上的浸渍顺序对焦炉煤气重整活性的影响,结果表明浸渍顺序影响Ni-Co-Mg三者之间相互作用,进而影响Ni颗粒大小、金属分散度、CO2的吸附能力。其中,Ni/Co/MgO催化剂(先浸渍Co,再浸渍Ni)的CO2转化率可达80%左右。MgO与Al2O3质量比对催化性质的影响研究表明,二者比例不仅影响催化剂碱性,而且影响催化剂的分散性和催化剂表面还原性[65]。另外,结构也是影响催化性能的重要参数。通过形貌调控将Ni限域到MCM-41中可有效提高抗积碳性和循环稳定性,使负载10% Ni的催化剂在200 h内仍保持良好的活性[66]。通过水热法在棒状Si-1分子筛上原位掺杂Ni,该催化剂的TOFs是传统1% Ni/La2O3-ZrO2的3倍[67]。
焦炉煤气水气重整反应可获得富氢合成气,但常伴随逆水气变换等产CO2副反应的发生,通过CO2吸附剂及时将其移除,促使反应正向进行,实现CH4转化和产物分离,从而获得更高纯度的H2和CO。CaO用于CO2吸附增强促进焦炉煤气中CH4和CO转化研究很多[68-69],核心是强化副反应,实现H2的分离、净化以及CO2捕集。在Ni/γ-Al2O3催化剂上添加CaO对其进行改性,可增加碱性位点,促进CH4和CO2的转化[70]。转炉炼钢炉渣中富含Ca、Al、Fe、Mg等金属氧化物,可用于吸附增强蒸汽-焦炉煤气重整制氢。ZHANG等[68]对钢渣进行研磨、酸洗、过滤、干燥(滤液)、焙烧获得钙基吸附强化蒸汽重整吸附剂,经过35次吸附/脱附,CO2吸附量仍可达0.48 g/g(以吸附剂计),这与介孔结构以及MgO、Fe2O3的存在有关。还考察了浸出酸浓度对上述钙基吸附剂吸附CO2性能的影响,其中,乙酸浓度为1 mol/L时CO2的循环吸附性能最佳[71]。Ca12Al14O33基吸附剂也被用于焦炉煤气蒸汽重整中,高温焙烧法可获得大比表面积和更好的催化活性[72]。热力学和动力学研究表明,相比传统蒸汽重整,CO2吸附强化蒸汽重整可获得超过95% H2的产品气,重整温度有所降低,CH4重整反应是限制性环节[73-74]。800 ℃高温下,CaO具有比Fe3O4更高的水气变换活性,且对硫的吸附能力不足镍的1/3。处理含H2S的粗焦炉煤气时,Ni/钙铝石催化剂通过牺牲Ni而保护位于表面的活性相CaO。此外,CO2、CO和H2的存在会对H2S在CaO上的吸附产生一定抑制作用,从而使催化剂表现出优异的水气变换活性[75]。催化剂结构对水气变换活性影响很大,特别是H2S和HCl存在时,强Ni-载体相互作用可降低其毒害作用[76]。一种用于膜吸附增强蒸汽-焦炉煤气重整工艺,催化剂为双金属Ni-Fe/钙铝石,可以在线分离H2,产品H2纯度达99.9%(未计算N2),膜与快速反应区越近,其对焦炉煤气重整反应的促进作用越显著[77-78]。CO易使H2燃料电池Pt电极中毒,付威等[79]探究了Cu/ZnO/Al2O3催化剂前驱体中铝含量对模拟焦炉煤气(φ(H2)∶φ(CO)∶φ(CO2)=0.75∶0.06∶0.19)重整制氢催化活性的影响,认为适当的铝含量可使催化剂产生协同效应,增强低温水气变换活性,促进CO转化。反应温度在483 K 以上时,Al摩尔分数为12%催化剂的CO转化率接近理论值97%。
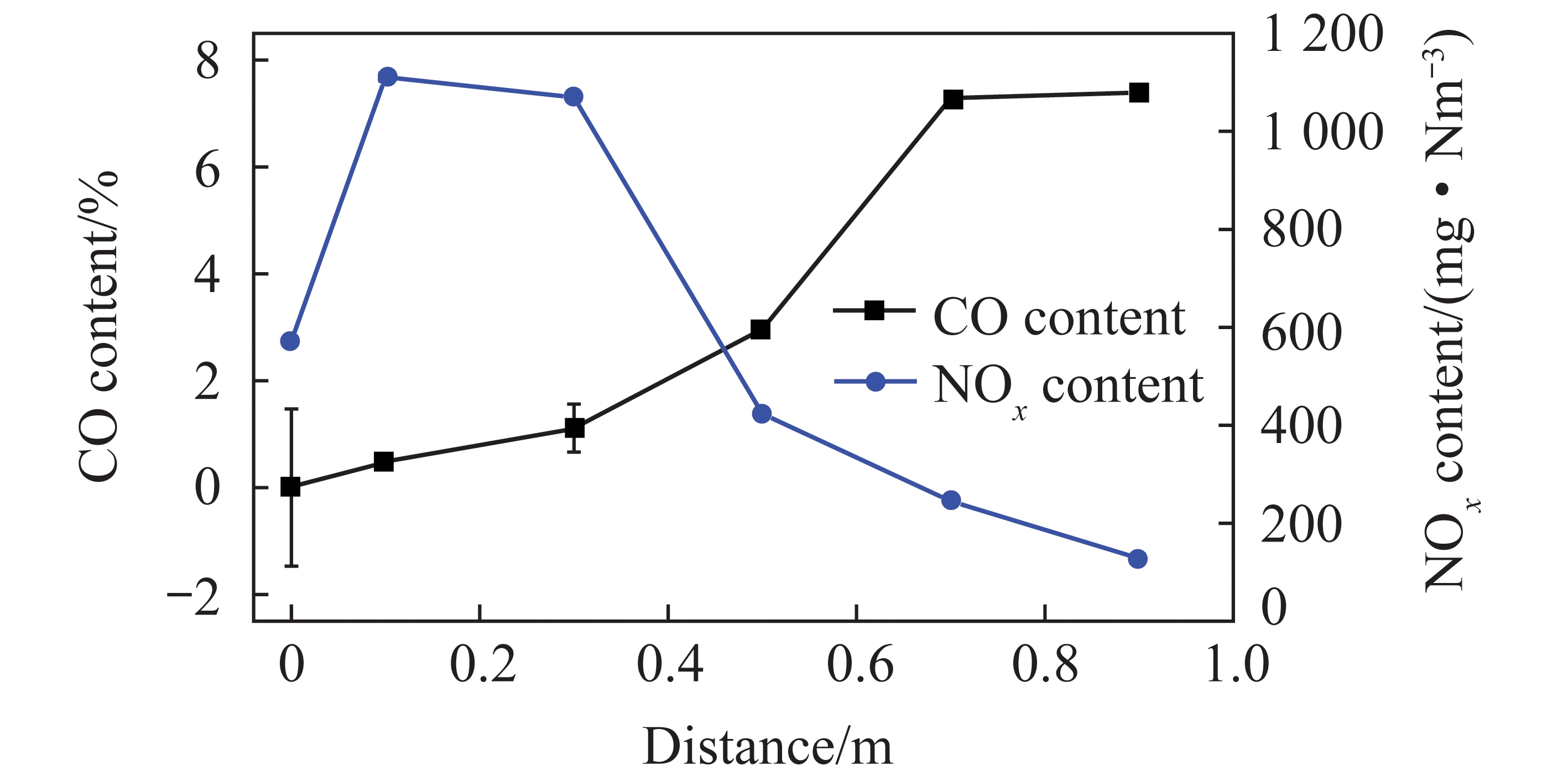
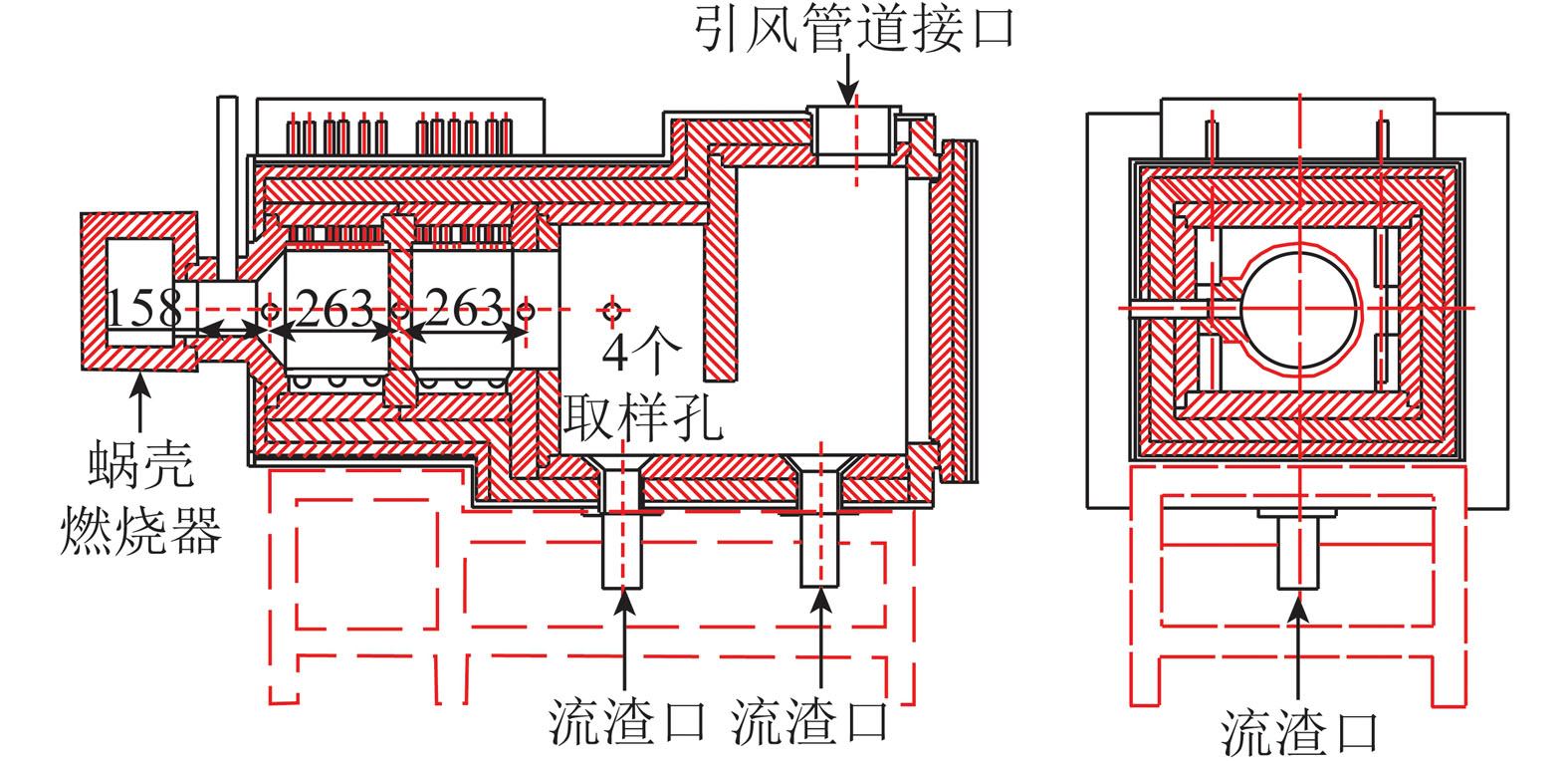
焦炉煤气非催化重整要求条件苛刻,文献报道较少。ANGEL等[80]对焦炉煤气、高炉煤气共进料非催化干重整反应进行数值模拟,在1 350 ℃、5.5×105 Pa、焦炉煤气与高炉煤气(COG/BFG)比值0.6的条件下,CH4和CO2转化率分别为95.0%、78.5%,为冶金尾气的高效转化利用提供理论指导。也有学者将热焦炉煤气与焦油进行部分氧化和重整,成功实现5 h连续产氢,产率达1 m3/h(标况下),98%的含碳气体被转化成H2和CO[81]。NORINAGA等[82]在1/10工业生产规模中试设备上进行焦炉煤气非催化重整试验,在最佳条件下操作重整器,可使合成气体积流量增加1倍,粗COG中烃类转化率达95%以上。
2.2 氧传输膜重整制氢
氧传输膜重整制氢的本质是CH4部分氧化。通过膜反应进行氧和电子的传递,使CH4在不与空气直接接触的情况下发生部分氧化,产生合成气。常见的5种OTM反应器结构示意如图5所示。

图5 5种类型的OTM反应器
Fig.5 Five types of OTM reactors
焦炉煤气中丰富的H2易使膜产生氢脆,造成氧
传输膜破损,是限制其应用于焦炉煤气制氢的关键因素。氧传输膜材料以萤石型(CeO2、ZrO2等)和钙钛矿型(A位一般为La、Ba、Sr,B位一般为Fe、Co)为主,其中钙钛矿型膜材料研究最广泛。以BaCo0.7Fe0.2Nb0.1O3-δ 单相钙钛矿为OTM(未添加催化剂),氧渗透侧为空气,其CH4转化率为92%,H2选择性为90%,CO选择性为104%,透氧速率达15 mL/(cm2·min),在1 148 K下运行550 h活性几乎不下降[83]。YANG等[84]在通入焦炉煤气侧添加NiO/MgO催化剂,由于透氧速率提高,部分O2-与H2反应生成水,导致H2选择性下降。金属Ta含量对BaCo0.7Fe0.3-xTaxO3-δ陶瓷膜结构稳定性和氧渗透性的影响表明,Ta的添加使氧渗透性略下降,但显著提高了膜在还原气氛下的相结构稳定性,降低氧空位浓度[85-86]。上侧以CO2/He为吹扫气时由于碳酸盐的形成导致氧渗透通量骤降,而切换成He时由于碳酸盐分解氧渗透通量恢复。普遍认为,氧分压是影响氧渗透通量的关键因素,富还原性气体如H2、CH4、CO与氧结合能力强,可促进氧的转移或消耗,因而可显著提高OTM的氧渗透通量[87-89]。2种新型管式膜反应器被应用于焦炉煤气制氢反应,膜管内均通入空气,管外通焦炉煤气,同时填充一定量催化剂,有效提高了焦炉煤气制氢活性[90-92]。SrFeCo0.5O3-δ透氧膜在CH4气氛下可稳定存在,而在焦炉煤气气氛下遭到破坏,XRD分析表明富氢气氛会导致膜的相分离,降低其寿命[93]。
CO2和SO2耐受性是限制氧传输膜工业化应用的另一关键因素。碱土金属常用于膜的合成,然而其易与CO2和SO2结合,生成碳酸盐和硫酸盐,降低氧传输膜的机械性能[94]。钙钛矿型氧传输膜研究较多,特别是A位元素为碱土金属Ba和Sr。BaCo0.7Fe0.2Nb0.1O3-δ氧透过通量高,是一种有前景的膜材料,但稳定性较差。经过A位缺陷处理后得到的Ba0.9Co0.7Fe0.2Nb0.1O3-δ在400 h耐久性试验中氧透过通量和CH4转化率均未下降,稳定性明显优于BaCo0.7Fe0.2Nb0.1O3-δ[95]。氧传输膜设计为3层结构,即致密薄膜和2个多孔支撑层,其中一侧多孔支撑层上负载有Ni,可进一步提升其反应活性和稳定性[96]。而对于LaFe0.8Cu0.2O3氧传输膜,在低浓度SO2气氛(小于2×10-5)中,由于SO2和反应物的竞争性吸附及表面亚硫酸盐和硫酸盐物种对活性位点的覆盖,出现可逆性失活[97]。SO2体积分数达8×10-5时钙钛矿被严重硫酸化,结构破坏,出现La2(SO4)3相和Fe2O3相,导致不可逆失活。
双相氧传输膜比单向氧传输膜在CO2和SO2耐受性方面更具优势,因而受到广泛关注[98-102]。CHEN等[103]认为,调整B位中Co/Fe物质的量比可提高La0.6Ca0.4Co1-xFexO3-δ钙钛矿单相氧传输膜的CO2耐受性,其中x为0.7时,在空气/CO2气氛中氧透过通量为0.5 mL/(min·cm2)。双相氧传输膜的CO2耐受性比单向膜更具优势,经2 050 h CO2耐受试验后Ce0.9Pr0.1O2-δ-La0.5Sr0.5Fe0.9Cu0.1O3-δ双相膜的XRD中未观察到碳酸盐物种[104]。通过分析60% Ce0.8M0.2O2-δ(M=La,Pr,Nd,Sm,Gd)-40% La0.5Sr0.5Fe0.8Cu0.2O3-δ双相氧传输膜的氧透过通量及CO2耐受性发现,粒径和电导率是影响氧传输膜性能的关键参数[105]。粒径越小、电导率越高,膜性能越好。NiFe2O4-Ce0.8Tb0.2O2-δ双相膜在含CO2、SO2、H2O的复杂气氛中能够稳定存在,而单相膜La0.6Sr0.4Co0.2Fe0.8O3-δ 则会分解产生SrCO3和SrSO4。SO2与La0.6Sr0.4Co0.2Fe0.8O3-δ作用性明显强于CO2,在CO2中加入2.0 ×10-3 SO2能抑制SrCO3的形成[106]。
氧传输膜在焦炉煤气制氢中的应用还局限于单侧制合成气,氧渗透侧若以水蒸气取代空气则可制取纯H2。第1个耦合水分离制氢与乙烷脱氢制乙烯的中空纤维膜反应器在2010年首次被报道,采用的膜材料为BaCoxFeyZr1-x-yO3-δ,在800 ℃下可以实现1.0 cm3/(min·cm2)的产氢速率,乙烯产率达55%[107]。ZHU等[88]以La0.9Ca0.1FeO3-δ为氧传输膜,探究CH4制合成气偶联水分离制氢,在不同还原气氛下(CO、H2/CO、CH4)的产氢速率依次为0.061 7、0.052 3、0.039 0 μmol/(s·cm2),膜还原侧和氧化侧材料晶粒的生长均与还原气氛有关,生长速率依次为CH4> H2/CO >CO。xCe0.85Pr0.15O2-δ(CP)-(100-x)Pr0.6Sr0.4Fe0.9Al0.1O3-δ(PSFA)双相氧传输膜中60CP-40PSFA膜在100 h测试中产氢保持率为90%,产H2速率为0.99 mL/(cm·min),吹扫侧Fe(SrO3)和Sr3Fe2O7的形成是导致产氢速率下降的主要原因[87]。JIA等[108]制备了双相氧传输膜Ce0.9Pr0.1O2-δ-Pr0.1Sr0.9Mg0.1Ti0.9O3-δ用于净化H2,进料侧为含氢混合气,吹扫侧为水蒸气。反应过程中进料侧的氢与氧结合变成水,吹扫侧的水失氧变成纯氢,940 ℃下产氢速率可达0.52 mL/(min·cm2)。75% Sm0.15Ce0.85O1.925-25% Sm0.6Sr0.4Al0.3Fe0.7O3-δ不对称OTM也被用于H2分离净化中,在长时间稳定性测试中可耐受2.0×10-4 H2S,H2分离速率达16.3 mL/(min·cm2),为氧传输膜用于含硫杂质粗焦炉煤气高效制氢提供可能。
氧传输膜重整制氢优势在于可以实现氧空分离和焦炉煤气部分氧化一体化操作,不需纯氧;H2浓度高,易分离;整个反应更加受控,有效避免O2直接与反应气接触,防止爆炸发生。相比单相氧传输膜,双相氧传输膜可在高温、复杂气氛下保持稳定,是未来研究方向,特别是含钙钛矿型。膜反应器焦炉煤气制氢还须克服以下问题:氧离子和电子传输速率慢、氢脆性、膜面积受限、膜的CO2、SO2和H2S耐受性差。
2.3 化学链重整制氢
化学链技术兴起于20世纪80年代,其中,化学链燃烧技术已被应用于发电,化学链制合成气、H2、CO的研究也较广泛,其技术示意如图6所示。该技术由2部分构成:① 将燃料气体如CH4、焦炉煤气等还原性气体通入燃料反应器中,与载氧体(供氧)反应生成富氢合成气;② 将H2O、CO2等氧化性气体通入空气反应器中,氧化性气体中的氧补给到载氧体,实现载氧体再生,同时产生H2、CO等高附加值气体。化学链技术和氧传输膜技术的核心思想是实现物质的分离、净化与提纯,区别在于化学链技术使用的反应器不局限于固定床,也适用于工业上主流的流化床。其中,氧传输媒介为载氧体(Oxygen Carrier,OC)。

图6 化学链转化技术示意
Fig.6 Schematic illustration of chemical looping conversion technology[109]
化学链技术应用于焦炉煤气产氢相关文献报道还较少,特别是重整制氢。焦炉煤气化学链重整制氢可以实现富氢合成气和纯氢或CO共产,工艺关键在于选择性转化CH4为合成气,与原有H2和CO共同构成富氢合成气。实际操作中H2、CO同CH4在还原载氧体时存在竞争性关系,应避免前者优先氧化消耗,从而降低H2产出。其主要反应如下:
化学链甲烷部分氧化:
燃料反应器
δCH4 MxOy![]() δ(CO 2H2) MxOy-δ,
δ(CO 2H2) MxOy-δ,
(6)
空气反应器
δO2 2MxOy-δ![]() 2MxOy。
2MxOy。
(7)
化学链甲烷水气重整:
燃料反应器
δCH4 MxOy![]() δ(CO 2H2) MxOy-δ,
δ(CO 2H2) MxOy-δ,
(8)
空气反应器
δH2O MxOy-δ![]() δH2 MxOy。
δH2 MxOy。
(9)
化学链甲烷干重整:
燃料反应器
δCH4 MxOy![]() δ(CO 2H2) MxOy-δ,
δ(CO 2H2) MxOy-δ,
(10)
空气反应器
δCO2 MxOy-δ![]() δCO MxOy。
δCO MxOy。
(11)
实现最大化产氢目标可在空气反应器中引入水蒸气,实现两步共产氢。化学链焦炉煤气两步共产H2受到关注,掺杂改性LaFeO3时,Sr的加入可增加载氧体的氧空位,提高抗积碳能力和水解离阶段的H2纯度[110]。当Sr的A位掺杂量和La相当时,在水蒸气氧化阶段可持续产氢约40 min,H2纯度为99.85%。比较了COG-H2O和COG-H2O-O2工艺,结果表明水蒸气氧化后再用O2进行深度氧化可使载氧体催化活性较高。通过分析CO、H2、CH4间的氧化竞争关系发现温度是影响CH4选择性转化为合成气的重要参数。镍具有优异的CH4催化性能,是仅次于贵金属的活性金属。通过镍掺杂LaFeO3可获得优异的焦炉煤气催化活性[111],相比LaFeO3原样,LaNi0.07Fe0.93O3-λ的CH4转化率、合成气产量及水解离阶段H2产量分别提升了99.59%、47.13%、72.77%,达98.60%、12.58 mol/kg、3.30 mol/kg。结合试验表征和密度泛函理论(DFT),认为Ni离子掺入LaFeO3晶格后弱化了Fe—O键,使晶格氧迁移率增加。还原初期,表面Ni析出可有效活化CH4,促进其转化。XIANG等[112-115]提出了大量关于焦炉煤气制氢耦合甲醇、乙烯、氨、CH4生产的工艺,认为工艺耦合可提高![]() 效率与H2纯度,显著提升CO2捕集率,达100%,加入PSA净化工艺及富氧燃烧在经济性上更具优势。ZHAO等[116]提出一种利用化学链技术高效转化COG和粉煤生产甲醇和氨的工艺,可实现88.8%的氢利用率与78.7%的
效率与H2纯度,显著提升CO2捕集率,达100%,加入PSA净化工艺及富氧燃烧在经济性上更具优势。ZHAO等[116]提出一种利用化学链技术高效转化COG和粉煤生产甲醇和氨的工艺,可实现88.8%的氢利用率与78.7%的![]() 效率。
效率。
利用化学链技术选择性转化CH4制合成气和H2研究较广泛,化学链CH4水气重整的载氧体多选用铁基、铈基、镍基及钙钛矿[109,117]。铁基载氧体来源广、易获得,但循环性能较差。HE等[118-119]采用不同方式对LaFeO3载氧体进行改性,探究其对化学链CH4重整反应的影响。载氧体上存在表面氧和晶格氧,前者易使CH4发生完全氧化生成H2O和CO2;后者倾向于部分氧化,生成CO和H2。三维有序大孔LaFeO3比普通形式的LaFeO3具有更高的储氧量,更易在较长时间内持续生成H2/CO体积比为2的合成气。NEAL等[120-121]则将LaFeO3做成核壳结构,认为CH4还原Fe2O3@LSF时存在4个阶段(图7):① 以深度氧化为主的初始阶段;② 深度氧化和选择性氧化共存的过渡阶段;③ 活性增加的选择性氧化阶段;④ 以CH4裂解为主的积碳阶段。与其他几种常用的铁基氧化还原催化剂相比,核壳型载氧体在CH4制合成气中具有更高的活性和选择性。肖睿团队对A0.25Co0.25Fe2.5O4(A = Co,Mn,Cu,Ni)三元混合尖晶石氧化物载氧体进行研究[122],Cu0.25Co0.25Fe2.5O4在550 ℃水氧化阶段的H2产量高达11.9 mmol/g,XPS和XRD分析结果显示该载氧体具有高的相可逆性。Fe2O3和CeO2间存在强相互作用,可降低还原温度,CeO2的存在可显著提高Fe2O3的氧化还原性能[123-124]。5% Fe含量可完全进入CeO2晶格中形成固溶体,其氧化还原性明显高于纯CeO2,而铁含量较高时则会存在非晶态或晶态的Fe2O3粒子。铈铁固溶体在高温下并不能稳定存在,温度高于800 ℃时可在Ce0.8Fe0.2O2-x载氧体上观察到游离的Fe2O3相[125]。铈修饰的Fe2O3具有更好的抗烧结性[126],且在化学链水气重整反应中加入摩尔分数20%的CeO2时,产氢量可达8 651 μmol/g。

图7 CH4还原Fe2O3@LSF过程中气态产物的瞬时产量
Fig.7 Temporal yields of gaseous products during the reduction of Fe2O3@LSF with CH4
在实验室范围内,载氧体的设计、制备与性能评价研究较多,但化学链技术仍停留在中试阶段,反应器大型化、载氧体的循环稳定性与硫物种耐受性、载氧体规模合成工艺的成熟性及性能评价标准体系等尚未成熟,是限制其工业化的关键因素,也是今后研究重点。焦炉煤气组分复杂,载氧体的硫物种耐受性、各气体组分间的竞争性吸附应受到足够重视。
3 脱硫脱硝与杂质利用
热焦炉煤气中含有硫化物、NOx、NH3等气体污染物以及焦油、苯等有机物,直接利用易导致后续制氢工艺使用的吸附剂、催化剂中毒,降低使用寿命,增加运维成本,严重阻碍焦炉煤气的利用,严重危害环境。《关于推进实施钢铁行业超低排放的意见》(环大气[2019]35号)对焦炉烟气中SO2、NOx排放质量浓度做出规定,要求分别低于30、130 mg/m3。焦油、苯等有机物利用率较低,促进有机物的转化是提高焦炉煤气制氢效率和经济效益的重要环节。
常用的焦炉煤气除杂、净化方式为溶液吸收以及固体催化/吸附。焦炉烟气脱硫方法可分为氨-硫酸铵湿法、喷雾旋转半干法(SDA)、碳酸氢钠干法(SDS),其中SDA半干法脱硫是焦化企业脱硫脱硝的主流技术,脱硫废渣的处理是难题。此处主要阐述处于探索阶段的技术和材料,对已应用的技术不再赘述。脱硫褐铁矿作为脱硫剂时,焦炉煤气中CO对脱硫有抑制作用,在无积碳情况下加入5% H2O或5% CO2可提高脱硫效果,还可将NH3几乎完全转化为N2[127-128]。褐煤含碳量在60%~77%,比表面积较大,DOU等[129-132]以褐煤负载Fe-Zn为H2S吸附剂,随金属负载量的增加脱硫效果增强。还加入Cu、Mo元素对上述吸附剂改性,发现Fe-Zn-Cu吸附剂在硫化过程中形成的复合金属氧化物在吸附剂中转化为金属硫化物,500 ℃再生过程中又转化为金属氧化物,而Mo的加入则显著提高了吸附剂的脱硫性能(即突破时间、硫容和脱硫效率)。
在噻吩加氢脱硫(HDS)催化反应中,通过不同方式添加P对Ni-Mo/Al2O3催化剂进行改性,P可削弱活性金属与载体间的相互作用,提高活性金属分散性,其中P-Ni-Mo/Al 在250 ℃下对噻吩的脱硫率达61%[133]。商业Pd/Al2O3在转化焦炉煤气中的COS、CS2和O2也有一定效果,特别是温度高于200 ℃时,通过加氢反应可有效脱除焦炉模拟气中上述杂质,实现催化剂再生[134]。
通过浸渍法将少量钒负载到煤炭气化渣上用于NOx转化,在240~290 ℃路易斯酸是NO选择性催化还原的活性位点,且在SO2存在情况下具有更好的NO移除效率[135]。α-FeOOH催化剂则可通过催化H2O2分解产生HO2·和·OH来增强焦炉煤气中NO的氧化[136]。XU等[137]从控制载体、含量、制备方法和反应条件等方面为提高K 在各种催化反应中的促进作用提出建议,并比较了不同碱金属的促进作用,认为K 在催化脱除工业燃料气中NOx、COx、VOCs方面具有一定应用前景。基于DFT分析3种焦炉煤气分子(H2S、HCN和NH3)在Fe(100)表面的吸附性能(图8),这些杂质分子与Fe(100)表面的相互作用能依次为H2S >HCN >NH3,因而H2S在催化剂表面更易产生硫沉积[138]。

图8 H2S、HCN、NH3在Fe(100)最佳吸附位点吸附前后的分态密度
Fig.8 PDOS of H2S,HCN and NH3 before and after adsorption at the optimal adsorption site of Fe(100)
超深脱除噻吩至0.1×10-6水平是焦炉煤气转化CH4工艺的必要条件,NaY分子筛具有较强的Brønsted酸性位点,可与噻吩发生聚合反应,从而有效降低噻吩含量[139]。ZOU等[140]在旋转填充床上研究了掺有20 mg/L “888”商业催化剂Na2CO3溶液的催化氧化吸附脱硫性能,该工艺相较填充塔性能更优异。周昊等[141]比较了Na2CO3溶液和Ca(OH)2溶液的脱硫特性,在一定化学计量比范围内前者的脱硫效率增长速率更快。出口烟气温度不变时,较高的入口烟气温度和烟气温降(脱硫塔内)有利于脱硫。对于吸收柱,在甲基二乙醇胺(MDEA,质量分数45%)与焦炉煤气质量比为1.3 kg/kg、气流量为500 m3/h、H2S摩尔分数为0.3%和3.0%时,H2S脱除率接近99%[142]。在最佳条件下,MDEA溶液用量和加热负荷分别降低35%和23%。也有学者将MDEA与[N1111][Arg]按照一定比例制成H2S吸附剂,比单独MDEA和([N1111][Gly])-MDEA溶液具有更强的脱硫效果[143]。在含水量小于40%条件下仅含4个筛板的塔板的H2S脱除率达100%,可显著降低能耗。汤志刚等[144]提出双氨法一体化脱硫脱硝工艺,净化后的焦炉煤气中SO2和NO质量浓度分别降至10和150 mg/m3以下,达到国家标准。以煤油为有机溶剂、L-113B为表面活性剂、蒸馏水为内相液和外相液,制备了W/O乳液,在最佳配比条件下焦油脱除率为98%[145]。以Na2CO3为碱源配置新型络合铁催化剂,H2S质量浓度由2.0~4.0 g/m3降至20 mg/m3以下,相比传统PDS催化剂,该催化剂在环保、脱硫效果方面更具优势[146]。
焦炉煤气中焦油、萘等有机物的利用应引起重视。通过非催化蒸汽重整和催化重整可将这些有机物转化为H2和CO,提高H2含量。ONOZAKI等[81]在2006年提出一种非催化蒸汽重整热焦炉煤气(1 050 K)工艺,该技术可回收粗焦炉煤气中3~5倍的H2和CO,相比分离冷焦炉煤气具有显著优势。蒸汽催化重整更具有吸引力,ROBERTO等[147]研究了催化蒸汽重整法去焦油净化生物质合成气的工艺,对UCI G90-C和ICI 46-12种商用镍基催化剂进行评价,萘是最难进行蒸汽重整的化合物,而随芳香族化合物分子量增加,形成焦炭的倾向随之增大。一般情况下,催化剂温度和S/C比(水蒸气与碳的比值)高于石脑油,以防止催化剂上形成结焦。在MgAl2O4上负载Ni和Ir,合金态比单金属具有更好的抗结焦性和催化稳定性[148]。低成本钢渣也被用于焦油重整,Fe2O3和MgFe2O4使钢渣具有疏松多孔的结构,800 ℃焦油转化率达94.1%,气体产量为493.5 mL/g[149]。气体与催化剂接触时间为80 h时,2.5% Ir和15% Ni的双金属催化剂的活性损失为12%,远低于单金属Ni或Ir的活性损失(超过40%)。
硫物种和S/C对有机物转化具有重要影响。噻吩存在的情况下,Rh/Al2O3具有更佳的苯蒸汽重整活性[75]。新日铁公司探究了纯CeO2在H2S、萘共存的焦炉煤气蒸汽重整中的抗硫性,认为S/C大于2.0时H2S可促进萘蒸汽重整,降低积碳,提升CeO2的稳定性[150]。DOU等[76]考察了H2S和HCl对Ni-Fe催化剂的萘蒸汽重整和水气变换反应的毒害作用,在二者共存情况下萘重整活性的中毒由H2S和表面Ni物种形成NiS引起,不受HCl影响。H2S和HCl均可引起水气变换反应中毒,当H2S和HCl从气体中去除后,水气变换活性可以完全恢复。NiO/CaO@Ca12Al14O33双功能催化剂用于粗焦炉煤气中焦油的吸附增强水气重整反应,具有比单一吸附增强、水气重整更高的H2产率[151]。MgO用于改性NiO/Ca12Al14O33催化剂,在850 ℃、S/C比为12∶1时,产氢率达93.16%,碳转化率达97.14%[72]。
4 结语及展望
1)我国富煤、缺油、少气的化石能源资源结构特点决定了煤的清洁利用在未来若干年中仍将占据主导地位,尽管短流程炼钢、氢冶金等清洁冶炼技术快速发展,但以焦炭为还原剂的高炉炼铁技术仍是主流技术。焦炭生产过程产生的焦炉煤气富含高利用价值H2,然而成分复杂,净化、分离、提纯工艺繁琐,利用难度高。本文介绍了变压吸附技术、膜分离技术、深冷分离技术、非催化与催化重整技术、氧传输膜重整技术以及化学链重整技术的基本原理,分析了不同技术在焦炉煤气制氢中的研究与应用现状以及存在的技术问题,指出了不同技术未来发展方向,并针对焦炉煤气净化及其有机物(如焦油、苯、萘)的转化利用提供解决思路。
2)对于传统的变压吸附技术、膜分离技术和深冷分离技术而言,高效、价廉的吸附剂和分离膜的设计与开发,以及工艺的升级与设备的集约化设计是今后研究重点。对于催化重整技术、氧传输膜重整技术和化学链重整技术而言,具有良好的硫耐受性与反应稳定性的催化剂、氧传输膜材料和载氧体的选择与开发,反应器的设计与放大以及工业化探索是今后发展方向,是提升H2产量的重要途径。加快焦炉煤气化学方法制氢工业化进程,探索化学方法 物理方法联合制氢工艺,是实现焦炉煤气高效制氢、深度利用的关键,是未来重要发展趋势。
3)化学方法 物理方法联合制氢工艺可由净化、重整、分离3个工序组成。净化工序脱除粗焦炉煤气中的焦油、苯、硫化物等杂质组分。重整工序利用催化重整、膜重整和化学链重整等化学方法将焦炉煤气中CH4转化为H2,膜重整和化学链重整还可通过水解离实现两步共产H2,从而有效提高焦炉煤气制氢的H2产量。分离工序利用变压吸附技术、深冷分离技术、膜分离技术等物理方法从重整工序得到的富氢混合气中分离H2。目前,焦炉煤气催化重整耦合变压吸附制氢技术已实现工业化应用,焦炉煤气膜重整、化学链重整耦合物理分离法制氢工艺正在探索中,高效的化学方法 物理方法联合制氢工艺或将成为提升焦炉煤气制氢产量的有效途径。
[1] 张继龙, 李晴, 帖呈,等.焦炉煤气利用的分析与建议[J].煤化工, 2013, 41(3):4-8.
ZHANG Jilong, LI Qing, TIE Cheng, et al.Analysis and suggestion of coke oven gas utilization[J].Coal Chemical Industry, 2013, 41(3):4-8.
[2] ZHANG Y, TIAN Z, CHEN X, et al.Technology-environment-economy assessment of high-quality utilization routes for coke oven gas[J].International Journal of Hydrogen Energy, 2022, 47(1): 666-685.
[3] 陈凌, 张涛, 郭敏,等.利用焦炉煤气生产海绵铁的前景分析[J].钢铁研究, 2013, 41(5):56-59.
CHEN Ling, ZHANG Tao, GUO Min, et al.Prospect analysis for production of sponge iron using coke oven gas[J].Research on Iron and Steel, 2013, 41(5):56-59.
[4] 唐珏, 储满生, 李峰,等.我国氢冶金发展现状及未来趋势[J].河北冶金, 2020(8):1-6,57.
TANG Yu, CHU Mansheng, LI Feng, et al.Development status and future trend of hydrogen metallurgy in China[J].Hebei Metallurgy, 2020(8):1-6,57.
[5] 李子烨, 劳力云, 王谦.制氢技术发展现状及新技术的应用进展[J].现代化工, 2021, 41(7):86-89,94.
LI Ziye, LAO Liyun, WANG Qian.Development of hydrogen production technologies and application of new technologies[J].Modern Chemical Industry, 2021, 41(7):86-89,94.
[6] 田江南, 蒋晶, 罗扬, 等.绿色氢能技术发展现状与趋势[J].分布式能源, 2021, 6(2): 8-13.
TIAN Jiangnan, JIANG Jing, LUO Yang, et al.Development status and trend of green hydrogen energy technology[J].Distributed Energy, 2021, 6(2): 8-13.
[7] 张剑光.氢能产业发展展望:制氢与氢能储运[J].化工设计, 2019,29(4): 3-6,26.
ZHANG Jianguang.Prospect of hydrogen energy industry development:Hydrogen production and hydrogen storage and transportation[J].Chemical Engineering Design, 2019, 29(4): 3-6,26.
[8] 俞红梅, 邵志刚, 侯明,等.电解水制氢技术研究进展与发展建议[J].中国工程科学, 2021, 23(2): 146-152.
YU Hongmei, SHAO Zhigang, HOU Ming, et al.Hydrogenproduction by water electrolysis: Progress and suggestions[J].Strategic Study of CAE, 2021, 23(2): 146-152.
[9] 周云辉, 刘新, 粟莲芳.变压吸附技术在焦炉煤气制氢中的应用[J].河南冶金,2007, 15(5): 35-37.
ZHOU Yunhui, LIU Xin, SU Lianfang.Application of pressure shift absorbing technique in hydrogen generation from COG[J].Henan Metallurgy, 2007, 15(5): 35-37.
[10] 王瑾辉.变压吸附制氢技术在邯钢冷轧工程中的应用[J].冶金动力, 2006(1): 53-56.
WANG Jinhui.Application of PSA hydrogen making technology in cold rolling engineering[J].Metallurgical Power, 2006(1): 53-56.
[11] 孟强, 王利霞, 张彩丽.改造焦炉煤气吸附制氢装置, 提高氢气产量[J].冶金动力, 2007(3): 21-24.
MENG Qiang, WANG Lixia, ZHANG Caili.Technical reconstruction of PSA hydrogen making device of coke oven gas to increase hydrogen output[J].Metallurgical Power, 2007(3): 21-24.
[12] LOPES F V S, GRANDE C A, RODRIGUES A E.Activated carbon for hydrogen purification by pressure swing adsorption: Multicomponent breakthrough curves and PSA performance[J].Chemical Engineering Science, 2011, 66(3): 303-317.
[13] SHAMSUDIN I K, ABDULLAH A, IDRIS I, et al.Hydrogen purification from binary syngas by PSA with pressure equalization using microporous palm kernel shell activated carbon[J].Fuel, 2019, 253: 722-730.
[14] AGUEDA V I, DELGADO J A, UGUINA M A, et al.Adsorption and diffusion of H2, N2, CO, CH4 and CO2 in UTSA-16 metal-organic framework extrudates[J].Chemical Engineering Science, 2015, 124:159-169.
[15] DOBLADEZ J A D, MATÉ V I A, TORRELLAS S A, et al.Efficient recovery of syngas from dry methane reforming product by a dual pressure swing adsorption process[J].International Journal of Hydrogen Energy, 2020, 46(33): 17522-17533.
[16] AUGELLETTI R,CONTI M,ANNESINI M C.Pressure swing adsorption for biogas upgrading:A new process configuration for the separation of biomethane and carbon dioxide[J].Journal of Cleaner Production, 2017, 140: 1390-1398.
[17] SIRCAR S, WALDRON W E, RAO M B, et al.Hydrogen production by hybrid SMR-PSA-SSF membrane system[J].Separation and Purification Technology, 1999, 17(1): 11-20.
[18] LIN Y, LI Y, XU Z, et al.Carbon consumption and adsorption-regeneration of H2S on activated carbon for coke oven flue gas purification[J].Environmental Science and Pollution Research, 2021, 28(43): 60557-60568.
[19] 张敏.焦炉煤气变压吸附制氢在宝钢的应用[J].冶金动力, 2006(6): 23-25.
ZHANG Min.Application of pressure swing adsorption hydrogen making process of coke oven gas[J].Metallurgical Power, 2006(6): 23-25.
[20] 刘飞, 熊源泉.南钢富余焦炉煤气提纯制氢-电力多联产综合利用[J].钢铁研究, 2009, 37(5): 43-45,57.
LIU Fei, XIONG Yuanquan.Comprehensive utilization of surplus coke oven gas to make hydrogen and electric power in Nanjing Iron and Steel Co.Ltd.[J].Research on Iron and Steel, 2009, 37(5): 43-45,57.
[21] 宁红军, 赵新亮, 曹晓宝.焦炉煤气变压吸附制氢新工艺[J].河南化工, 2007(11): 48-50.
NING Hongjun, ZHAO Xinliang, CAO Xiaobao.New process of hydrogen production from coke oven gas by pressure swing adsorption[J].Henan Chemical Industry, 2007(11): 48-50.
[22] GOLMAKANI A, NABAVI S A, MANOVI V.Effect of impurities on ultra-pure hydrogen production by pressure vacuum swing adsorption[J].Journal of Industrial and Engineering Chemistry, 2020, 82: 278-289.
[23] BANG G, MOON D K, KANG J H, et al.High-purity hydrogen production via a water-gas-shift reaction in a palladium-copper catalytic membrane reactor integrated with pressure swing adsorption[J].Chemical Engineering Journal, 2021, 411: 128473-128484.
[24] VAN ACHT S C J , LAYCOCK C, CARR S J W, et al.Simulation of integrated novel PSA/EHP/C process for high-pressure hydrogen recovery fromcoke oven gas[J].International Journal of Hydrogen Energy, 2020, 45(30):15196-15212.
[25] VAN ACHT S C J , LAYCOCK C, CARR S J W, et al.Optimization of VPSA-EHP/C process for high-pressure hydrogen recovery fromcoke oven gas using CO selective adsorbent[J].International Journal of Hydrogen Energy, 2021, 46(1): 709-725.
[26] BREA P, DELGADO J A,  GUEDA V I, et al.Comparison between MOF UTSA-16 and BPL activated carbon in hydrogen purification by PSA[J].Chemical Engineering Journal, 2019, 355: 279-289.
GUEDA V I, et al.Comparison between MOF UTSA-16 and BPL activated carbon in hydrogen purification by PSA[J].Chemical Engineering Journal, 2019, 355: 279-289.
[27] CHOU Chengtung, CHEN Feihong, HUANG Yujie, et al.Carb-on dioxide capture and hydrogen purification from synthesis gas by pressure swing adsorption[J].Chemical Engineering Transactions, 2013, 32: 1855-1860.
[28] DELGADO J A, AGUEDA V I, UGUINA M A, et al.Hydrogen recovery from off-gases with nitrogen-rich impurity by pressure swing adsorption using CaX and 5A zeolites[J].Adsorption, 2015, 21(1): 107-123.
[29] DELGADO J A,  GUEDA V I, UGUINA M A, et al.Adsorption and diffusion of H2, CO, CH4, and CO2 in BPL activated carbon and 13X zeolite: Evaluation of performance in pressure swing adsorption hydrogen purification by simulation[J].Industrial &Engineering Chemistry Research, 2014, 53(40): 15414-15426.
GUEDA V I, UGUINA M A, et al.Adsorption and diffusion of H2, CO, CH4, and CO2 in BPL activated carbon and 13X zeolite: Evaluation of performance in pressure swing adsorption hydrogen purification by simulation[J].Industrial &Engineering Chemistry Research, 2014, 53(40): 15414-15426.
[30] MIVECHIAN A, PAKIZEH M.Hydrogen recovery from Tehran refinery off-gas using pressure swing adsorption, gas absorption and membrane separation technologies: Simulation and economic evaluation[J].Korean Journal of Chemical Engineering, 2013, 30(4): 937-948.
[31] 刘来志, 薛子文.羰基合成工业中分离提纯CO方法[J].化工设计通讯, 2010, 36(4): 46-48,51.
LIU Laizhi, XUE Ziwen.Separation and purification of CO in carbonyl synthesis industry[J].Chemical Engineering Design Communications, 2010, 36(4): 46-48,51.
[32] 李雪峰.天然气制氢研究进展[J].河南化工, 2012, 29(12): 3-4.
LI Xuefeng.Progress in hydrogen production from natural gas[J].Henan Chemical Industry, 2012, 29(12): 3-4.
[33] Y
 EZ M, ORTIZ A, GORRI D, et al.Comparative performa-nce of commercial polymeric membranes in the recovery of industrial hydrogen waste gas streams[J].International Journal of Hydrogen Energy, 2021, 46(33): 17507-17521.
EZ M, ORTIZ A, GORRI D, et al.Comparative performa-nce of commercial polymeric membranes in the recovery of industrial hydrogen waste gas streams[J].International Journal of Hydrogen Energy, 2021, 46(33): 17507-17521.
[34] TANAKA K, KITA H, OKANO M, et al.Permeability and per-mselectivity of gases in fluorinated and non-fluorinated polyimides[J].Polymer, 1992, 33(3): 585-592.
[35] 田文中, 李燕燕, 付娟,等.焦炉煤气膜分离提取高纯H2的方法[J].上海煤气, 2013(4): 8-9,11.
TIAN Wenzhong, LI Yanyan, FU Juan, et al.The methods of seperation and extraction high pure H2 from coke oven gas by member seperation.Shanghai Gas, 2013(4): 8-9,11.
[36] LI H, CARAVELLA A, XU H Y.Recent progress in Pd-based composite membranes[J].Journal of Materials Chemistry A, 2016, 4(37): 14069-14094.
[37] 林定标, 唐春华, 李慧,等.多通道型高效钯复合膜在超高纯氢气提纯的应用[J].低温与特气, 2018, 36(2): 41-47.
LIN Dingbiao,TANG Chunhua,LI Hui,et al.The application of highly efficient multi-channel Pd composite membranes in ultra-pure hydrogen purification[J].Low Temperature and Specialty Gases, 2018, 36(2): 41-47.
[38] 马玉钰, 李慧.钯银合金膜制备研究进展[J].天然气化工(C1化学与化工), 2020, 45(5): 115-120.
MA Yuyu, LI Hui.Recent research progress in preparation of palladium-silver alloy films[J].Natural Gas Chemical Industry, 2020, 45(5): 115-120.
[39] KHAN A L, CANO-ODENA A, GUTIéRREZ B, et al.Hydrogen separation and purification using polysulfone acrylate-zeolite mixed matrix membranes[J].Journal of Membrane Science, 2010, 350(1/2): 340-346.
[40] 张健青.兰炭伴生焦炉煤气膜分离增强制氢分离工艺及经济性分析[J].煤炭技术, 2013,32(9): 220-222.
ZHANG Jianqing.Separation processes and economic analysis of associated semi-coke oven gas membrane separation enhanced hydrogen[J].Coal Technology, 2013,32(9): 220-222.
[41] 王旭俊.甲醇合成驰放气中氢的回收[J].江西化工, 2020(4): 173-174.
WANG Xujun.Recovery of hydrogen from the exhaust gas of methanol synthesis[J].Jiangxi Chemical Industry, 2020(4): 173-174.
[42] 韩坤鹏, 耿新国, 刘铁斌.炼厂低浓度氢气回收利用的技术现状及进展[J].当代化工, 2020, 49(3): 665-669,682.
HAN Kunpeng, GENG Xinguo, LIU Tiebin.Technology status and development of recovering hydrogen from refinery offgas[J].Contemporary Chemical Industry, 2020, 49(3): 665-669,682.
[43] 荀航, 张卫帅.合成气分离技术探讨[J].机械管理开发, 2013(5): 61-63.
XUN Hang, ZHANG Weishuai.Discussion on syngas separation technology[J].Mechanical Management and Development, 2013(5): 61-63.
[44] 王萍, 吴昊鹏, 徐以泉.加氢型炼厂富氢尾气回收氢气技术[J].中外能源, 2016, 21(4): 78-82.
WANG Ping, WU Haopeng, XU Yiquan.Technology of hydrogen recovery from hydrogen-rich offgas in hydrogenation refinery[J].Sino-Global Energy, 2016, 21(4): 78-82.
[45] 杨晓勤, 肖聪, 杨晓华,等.合成氨尾气综合回收副产液化天然气研究与实践[J].小氮肥, 2015, 43(9): 13-15.
YANG Xiaoqin, XIAO Cong, YANG Xiaohua, et al.Research and practice of comprehensive recovery of by-product liquefied natural gas from synthetic ammonia offgas[J].Small Nitrogenous Fertilizer Plant, 2015, 43(9): 13-15.
[46] 闫立志.深冷分离技术装置在煤制烯烃中的优化与发展[J].化工管理, 2017(13): 157.
YAN Lizhi.Optimization and development of cryogenic separation technology device in coal to olefin[J].Chemical Enterprise Management, 2017(13): 157.
[47] 张准.浅谈深冷分离技术在氧气安全生产中的应用[J].中国化工贸易, 2015(14): 226.
ZHANG Zhun.The application of cryogenic separation technology in oxygen safety production[J].China Chemical Trade, 2015(14): 226.
[48] 罗东晓.一种高效利用焦炉煤气的新工艺[J].天然气工业, 2009, 29(12): 94-96.
LUO Dongxiao.A new process for high efficiency utilization of coke oven gas[J].Natural Gas Industry, 2009, 29(12): 94-96.
[49] 杨智锋, 张卫帅, 董跃,等.焦炉煤气作为加氢工艺氢源的综合利用[J].中国石油和化工标准与质量, 2018, 38(5): 104-105.
YANG Zhifeng, ZHANG Weishuai, DONG Yue, et al.Comprehensive utilization of coke oven gas as hydrogen source in hydrogenation process[J].China Petroleum and Chemical Standard and Quality, 2018, 38(5): 104-105.
[50] 赵永刚, 常力鹏.深冷法制氮与PSA法制氮的比较分析[J].民营科技, 2011(12): 28.
ZHAO Yonggang, CHANG Lipeng.Comparative analysis of nitrogen production by cryogenic method and PSA method[J].Private Science and Technology, 2011(12): 28.
[51] 陈顺杭.PSA变压吸附制氮技术与低温法制氮技术比较[J].现代化工, 2013, 33(2): 76-78.
CHEN Shunhang.Comparison of nitrogen producing processes of pressure shift adsorption(PSA)and cryogenic separation[J].Modern Chemical Industry, 2013, 33(2): 76-78.
[52] ATSONIOS K, PANOPOULOS K D, DOUKELIS A, et al.Cryogenic method for H2 and CH4 recovery from a rich CO2 stream in pre-combustion carbon capture and storage schemes[J].Energy, 2013, 53: 106-113.
[53] 李训明, 张长征.焦炉煤气制液化天然气技术探讨[J].化学工程与装备, 2014(8): 68-70.
LI Xunming, ZHANG Changzheng.Study on liquefied natural gas production from coke oven gas[J].Chemical Engineering and Equipment, 2014(8): 68-70.
[54] 朱加宝.焦炉煤气制LNG预处理净化工艺探讨[J].山东化工, 2015, 44(8): 117-119.
ZHU Jiabao.Coke oven gas making of natural gas(LNG)pretreatment and purification process study[J].Shandong Chemical Industry, 2015, 44(8): 117-119.
[55] 周烨, 史元利, 李乃厚,等.焦炉煤气制液化天然气的实践应用[J].山东化工, 2014, 43(1): 146-147.
ZHOU Ye,SHI Yuanli,LI Naihou,et al.The practical application of coke oven gas produce liquefied natural gas[J].Shandong Chemical Industry, 2014, 43(1): 146-147.
[56] ZHU Q H, CHENG H W, ZOU X L, et al.Synthesis, characterization, and catalytic performance of La0.6Sr0.4NixCo1-xO3 perovskite catalysts in dry reforming of coke oven gas[J].Chinese Journal of Catalysis, 2015, 36(7): 915-924.
[57] KIM A R, LEE H Y, CHO J M, et al.Ni/M-Al2O3(M= Sm, Ce or Mg)for combined steam and CO2 reforming of CH4 from coke oven gas[J].Journal of CO2 Utilization, 2017, 21: 211-218.
[58] LEE Y L, KIM B J, PARK H R, et al.Customized Ni-MgO-Al2O3 catalyst for carbon dioxide reforming of coke oven gas: Optimization of preparation method and co-precipitation pH[J].Journal of CO2 Utilization, 2020, 42: 101354-101362.
[59] SHEN S G, CHEN P P, LI A Q, et al.Effect of three processes on CO2 and O2 simultaneously reforming of coke oven gas to syngas[J].Chemical Engineering and Processing: Process Intensification, 2014, 75: 75-80.
[60] TAO W, CHENG H, YAO W, et al.Syngas production by CO2 reforming of coke oven gas over Ni/La2O3-ZrO2 catalysts[J].International Journal of Hydrogen Energy, 2014, 39(32): 18650-18658.
[61] CHENG H W, LI G S, ZHAO H B, et al.Effects of preparation technique and lanthana doping on Ni/La2O3-ZrO2 catalysts for hydrogen production by CO2 reforming of coke oven gas[J].Catalysis Today, 2018, 318: 23-31.
[62] CHENG H W, FENG S H, TAO W, et al.Effects of noble metal-doping on Ni/La2O3-ZrO2 catalysts for dry reforming of coke oven gas[J].International Journal of Hydrogen Energy, 2014, 39(24): 12604-12612.
[63] LI G, CHENG H, ZHAO H, et al.Hydrogen production by CO2 reforming of CH4 in coke oven gas over Ni-Co/MgAl2O4 catalysts[J].Catalysis Today, 2018, 318: 46-51.
[64] JING J Y, YANG Z F, HUO J M, et al.Metal precursor impregnation sequence effect on the structure and performance of NiCo/MgO catalyst[J].International Journal of Hydrogen Energy, 2019, 44(16): 8089-8098.
[65] PARK H R, KIM B J, LEE Y L, et al.CO2 reforming of CH4 using coke oven gas over Ni/MgO-Al2O3 catalysts: Effect of the MgO∶Al2O3 ratio[J].Catalysts, 2021, 11(12): 1468.
[66] TIAN J, LI H, ZENG X, et al.Facile immobilization of Ni nanoparticles into mesoporous MCM-41 channels for efficient methane dry reforming[J].Chinese Journal of Catalysis, 2019, 40(9): 1395-1404.
[67] WANG D, WANG J, LU C, et al.Hydrogen production from coke oven gas by CO2 reforming over a novel Ni-doped Silicalite-1[J].Catalysis Letters, 2018, 148(5): 1424-1434.
[68] ZHANG B, CHEN Y, KANG B, et al.Hydrogen production via steam reforming of coke oven gas enhanced by steel slag-derived CaO[J].International Journal of Hydrogen Energy, 2020, 45(24): 13231-13244.
[69] WANG X, WANG T.Hydrogen amplification from coke oven gas using a CO2 adsorption enhanced hydrogen amplification reactor[J].International Journal of Hydrogen Energy, 2012, 37(6): 4974-4986.
[70] 申曙光, 李安琪, 陈攀攀,等.焦炉煤气三重整制合成气的工艺比较及催化剂改性[J].现代化工, 2013(5): 61-65.
SHEN Shuguang, LI Anqi, CHEN Panpan, et al.Comparison of processes on tri-reforming of coke oven gas to syngas and catalysts modification[J].Modern Chemical Industry, 2013(5): 61-65.
[71] ZHANG B, CHEN Y, ZHANG B, et al.Cyclic performance of coke oven gas-steam reforming with assistance of steel slag derivates for high purity hydrogen production[J].Renewable Energy, 2022, 184: 592-603.
[72] XIE H, YU Q, ZHANG J, et al.Preparation and performance of Ni-based catalysts supported on Ca12Al14O33 for steam reforming of tar in coke oven gas[J].Environmental Progress and Sustainable Energy, 2017, 36(3): 729-735.
[73] WU X, WU R, WU S.Kinetic study of reactive sorption-enhanced reforming of coke oven gas for hydrogen production[J].Journal of Natural Gas Science and Engineering, 2015, 27: 1432-1437.
[74] XIE H, YU Q, ZHANG Y, et al.New process for hydrogen production from raw coke oven gas via sorption-enhanced steam reforming: Thermodynamic analysis[J].International Journal of Hydrogen Energy, 2017, 42(5): 2914-2923.
[75] HERNANDEZ A D, KAISALO N, SIMELL P, et al.Effect of H2S and thiophene on the steam reforming activity of nickel and rhodium catalysts in a simulated coke oven gas stream[J].Applied Catalysis B: Environmental, 2019, 258: 117977-117987.
[76] DOU X, VEKSHA A, CHAN W P, et al.Poisoning effects of H2S and HCl on the naphthalene steam reforming and water-gas shift activities of Ni and Fe catalysts[J].Fuel, 2019, 241: 1008-1018.
[77] CHEN Y, PENG R, XIAO Y, et al.Efficient hydrogen production from coke oven gas by sorption-enhanced steam reforming in a membrane-assisted fluidized bed reactor[J].Energy &Fuels, 2019, 33(11): 11420-11438.
[78] CHEN Y, ZHANG B, PENG R, et al.Comprehensive modeling of sorption-enhanced steam reforming of coke oven gas in a fluidized bed membrane reactor[J].Energy &Fuels, 2020, 34(3): 3065-3086.
[79] 付威, 李谦, 鲍正洪,等.铝含量对焦炉煤气制氢用Cu/ZnO/Al2O3催化剂前驱体协同效应的影响[J].上海金属, 2010, 32(5): 50-54.
FU Wei, LI Qian, BAO Zhenghong, et al.Influence of Al on the synergistic effect of precursors in the Cu/ZnO/Al2O catalysts[J].Shanghai Metals, 2010, 32(5): 50-54.
[80] ANGELI S D, GOSSLER S, LICHTENBERG S, et al.Reduction of CO2 emission from off-gases of steel industry by dry reforming of methane[J].Angewandte Chemie, 2021, 60(21): 11852-11857.
[81] ONOZAKI M, WATANABE K, HASHIMOTO T, et al.Hydrogen production by the partial oxidation and steam reforming of tar from hot coke oven gas[J].Fuel, 2006, 85(2): 143-149.
[82] NORINAGA K, YATABE H, MATSUOKA M, et al.Application of anexisting detailed chemical kinetic model to a practical system of hot coke oven gas reforming by noncatalytic partial oxidation[J].Industrial &Engineering Chemistry Research, 2010, 49(21):10565-10571.
[83] ZHANG Y, LIU J, DING W, et al.Performance of an oxygen-permeable membrane reactor for partial oxidation of methane in coke oven gas to syngas[J].Fuel, 2011, 90(1): 324-330.
[84] YANG Z, DING W, ZHANG Y, et al.Catalytic partial oxidation of coke oven gas to syngas in an oxygen permeation membrane reactor combined with NiO/MgO catalyst[J].International Journal of Hydrogen Energy, 2010, 35(12): 6239-6247.
[85] LIU J, CHENG H, JIANG B, et al.Effects of tantalum content on the structure stability and oxygen permeability of BaCo0.7Fe0.3-xTaxO3-δ ceramic membrane[J].International Journal of Hydrogen Energy, 2013, 38(25): 11090-11096.
[86] CHENG H, YAO W, LU X, et al.Structural stability and oxygen permeability of BaCo0.7Fe0.2M0.1O3-δ(M=Ta, Nb, Zr)ceramic membranes for producing hydrogen from coke oven gas[J].Fuel Processing Technology, 2015, 131: 36-44.
[87] XU X, CHENG H, LIU Y, et al.Oxygen permeability and stability of dual-phase Ce0.85Pr0.15O2-δ-Pr0.6Sr0.4Fe0.9Al0.1O3-δ membrane for hydrogen production by water splitting[J].International Journal of Hydrogen Energy, 2021, 46(54): 27307-27318.
[88] ZHU X, SHI C, LI K, et al.Water splitting for hydrogen generation over lanthanum-calcium-iron perovskite-type membrane driven by reducing atmosphere[J].International Journal of Hydrogen Energy, 2017, 42(31): 19776-19787.
[89] ZHU X, YANG W.Microstructural andinterfacial designs of oxygen-permeable membranes for oxygen separation and reaction-separation coupling[J].Advanced Materials, 2019, 31(50): 1902547-1902568.
[90] YANG Z, ZHANG Y, WANG X, et al.Design of two-stage membrane reactor for the conversion of coke-oven gas to H2 and CO[J].Journal of Energy Chemistry, 2014, 23(4): 411-413.
[91] YANG Z, ZHANG Y, DING W.Investigation on the reforming reactions of coke-oven-gas to H2 and CO in oxygen-permeable membrane reactor[J].Journal of Membrane Science, 2014, 470: 197-204.
[92] ZHANG Y, SU K, ZENG F, et al.A novel tubular oxygen-permeable membrane reactor for partial oxidation of CH4 in coke oven gas to syngas[J].International Journal of Hydrogen Energy, 2013, 38(21): 8783-8789.
[93] 秦国利, 丁伟中, 张玉文,等.SrFeCo0.5O3-δ透氧膜用于焦炉煤气甲烷部分氧化重整的可行性研究[J].上海金属, 2009, 31(1): 51-55.
QIN Guoli, DING Weizhong, ZHANG Yuwen, et al.Feasibilitystudy of SrFeCo0.5O3-δ oxygen permeable membrane on partial oxygen reforming og COG[J].Shanghai Metals, 2009, 31(1): 51-55.
[94] ZHANG C, SUNARSO J, LIU S M.Designing CO2-resistant oxygen-selective mixed ionic-electronic conducting membranes: Guidelines, recent advances, and forward directions[J].The Royal Society of Chemistry, 2017, 46(10): 2941-3005.
[95] SONG S D, ZHANG P, HAN M F, et al.Oxygen permeation and partial oxidation of methane reaction in Ba0.9Co0.7Fe0.2Nb0.1O3-δ oxygen permeation membrane[J].Journal of Membrane Science, 2012, 415-416: 654-662.
[96] SONG S D, ZHANG P, ZHANG X, et al.Partial oxidation of methane reaction in Ba0.9Co0.7Fe0.2Nb0.1O3-δ oxygen permeation membrane with three-layer structure[J].International Journal of Hydrogen Energy, 2015, 40(34): 10894-10901.
[97] ZHANG R D, ALAMDARI H, KALIAGUINE S.SO2 poisoning of LaFe0.8Cu0.2O3 perovskite prepared by reactive grinding during NO reduction by C3H6[J].Applied Catalysis A: General, 2008, 340(1): 140-151.
[98] MENG B, WU S, ZHANG S D, et al.CO2-stable and cobalt-free Ce0.8Sm0.2O2-δ-La0.8Ca0.2Al0.3Fe0.7O3-δ dual-phase hollow fiber membranes for oxygen separation[J].Separation and Purification Technology, 2022, 300: 121900-121910.
[99] LUO L F, CHENG H W, LI G S, et al.Oxygen permeability and CO2-tolerance of Ce0.8Gd0.2O2-δ-LnBaCo2O5 δ dual-phase membranes[J].Journal of Energy Chemistry, 2015, 24(1): 15-22.
[100] CHENG H W, ZHANG N J, XIONG X L, et al.Synthesis,oxygen permeation, and CO2-tolerance properties of Ce0.8Gd0.2O2-δ-Ba0.95La0.05Fe1-xNbxO3-δ dual-phase membranes[J].ACS Sustainable Chemistry &Engineering, 2015, 3(9): 1982-1992.
[101] PIROU S, GARCíA-FAYOS J, BALAGUER M, et al.Improving the performance of oxygen transport membranes in simulated oxy-fuel power plant conditions by catalytic surface enhancement[J].Journal of Membrane Science, 2019, 580: 307-315.
[102] EMHJELLEN L K, XING W, LI Z A, et al.Oxygen permeability and surface kinetics of composite oxygen transport membranes based on stabilized δ-Bi2O3[J].Journal of Membrane Science, 2022, 660: 120875-120880
[103] CHEN G X, LIU W M, WIDENMEYER M, et al.High flux and CO2-resistance of La0.6Ca0.4Co1-xFexO3-δ oxygen-transporting membranes[J].Journal of Membrane Science, 2019, 590: 117082-117091.
[104] CHEN G X, TANG B J, WIDENMEYER M, et al.Novel CO2-tolerant dual-phase Ce0.9Pr0.1O2-δ-La0.5Sr0.5Fe0.9Cu0.1O3-δ membranes with high oxygen permeability[J].Journal of Membrane Science, 2020, 595: 117530-117538.
[105] CHEN G, ZHAO Z J, WIDENMEYER M, et al.A comprehensive comparative study of CO2-resistance and oxygen permeability of 60 wt% Ce0.8M0.2O2-(M = La, Pr, Nd, Sm, Gd)-40 wt% La0.5Sr0.5Fe0.8Cu0.2O3-δ dual-phase membranes[J].Journal of Membrane Science, 2021, 639: 119783-119794.
[106] BERMUDEZ J M, GARCIA-FAYOS J, REINA T R, et al.Thermochemical stability of LaxSr1-xCoyFe1-yO3-δ and NiFe2O4-Ce0.8Tb0.2O2-δ under real conditions for its application in oxygen transport membranes for oxyfuel combustion[J].Journal of Membrane Science, 2018, 562: 26-37.
[107] JIANG H Q, CAO Z W, SCHIRRMEISTER S, et al.A coupling strategy to produce hydrogen and ethylene in a membrane reactor[J].Angewandte Chemie, 2010, 49(33): 5656-5660.
[108] JIA L J, HE G H, ZHANG Y, et al.Hydrogen purification through a highly stable dual-phase oxygen-permeable membrane[J].Angewandte Chemie, 2021, 60(10): 5204-5208.
[109] LI D Y, XU R D, LI X Y, et al.Chemicallooping conversion of gaseous and liquid fuels for chemical production: A review[J].Energy &Fuels, 2020, 34: 5381-5413.
[110] YANG K, GU Z H, LONG Y H, et al.Hydrogen production via chemical looping reforming of coke oven gas[J].Green Energy &Environment, 2021, 6(5): 678-692.
[111] LONG Y H, YANG K, GU Z H, et al.Hydrogen generation from water splitting over polyfunctional perovskite oxygen carriers by using coke oven gas as reducing agent[J].Applied Catalysis B: Environmental, 2022, 301: 120778-120791.
[112] XIANG D, ZHOU Y.Concept design and techno-economic performance of hydrogen and ammonia co-generation by coke-oven gas-pressure swing adsorption integrated with chemical looping hydrogen process[J].Applied Energy, 2018, 229: 1024-1034.
[113] XIANG D, LIU S, XIANG J J, et al.A novel path toward methanol and olefins production fueled by syngas via a coupling of coke-oven gas reforming with pulverized coke chemical looping combustion[J].Energy Conversion and Management, 2017, 152: 239-249.
[114] XIANG D, ZHAO S.Parameter optimization and thermodynamic analysis of COG direct chemical looping hydrogen processes[J].Energy Conversion and Management, 2018, 172: 1-8.
[115] XIANG D, HUANG W Q, HUANG P.A novel coke-oven gas-to-natural gas and hydrogen process by integrating chemical looping hydrogen with methanation[J].Energy, 2018, 165: 1024-1033.
[116] ZHAO Y X, ZHAO Y J, YI Q, et al.Highly flexible and energy-efficient process for converting coke-oven gas and pulverized coke into methanol and ammonia using chemical looping technology[J].Energy Conversion and Management, 2021, 248: 114796-114810.
[117] LI D Y, XU R D, GU Z H, et al.Chemical-looping conversion of methane:A review[J].Energy Technology, 2019, 8(8): 1900925-1900952.
[118] HE F, ZHAO K, HUANG Z, et al.Synthesis of three-dimensionally ordered macroporous LaFeO3 perovskites and their performance for chemical-looping reforming of methane[J].Chinese Journal of Catalysis, 2013, 34(6): 1242-1249.
[119] HE F, LI X A, ZHAO K, et al.The use of La1-xSrxFeO3 perovskite-type oxides as oxygen carriers in chemical-looping reforming of methane[J].Fuel, 2013, 108: 465-473.
[120] NEAL L M, SHAFIEFARHOOD A, LI F.Dynamic methane partial oxidation using a Fe2O3@La0.8Sr0.2FeO3-δ core-shell redox catalyst in the absence of gaseous oxygen[J].ACS Catalysis, 2014, 4(10): 3560-3569.
[121] SHAFIEFARHOOD A, GALINSKY N, HUANG Y, et al.Fe2O3@LaxSr1-xFeO3 core-shell redox catalyst for methane partial oxidation[J].ChemCatChem, 2014, 6(3): 790-799.
[122] ZENG D W, QIU Y, LI M, et al.Ternarymixed spinel oxides as oxygen carriers for chemical looping hydrogen production operating at 550 degrees C[J].ACS Applied Materials &Interfaces, 2019, 11(47): 44223-44232.
[123] LI K Z, HANEDA M, GU Z H, et al.Modification of CeO2 on the redox property of Fe2O3[J].Materials Letters, 2013, 93: 129-132.
[124] LI K Z, HANEDA M, NING P H, et al.Microstructure and oxygen evolution of Fe-Ce mixed oxides by redox treatment[J].Applied Surface Science, 2014, 289: 378-383.
[125] LI K Z, HANEDA M, OZAWA M.Oxygen release-absorption properties and structural stability of Ce0.8Fe0.2O2-x[J].Journal of Materials Science, 2013, 48(17): 5733-5743.
[126] ZHU X, ZHANG M Y, LI K Z, et al.Chemical-looping water splitting over ceria-modified iron oxide: Performance evolution and element migration during redox cycling[J].Chemical Engineering Science, 2018, 179: 92-103.
[127] MOCHIZUKI Y, OGAWA A, TSUBOUCHI N.Removal ofhydrogen sulfide and ammonia by goethite-rich limonite in the coexistence of coke oven gas components[J].ISIJ International, 2017, 57(3): 435-442.
[128] MOCHIZUKI Y, TSUBOUCHI N.Removal of hydrogen sulfide in simulated coke oven gas with low-grade iron ore[J].Energy &Fuels, 2017, 31(8): 8087-8094.
[129] DOU J X, ZHAO Y Q, TAHMASEBI A, et al.Sulfidation and regeneration of iron-based sorbents supported on activated-chars prepared by pressurized impregnation for coke oven gas desulfurization[J].Korean Journal of Chemical Engineering, 2016, 33(10): 2849-2857.
[130] FENG Y, DOU J X, TAHMASEBI A, et al.Regeneration of Fe-Zn-Cusorbents supported on activated lignite char for the desulfurization of coke oven gas[J].Energy &Fuels, 2015, 29(11): 7124-7134.
[131] DOU J X, TAHMASEBI A, LI X C, et al.Char-supported Fe-Zn-Cu sorbent prepared by ultrasonic-assisted impregnation for simultaneous removal of H2S and COS from coke oven gas[J].Environmental Progress &Sustainable Energy, 2016, 35(2): 352-358.
[132] DOU J X, LI X C, TAHMASEBI A, et al.Desulfurization of coke oven gas using char-supported Fe-Zn-Mo catalysts: Mechanisms and thermodynamics[J].Korean Journal of Chemical Engineering, 2015, 32(11): 2227-2235.
[133] 汪佩华, 秦志峰, 吴琼笑,等.磷添加方式对NiMo/Al2O3催化剂加氢脱硫性能的影响[J].化工进展, 2021, 40(2): 890-900.
WANG Peihua, QIN Zhifeng, WU Qiongxiao, et al.Effect of phosphorus adding manners on the performance of NiMo/Al2O3 catalyst in hydrodesulfurization[J].Chemical Industry and Enginnering Progress, 2021, 40(2): 890-900.
[134] KAMP E, THIELERT H, VON MORSTEIN O, et al.Investigation on the simultaneous removal of COS, CS2 and O2 from coke oven gas by hydrogenation on a Pd/Al2O3 catalyst[J].Catalysis Science &Technology, 2020, 10(9): 2961-2969.
[135] HAN F, GAO Y C, HUO Q H, et al.Characteristics of vanadium-based coal gasification slag and the NH3-selective catalytic reduction of NO[J].Catalysts, 2018, 8(8): 327-342.
[136] MENG Z H, WANG C Y, WANG X R, et al.Efficient and stable catalyst of alpha-FeOOH for NO oxidation from coke oven flue gas by the catalytic decomposition of gaseous H2O2[J].RSC advances, 2020, 10(14): 8207-8211.
[137] XU Z C, LI Y R, SHI H M, et al.Application prospect of K used for catalytic removal of NOx, COx, and VOCs from industrial flue gas: A review[J].Catalysts, 2021, 11(4): 419-460.
[138] REN L, CHENG Y H, SHAO R, et al.DFT studies of adsorption properties and bond strengths of H2S, HCN and NH3 on Fe(100)[J].Applied Surface Science, 2020, 500: 144232-144245.
[139] WEI F J, GUO X Q, LIAO J J, et al.Ultra-deep removal of thiophene in coke oven gas over Y zeolite: Effect of acid modification on adsorption desulfurization[J].Fuel Processing Technology, 2021, 213: 106632-106641.
[140] ZOU H K, SHENG M P, SUN X F, et al.Removal of hydrogen sulfide from coke oven gas by catalytic oxidative absorption in a rotating packed bed[J].Fuel, 2017, 204: 47-53.
[141] 周昊, 陈建中, 周明熙,等.钠法与钙法焦炉烟气旋转喷雾脱硫特性对比[J].动力工程学报, 2017, 37(10): 848-854.
ZHOU Hao, CHEN Jianzhong, ZHOU Mingxi, et al.Characteristic study on calcium and sodium based spray-dry desulfurization of coke oven gas[J].Journal of Chinese Society Power Engineering, 2017, 37(10): 848-854.
[142] PARK J, LEE S Y, KIM J, et al.Energy, safety, and absorption efficiency evaluation of a pilot-scale H2S abatement process using MDEA solution in a coke-oven gas[J].Journal of Environmental Chemical Engineering, 2021,9(1):105037-105050.
[143] TIAN X F, WANG L M, ZHANG P, et al.A high efficient absorbent for the separation of H2S from low partial pressure coke oven gas[J].Environmental Science and Pollution Research, 2021, 28(5): 5822-5832.
[144] 汤志刚, 康春清, 刘敬学, 等.焦炉烟道气双氨法一体化脱硫脱硝:从实验室到工业实验[J].化工学报, 2017, 68(2): 496-508.
TANG Zhigang, KANG Chunqing, LIU Jingxue, et al.Desulfurization and denitration integrative process for coke oven flue gas using dual ammonia solution: From laboratory to industrial test[J].CIESC Journal, 2017, 68(2): 496-508.
[145] ZHANG J J, DONG P X, LI C Y, et al.Removal of tar from coke oven flue gas by emulsion liquid membrane[C]//IOP Conference Series: Earth and Environmental Science.Malaysia:Institute of Physics(IOP),2019.
[146] 李飞, 谷小虎, 王旭峰,等.新型络合铁催化剂在焦炉煤气净化中的研究[J].现代化工, 2021, 41(7): 225-227.
LI Fei, GU Xiaohu, WANG Xufeng, et al.Application of new complex iron catalyst in coke oven gas purification[J].Modern Chemical Industry, 2021, 41(7): 225-227.
[147] ROBERTO COLL, JOAN SALVADO, XAVIER FARRIOL, et al.Steam reforming model compounds of biomass gasification tars:Conversion at different operating conditions and tendency towards coke formation[J].Fuel Processing Technology, 2001, 74(1): 19-31.
[148] DAGLE V L, DAGLE R, KOVARIK L, et al.Steam reforming of hydrocarbons from biomass-derived syngas over MgAl2O4-supported transition metals and bimetallic IrNi catalysts[J].Applied Catalysis B: Environmental, 2016, 184: 142-152.
[149] GUO F Q, LIANG S, ZHAO X M, et al.Catalytic reforming of biomass pyrolysis tar using the low-cost steel slag as catalyst[J].Energy, 2019, 189: 116161-116168.
[150] TAIRA K, NAKAO K, SUZUKI K.Steam reforming of 1-methylnaphthalene over pure CeO2 under model coke oven gas conditions containing high H2S concentrations[J].International Journal of Hydrogen Energy, 2020, 45(58): 33248-33259.
[151] ZHANG W D, XIE H Q, YU Z Y, et al.Steam reforming of tar from raw coke oven gas over bifunctional catalysts: Reforming performance for H2 production[J].Environmental Progress &Sustainable Energy, 2020, 40(2): 13501-13511.
Research progress on hydrogen production technology from coke oven gas

LI Zhiqiang,WANG Hua,LI Kongzhai.Research progress on hydrogen production technology from coke oven gas[J].Clean Coal Technology,2023,29(4):31-48.