粉煤灰矿化CO2研究进展
0 引 言
持续的化石燃料燃烧正以前所未有的速度增加大气中CO2浓度[1],从而导致包括全球变暖、气候异常和海洋酸化在内的生态危机[2]。这将对人类食物、水及能源的供应造成毁灭性影响。为应对大气中CO2浓度升高,包括中国在内的许多国家开始制定和实施碳中和政策[3]。而对大气中CO2进行捕集、利用和封存(CCUS)则是实现碳中和的关键技术。近年来,尽管在政策的大力支持下,我国CCUS技术蓬勃发展,但与国外相比,其在项目数量、关键技术和工艺规模上仍有较大差距[4]。CO2封存是CCUS技术中的一项核心内容。探索大规模、低成本的CO2封存技术是亟待破解的技术难题[5]。目前CO2封存技术主要有地质封存、海洋封存和矿化封存[6]。海洋封存是将CO2通过轮船和管道运输至深海海底进行封存。然而,现阶段海洋封存成本极高,且存在泄漏风险,还有可能危害海洋生态环境。地质封存是将CO2注入地质结构(如油田、气田和咸水层等)中,虽然地质封存CO2潜力巨大,但仍存在CO2泄漏、地层变形和诱发地震等风险[7]。矿化封存因其泄漏风险低和封存安全高效等特点受到关注。
矿化封存CO2概念由SEIFRITZ于1990年率先提出[8],主要是模仿自然界中岩石风化并吸收CO2的过程,利用CO2气体同矿化原料发生矿化反应,生成稳定的固态碳酸盐从而实现CO2封存。通常,天然存在的钙镁硅酸盐矿物(如橄榄石、蛇纹石等)均可用作矿化封存的原料。虽然天然矿物来源广泛且储量大,但其开采范围通常固定,运输成本高。此外,矿化前通常需对天然矿物进行切割粉碎等预处理,也会增加额外封存成本和能耗。为此有学者采用工业固废代替传统天然矿物进行CO2矿化封存。
“十四五”期间,燃煤发电行业向着更节能、低碳和绿色高效的方向发展。受环保政策影响,产生的粉煤灰面临巨大处理难题。粉煤灰作为燃煤发电行业最大宗工业固废,含有的CaO和MgO等碱性金属氧化物反应活性较高,CO2矿化潜力大。与天然矿物相比,粉煤灰便于获得、矿化前无需进行高成本和高能耗加工和预处理,使粉煤灰在矿化原料选择上更具竞争优势[9]。此外,粉煤灰矿化封存CO2还可实现粉煤灰主要来源和CO2排放源(火力发电厂)一体化,极大降低运输和管理成本[10-13]。
利用粉煤灰矿化封存CO2在降低与粉煤灰堆积或处理相关环境风险的同时,还能为我国双碳目标的实现做出巨大贡献。迄今为止,关于粉煤灰矿化CO2方面的应用基础研究已经较为成熟。笔者介绍了粉煤灰矿化CO2的研究进展,重点综述利用粉煤灰矿化CO2的直接矿化和间接矿化两大工艺。
1 我国粉煤灰排放及利用现状
粉煤灰是煤燃烧时烟气中所捕获的细灰,是煤燃烧产生的主要固废之一。全球粉煤灰年产量60亿~80亿t,其中中国粉煤灰产量约占全球总量的10%[14]。虽然太阳能、风能等可再生能源的应用可减少粉煤灰排放,但这些可再生能源在能源系统中占比很少。火力发电仍是世界主要发电类型,占发电总量的60%以上。这也意味着粉煤灰排放量预计在短期内不会发生重大变化。中国作为最大煤炭生产国和消费国,火力发电占总发电量的71.13%,产生大量粉煤灰。2015—2023年中国粉煤灰产量及综合利用情况如图1所示,我国粉煤灰排放量由2015年的5.6亿t增至2023年的8.65亿t,粉煤灰已成为中国最大的固体污染源[16-18]。

图1 2015—2023年中国粉煤灰产量及综合利用情况[15]
Fig.1 Coal fly ash production and comprehensive utilization in China in 2015—2023[15]
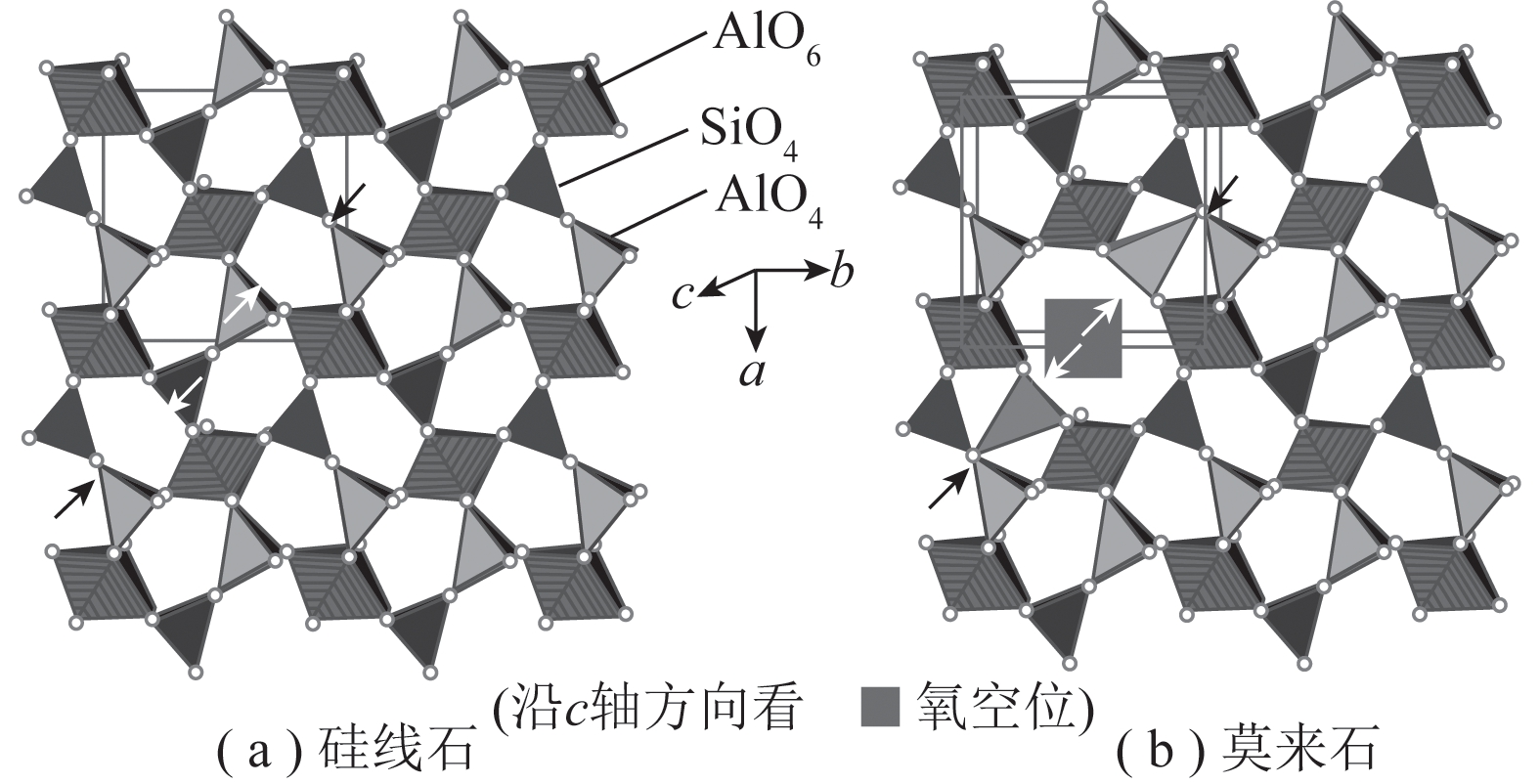
根据煤燃烧方式不同,粉煤灰可以分为煤粉炉(PC)粉煤灰和循环流化床(CFB)粉煤灰(表1)。在化学组成上,粉煤灰主要成分为SiO2、Al2O3、Fe2O3、CaO和MgO,此外还包含一些重金属如Pb、Cd和Hg等。主要矿物相为莫来石(Al6Si2O13)、石英(SiO2)、磁铁矿(Fe3O4)、石灰(CaO)和钙矾石(3CaO·Al2O3·3CaSO4·32H2O)等[19]。不同种类粉煤灰其组分含量也不同(表1)。目前,粉煤灰矿化CO2的研究主要集中在利用粉煤灰中含有的Ca(OH)2和CaO活性组分来矿化CO2[21-22]。文献[22-25]中报道的CO2矿化容量在7.66~264 kg/t(以粉煤灰计,下同)。不同种类的粉煤灰中参与矿化反应的碱金属氧化物含量有所不同。这也是粉煤灰CO2矿化容量存在差异的一个重要原因。
表1 中国主要电厂粉煤灰的化学组成[20]
Table 1 Chemical composition ofcoal fly ash from major power plants in China[20]

近年来,国家对环境保护和工业固废回收利用愈发重视,粉煤灰大量用于建材、农业和交通等领域。截至2023年我国粉煤灰综合利用量约6.96亿t,综合利用效率约80%。虽然我国粉煤灰综合利用效率由1994年的35%达到2023年的80%,但仍低于发达国家平均水平,如欧盟90%,日本98%等[26]。
各主要国家及地区粉煤灰综合利用途径如图2所示,我国粉煤灰利用方式主要集中在建筑领域,如水泥生产、建材生产和筑路填料等[28],在筑路回填和农林方面应用较少[29]。目前,传统建材方面粉煤灰需求量减少,而我国粉煤灰产出量巨大,导致短期内我国粉煤灰综合利用效率无法显著缓解。此外,粉煤灰本身含有钙镁氧化物,使掺入粉煤灰的建筑产品逐渐从空气中吸收水分从而膨胀,导致材料强度下降,使用寿命缩短。且未经处理的粉煤灰应用于建筑和农业等领域时,随时间迁移,其含有的Pb、Cd等有毒重金属从粉煤灰中浸出,易被农作物吸收或污染地下水,危害人体健康。随着研究深入,开发了越来越多粉煤灰高附加值利用工艺,如制备分子筛[30-31]、充当催化剂[32-33]和用作重金属吸附剂[34-35]等。然而,目前这些工艺尚不完善,大部分仍处于实验室研究阶段,未达到产业化应用水平[36]。

图2 各主要国家及地区粉煤灰综合利用途径[27]
Fig.2 Comprehensive utilization of coal fly ash in major countries and regions[27]
作为粉煤灰利用一个新探索方向,CO2矿化不仅有望解决粉煤灰利用难题,还能缓解CO2排放带来的环境压力。CO2矿化后粉煤灰性能更稳定,有利于扩大其在建筑材料生产等领域的应用[37]。
2 直接矿化法
CO2直接矿化是将CO2注入保持在一定温度和压力的反应器中,矿化原料直接与CO2反应。此外,为提高矿化效率,还会对原料进行预处理,但并不涉及使用溶剂从粉煤灰中提取活性反应成分 (如Ca2 或Mg2 )。
直接矿化具有工艺简单、操作方便和化学试剂消耗少等诸多优点。根据是否在反应器中掺入水分分为干法和湿法2种。
2.1 直接气固矿化(干法)
直接气固矿化是气态CO2与粉煤灰中的反应物在适当温度和压力下发生的反应,具有工艺简单和化学试剂消耗少等优点,具有良好的CO2封存前景[38]。在此过程中,主要发生如下化学反应:
CaO CO2![]() CaCO3 179 kJ/mol,
CaCO3 179 kJ/mol,
(1)
MgO CO2![]() MgCO3 118 kJ/mol,
MgCO3 118 kJ/mol,
(2)
CaSiO3 CO2![]() CaCO3 SiO2 90 kJ/mol,
CaCO3 SiO2 90 kJ/mol,
(3)
Mg2SiO4 2CO2![]() 2MgCO3 SiO2 89 kJ/mol。
2MgCO3 SiO2 89 kJ/mol。
(4)
为提升直接气固矿化的矿化效率,反应过程通常需要高温高压环境,其产生的高温蒸汽可用于发电以降低能耗成本[13]。然而,矿化反应总体是放热反应,随温度升高,平衡向逆方向偏移,导致矿化反应存在转化率上限。除粉煤灰本身组成影响CO2矿化外,操作条件也是重要影响因素。
2.1.1 温度影响
REVATHY等[39]通过响应面方法(RSM)研究操作因素对粉煤灰直接矿化CO2的影响。表明温度对粉煤灰矿化能力的影响更显著,但未从影响机理方面给出解释。
LIU等[25]利用粉煤灰进行CO2直接矿化,发现温度对粉煤灰矿化能力影响更显著。不同温度下的热重分析(TGA)结果如图3(a)所示,粉煤灰矿化效率(ξ)随温度升高而提高。CO2矿化反应是放热反应,持续升温并不能使矿化效益最大化。另外,反应温度升高带来额外能耗,增加矿化成本。微分热重分析(DTG)结果显示(图3(b)):粉煤灰直接气固矿化涉及2个阶段:化学反应控制阶段和扩散控制阶段。化学反应控制阶段在最初几分钟内,剧烈且迅速。扩散控制阶段反应缓慢,是由于粉煤灰表面形成致密的碳酸盐产物层,阻碍CO2扩散,使CO2难以与未反应碱性物质接触反应[40-41]。

图3 利用热重分析(TGA)和固定床(FB)探究不同温度对粉煤灰的气固矿化的影响[25]
Fig.3 Effect of different temperatures on gas-solidification mineralization of fly ash using thermogravimetric analysis (TGA) and fixed bed (FB)[25]
2.1.2 CO2浓度影响
此外,CO2矿化效果受CO2浓度影响,但远不及温度影响显著[25,39]。LIU等[25]利用固定床研究不同CO2体积分数(5%、10%、15%、20%和100%)下CFB粉煤灰气固矿化CO2过程,发现随CO2浓度增加,矿化反应的化学平衡正向移动,粉煤灰矿化性能得到改善。在扩散控制阶段,由于形成致密的碳酸盐保护层,扩散阻力不断增加(图4)。CO2体积分数为20% 时,粉煤灰1 h内CO2矿化效率最大为7.33%,CO2体积分数为100%时,封存效率最大为8.06%。CO2浓度增加对矿化反应性能提升没有显著影响。

图4 粉煤灰在530 ℃下不同体积分数CO2固定床中的气固矿化[25]
Fig.4 Gas-solid carbonation in fixed beds with different CO2 volume fractions at 530 ℃[25]
为进一步强化CO2扩散过程,突破气固矿化效率瓶颈,YUAN[42]等利用粉煤灰在超临界CO2环境下进行气固矿化。测量块状CaO扩散深度的试验过程如图5(a)所示,使用块状CaO进行气固矿化试验。试验完成后,切割块状 CaO 露出其内表面,使用扫描电子显微镜扫描 CaO 横截面,以测量其扩散深度。CaO方块上的扩散深度试验结果表明:非超临界最大扩散深度为112.5 μm(图5(b)),而超临界最大扩散深度为142.8 μm(图5(c))。超临界CO2扩散深度是非超临界CO2扩散深度的1.27倍,这直观表明了超临界CO2的强扩散特性。

图5 超临界CO2气固矿化试验[42]
Fig.5 Supercritical CO2 gas-solid mineralization experiment[42]
与非超临界CO2相比,超临界CO2下粉煤灰的CO2矿化容量由42.3 kg/t提高至54.9 kg/t,提升近30%。
具有高扩散系数和低表面张力特性的超临界CO2有希望改善CO2在产物层扩散的限制,并且提高气固矿化效率。然而,在工业化实际应用时,往往采取高温环境而不是高压环境。相比于高压操作条件,高温条件不仅操作方便,对设备要求也比较宽松。
工业燃煤电厂排放的烟气通过其燃烧排放的粉煤灰直接矿化封存具有更高的实用性和经济效益[39,43]。相比实验室使用纯CO2气体而言,应关注电厂燃煤烟气中CO2外如SO2等其他气体对粉煤灰直接矿化过程的影响。
2.2 直接气液矿化(湿法)
直接气液矿化是指原料(粉煤灰)在含水或盐水悬浮液中与CO2反应[13]。与直接气固矿化不同的是,直接气液矿化反应涉及气固液三相,CO2溶于水形成碳酸,粉煤灰中的反应组分在弱酸环境中逐渐溶解,与![]() 发生沉淀反应,形成固体碳酸盐实现CO2矿化。
发生沉淀反应,形成固体碳酸盐实现CO2矿化。
2.2.1 温度影响
REVATHY等[39]利用粉煤灰直接气液矿化CO2,研究了温度、压力和液固比对粉煤灰矿化能力的影响。研究发现,温度影响最显著,其次为液固比,然后是CO2压力。 等[21]也得到类似结果,表明温度在矿化过程中的重要性。初始CO2压力2 MPa,固液比200 g/L,搅拌速度450 r/min条件下,BJ粉煤灰在不同温度下的矿化能力如图6所示。不同温度下,2 h内BJ粉煤灰的碳化效率依次降低:220 ℃>180 ℃>140 ℃>40 ℃>60 ℃>100 ℃>80 ℃。温度由40 ℃升至220 ℃时,矿化效率先下降后上升。说明温度对直接气液矿化的影响较复杂[24]。
等[21]也得到类似结果,表明温度在矿化过程中的重要性。初始CO2压力2 MPa,固液比200 g/L,搅拌速度450 r/min条件下,BJ粉煤灰在不同温度下的矿化能力如图6所示。不同温度下,2 h内BJ粉煤灰的碳化效率依次降低:220 ℃>180 ℃>140 ℃>40 ℃>60 ℃>100 ℃>80 ℃。温度由40 ℃升至220 ℃时,矿化效率先下降后上升。说明温度对直接气液矿化的影响较复杂[24]。

图6 BJ粉煤灰在不同温度下的矿化能力[24]
Fig.6 Mineralization capacity of BJ coal fly ash at different temperatures[24]
从动力学角度来看,升高温度提高传质速率,促进分子热运动并增加其平均动能,从而提高反应速率。然而液体中游离CO2平衡浓度遵循亨利定律:
C(CO2)=kHP(CO2)。
(5)
其中,C(CO2)为液体中游离CO2 的平衡浓度;kH为亨利常数;P(CO2)为CO2分压,会随温度升高而降低。提高反应温度会降低CO2在溶液中的溶解度,从而导致碳酸根离子浓度降低。此外,温度升高,降低Ca(OH)2溶解度及其在溶液中浓度,而溶液中低浓度的![]() 和Ca2 会减缓CaCO3的形成。另外,矿化反应本身是放热反应,平衡随温度升高而逆向移动。因此,仅提高温度并不能有效提高矿化效率,需在矿化速率和平衡移动之间取得平衡。
和Ca2 会减缓CaCO3的形成。另外,矿化反应本身是放热反应,平衡随温度升高而逆向移动。因此,仅提高温度并不能有效提高矿化效率,需在矿化速率和平衡移动之间取得平衡。
2.2.2 液固比影响
湿法矿化反应有2种反应形式: ① CaO与CO2直接反应生成碳酸盐(CaCO3); ② CaO溶于水生成氢氧化物(Ca(OH)2),与CO2反应生成碳酸盐。CO2过量时,可以形成碳酸氢盐(Ca(HCO3)2)[44]。液固比增大会增强反应②的趋势。但液固比增至某个临界点时,过量水会形成传质屏障,该屏障会降低离子强度,导致Ca2 浸出速率降低,矿化效率不再显著增加[45-46]。
在反应时间1 h、转速900 r/min、初始CO2压力0.2 MPa和室温条件下,粉煤灰浆料在不同液固比下的矿化能力如图7所示,DANANJAYAN等[47]利用Tamilnadu电厂粉煤灰进行CO2矿化时,发现液固比小于15 mL/g时,矿化效率随液固比增加而增加。液固比大于15 mL/g时,液固比增加矿化效率降低。液固比=15 mL/g是形成传质屏障的临界点。另外,UKWATTAGE等[22]用Hazelwood电厂粉煤灰进行CO2矿化时发现液固比=5 mL/g是形成传质屏障的临界点。虽然不同煤种粉煤灰其液固比临界值不同,但较低的液固比有助于提高粉煤灰湿法矿化效率[44,47-48]。

图7 粉煤灰浆料在不同液固比下的矿化能力[47]
Fig.7 Sequestration capacity of CFA slurry at varying liquid-solid ratio[47]
2.2.3 溶液体系影响
溶液体系影响湿法矿化。一些研究通过添加剂改变溶液体系从而改善CO2矿化[49-50]。添加剂主要通过影响整个体系pH从而影响CO2矿化过程。CO2作为一种酸性气体,碱性体系能吸收更多CO2,提供更多的![]() 参与矿化过程。此外,碱性体系还可强化CO2从气相到水相的溶解过程,促进CaCO3形成[51]。如SOONG等[49]在高压反应器中,利用NaOH作为添加剂,开发了一种在盐水中粉煤灰矿化CO2的方法,并表明该混合盐水的CO2封存能力高于使用粉煤灰-水和粉煤灰-盐水体系。
参与矿化过程。此外,碱性体系还可强化CO2从气相到水相的溶解过程,促进CaCO3形成[51]。如SOONG等[49]在高压反应器中,利用NaOH作为添加剂,开发了一种在盐水中粉煤灰矿化CO2的方法,并表明该混合盐水的CO2封存能力高于使用粉煤灰-水和粉煤灰-盐水体系。
JI等[52]研究在半间歇反应器中粉煤灰直接气液矿化过程中添加剂对其矿化CO2能力的影响。在转速500 r/min,固液比100 g/L, 初始 CO2 压力2 MPa条件下,通过添加不同添加剂构建不同溶液体系,进行2 h矿化反应,如图8所示。

图8 不同添加剂对粉煤灰矿化的影响[52]
Fig.8 Effect of different additives on carbonation reaction[52]
不同溶液体系的矿化效率顺序为:Na2CO3>Na2CO3 &NaCl>NaHCO3>H2O。虽然Na2CO3和 NaHCO3 都能使体系处于碱性环境,且有助于保持液相中![]() 浓度。Na2CO3能提供更强的碱性环境,吸收更多CO2提供更多
浓度。Na2CO3能提供更强的碱性环境,吸收更多CO2提供更多![]() 从而在相同反应时间内矿化效率更高。虽然添加NaCl并未改变体系pH,但增加了CaCO3在液相中溶解度,不利于CaCO3沉淀[51]。因此,0.5 mol/L Na2CO3 体系矿化效率高于0.5 mol/L Na2CO3 &0.5 mol/L NaCl 混合体系时的矿化效率。
从而在相同反应时间内矿化效率更高。虽然添加NaCl并未改变体系pH,但增加了CaCO3在液相中溶解度,不利于CaCO3沉淀[51]。因此,0.5 mol/L Na2CO3 体系矿化效率高于0.5 mol/L Na2CO3 &0.5 mol/L NaCl 混合体系时的矿化效率。
2.2.4 预处理的影响
除此之外,粉煤灰预处理也会影响直接气液矿化中粉煤灰的矿化性能[52]。通常炉内高温燃烧后产生的粉煤灰颗粒表面烧结严重,孔隙不发达。矿化前的机械球磨处理可以产生新鲜的表面和孔隙,暴露出更多的反应组分,大幅度增加了接触面积,提高粉煤灰的矿化量[53-54]。例如YUAN等[55]利用球磨机对CFB粉煤灰矿化前进行湿磨预处理,结果发现其矿化容量为37.1 kg/t,远大于原粉的1.8 kg/t。
除常规机械处理外,CO2吸附剂的简单浸渍和掺入也能提升粉煤灰的矿化性能[56-58]。SARMAH等[56]用单乙醇胺/二甲胺(MEA/DMA)和二乙醇胺/二甲胺(DEA/DMA)浸渍粉煤灰进行CO2矿化,发现2种溶剂浸渍的粉煤灰CO2矿化容量明显高于原粉煤灰。化学吸附剂的掺入赋予粉煤灰更多的活性组分参与矿化反应,而粉煤灰又能更好地分散吸附剂,产生更多表面积吸附CO2[57]。粉煤灰直接矿化CO2文献总结见表2。
表2 粉煤灰直接矿化法总结
Table 2 Overview of coal fly ash direct carbonization method

3 间接矿化法
间接矿化常通过使用氢氧化钠、乙酸和氨水等从原料中浸出反应组分 (如Ca2 、Mg2 ),在碱性环境下将其与CO2进行矿化反应[13]。目前,以HCl 和 HNO3代表的无机酸、铵盐和以乙酸为代表的有机酸,都被用作萃取剂用于粉煤灰间接矿化CO2。根据萃取剂类型对粉煤灰间接矿化CO2进行概括。
3.1 无机酸萃取
HCl提取工艺在20世纪四五十年代开发,最先用于从蛇纹石中提取钙镁[13]。后来被用于从粉煤灰中萃取Ca2 。例如YU[64]等利用HCl作为萃取剂用于粉煤灰间接矿化,其中钙的有效提取可以达到80%以上。但如果不将萃取剂回收,该工艺经济效益很低。
传统无机酸萃取剂主要通过传统蒸馏回收。如TEIR等[65]开发出一种可回收萃取剂的新工艺。首先使用HCl或HNO3将蛇纹石中反应组分提取出来,然后通过蒸馏的方式将萃取使用的酸回收(70%~80%)。虽然该工艺浸出率很高,并且能产生纯度高的碳酸盐,但是高昂的试剂成本使得此工艺经济压力极大,并且蒸馏工艺还会带来额外的高能耗。
最近,HO等[3]使用双电极膜电渗析(BPED)技术电解NaNO3溶液,实现低能耗再生使用的HNO3萃取剂和NaOH,CO2矿化容量达110 kg/t。用于酸碱溶液再生的BPED装置如图9所示,与传统的蒸馏回收无机酸萃取剂相比,电解回收萃取剂能耗较低。相比传统再生工艺,电解法不仅能实现低能耗再生,还能产生额外碱或盐等副产品弥补经济效益。但在萃取剂再生阶段,溶液中杂质与OH-发生沉淀反应产生结垢而影响电解过程。此外,电解过程中通常使用风能、太阳能发电取代燃煤发电降低CO2排放,但受气候影响较大。

图9 用于酸碱溶液再生的BPED装置[3]
Fig.9 Configuration of BPED for regeneration of acid and alkaline solution[3]
3.2 铵盐萃取
铵盐提取工艺由PUNDSACK[66]于1967年提出,起初用于从蛇纹石、二氧化碳和硫酸氢铵中生产二氧化硅、氧化铁和碳酸镁。铵盐萃取无需其他试剂升高pH以实现碳酸盐沉淀,因为随反应进行,铵盐水解使溶液碱性增强从而达到碳酸盐沉淀所需pH[67]。
WANG等[68]开发了一种利用硫酸氢铵等铵盐溶解矿物矿化CO2的方法,虽然实现高矿化效率,但矿化过程需消耗大量化学试剂。计算表明,封存1 t CO2,大约需要0.12 t NH4HSO4、2.63 t 蛇纹石、0.04 t NH3和7.48 t NH4HCO3。因此,减少萃取剂量的工艺优化非常重要。
HE等[69]利用可回收的铵盐(NH4Cl/NH4NO3/ CH3COONH4)萃取粉煤灰中的Ca2 用于间接矿化CO2。结果显示NH4Cl/NH4NO3/CH3COONH4能在1 h内从粉煤灰萃取Ca2 用于间接矿化。在25 ℃、铵盐浓度1 mol/L、固液比50 g/L、转速500 r/min、反应时间120 min条件下,钙提取效率随时间变化如图10所示,CH4COONH4的Ca2 萃取效果最好,约40%的Ca2 被萃取到溶液中,其次是NH4NO3和NH4Cl。

图10 不同铵盐提取钙的效率[69]
Fig.10 Extraction efficiency of calcium with different ammonium salts[69]
此研究还报道了一种新工艺,在间接矿化浸出液矿化阶段,传统的直接通入CO2进行矿化的矿化效率比较低(41%~47%),然而用NH4HCO3替代CO2提供![]() 可以大幅度提高其矿化效率(90%~93%)。
可以大幅度提高其矿化效率(90%~93%)。
用NH4HCO3对富含钙的浸出液进行矿化,不仅能提高矿化效率和速率,还能将间接矿化与NH3-H2O体系捕集CO2过程相结合,实现CO2捕集和存储一体化。
对于配备NH3-H2O体系捕集CO2工艺的燃煤电厂,在捕获过程中将形成的NH4HCO3用于对粉煤灰产生的富钙浸出液进行矿化,将高品质碳酸钙矿化作为增值副产物进行回收,在同一个排放点同时实现CO2的捕集和矿化利用。
3.3 有机酸萃取
有机酸起初被用作天然矿物的选择性萃取剂[70],BALDYGA等[71]曾分别以丁二酸、己二酸、醋酸作为萃取剂从CaSiO3中提取Ca2 ,发现使用己二酸或丁二酸代替乙酸时,提取过程更快。在温度80 ℃和压力≥3 MPa条件下,丁二酸的矿化效率高达90%,远超乙酸的30%。同样,有机酸也可用于粉煤灰间接矿化CO2。SUN等[23]将乙酸作为褐煤粉煤灰间接矿化CO2的萃取剂,在60 ℃,1 MPa条件下其矿化容量高达264 kg/t,且温度升高不利于钙形成CaCO3沉淀,而有利于Mg(HCO3)2分解为碳酸盐沉淀物;增加CO2分压可抑制MgCO3沉淀,提高CaCO3纯度。虽然通过有机酸萃取的间接矿化效果与天然矿物CO2矿化性能相似,但在高效实现有机酸萃取剂回收方面关注较少。
最近,ZHENG等[72]开发了一种以甘氨酸作为萃取剂的粉煤灰浸出-矿化循环(LMC)工艺,如图11所示,甘氨酸-甘氨酸根(Gly0-Gly-)可提供pH缓冲体系,使浸出过程中pH维持在8.83~9.59,而pH在8.0~10.5有利于Ca2 浸出不利于杂质离子析出。矿化过程中溶解反应生成的Gly-,不仅可大幅增加CO2在气液相之间的传质[73],还可减缓pH降低,从而促进CO2矿化[74]。

图11 甘氨酸作为萃取剂的LMC工艺机理[72]
Fig.11 Mechanism of LMC process with glycine as extractant[72]
由于整个矿化过程是放热反应,萃取剂再生利用甘氨酸自发质子转移过程的双离子机制,所以LMC工艺可在不需额外能量和物质输入的情况下再生Gly0。
此外,在多循环浸出-矿化试验中,LMC工艺循环性能稳定。浸出液和矿化溶液的Ca2 /Mg2 浓度、CO2负载和pH如图12(a)所示(L-i为第i次循环的浸出液,M-i为第i次循环的矿化溶液),渗滤液的 Ca2 质量浓度9 000~13 000 mg/L,矿化溶液的Ca2 质量浓度2 200~6 300 mg/L,每个周期的渗滤液和矿化溶液的Ca2 浓度接近,约 6 000 mg/L。每次循环后,溶液中钙镁都能被有效消耗。5个周期中,浸出液和矿化溶液的pH均有轻微变化(图12(b)),表明LMC运行稳定。文献中粉煤灰间接矿化CO2的总结见表3。
表3 粉煤灰间接矿化CO2概述
Table 3 Overview of indirect carbonization method of coal fly ash


图12 甘氨酸作为萃取剂的LMC循坏工艺[72]
Fig.12 Glycine as an extractant for LMC-based bad process[72]
与直接矿化相比,间接矿化因其矿化条件温和(避免了直接矿化中高温高压操作)、矿化效率更高和副产物更纯净而备受关注。CO2吸收-矿化一体化技术(IAM)作为一种新型CO2减排封存技术,不仅能快速吸收CO2,且吸收容量大,矿化效率高。通过将粉煤灰矿化CO2技术与IAM工艺结合,利用IAM工艺化学吸收CO2产物(有机胺、铵盐)作为间接矿化萃取剂,不仅解决了间接矿化的萃取剂来源问题,还可将总体工艺成本降低约60%[81]。此外,间接矿化产生的最终矿化产品纯度较高,如WANG等[82]对高炉炉渣间接矿化时获得了高品质和高附加值的富钛、富铝产品,使得CO2间接矿化在经济上更具竞争力。
4 矿化机理
尽管粉煤灰CO2矿化工艺愈发成熟,但仍需要研究矿化机理以更好地控制矿化反应速率和效率。动力学分析可有效表征反应体系中控制反应快慢和平衡的机理因素。CO2矿化过程是复杂的传质反应过程,为简化计算,通常会提出合理假设,基于假设建立模型模拟矿化过程[83],矿化动力学模型示意如图13所示,主要介绍描述矿化反应的2种主流模型:表面覆盖模型和缩核模型[85-89]。

图13 矿化动力学模型示意[84]
Fig.13 Schematic modeling of mineralization dynamics[84]
4.1 缩核模型
对于固体与周围流体的非催化反应,缩核模型可对其反应动力学进行快速评估并确定其反应速率决定步骤[90]。缩核模型特点包括[91]: ① 适用于每个颗粒,但颗粒不作为一个整体。 ② 不适用于解释完全转化的试验。 ③ 在颗粒反应表面周围存在无孔钝化产物层。
在缩核模型中,通常假设在颗粒完全转化为产物前存在未反应的物质核。反应发生在未反应核心表面,然后进入核心内部,留下反应边缘(称为灰层)。未反应核心随反应进行逐渐收缩。反应过程中,以下3个步骤被认为串联发生: ① 流体反应物由流体膜的主体扩散到固体表面; ② 流体反应物和固体在表面上反应;③ 流体反应物通过产物层扩散到未反应的核心表面。
缩核模型能很好描述粉煤灰矿化CO2时出现的钝化层、矿化速率变缓等反应特征。因此,缩核模型在解释CO2矿化反应机理时得到运用[92-93]。由于反应场所、矿化原料、萃取试剂和处理数据方法差异,不同体系机理不同。基于缩核模型,其机理又可细化为产物层扩散 (D-机理)、化学反应控制(C-机理)、薄膜扩散(F-机理)及各机理的联合控制。
ZHONG等[94]用磷石膏(PG)脱硫渣间接矿化CO2,如图14所示,利用缩核模型将浸出过程分为以下5个步骤: ①![]() 通过液相表面边界层扩散到颗粒壳表面;②
通过液相表面边界层扩散到颗粒壳表面;②![]() 通过固体产物层由外壳表面扩散到核心表面;③ 在核心表面发生反应,形成Ca2 和其他产物;④ Ca2 通过固体产物层由核心表面扩散到外壳表面;⑤ Ca2 通过表面边界层由颗粒外壳表面扩散到流体中。
通过固体产物层由外壳表面扩散到核心表面;③ 在核心表面发生反应,形成Ca2 和其他产物;④ Ca2 通过固体产物层由核心表面扩散到外壳表面;⑤ Ca2 通过表面边界层由颗粒外壳表面扩散到流体中。

图14 间接矿化浸出过程动力学模型示意[94]
Fig.14 Schematic of the kinetic model of the extraction process of indirect mineralization[94]
整个过程包括2个液相薄膜扩散、1个化学反应过程和2个固体薄膜扩散过程。通过数据拟合,得出该过程受固体薄膜控制(F-机理)。
MIAO等[95]使用粉煤灰直接气液矿化CO2时,通过反应前后形貌观察到粉煤灰颗粒被结晶CaCO3产物层覆盖,根据缩核模型模拟矿化过程,认为反应开始时气液界面薄膜扩散是速率控制步骤,随时间推移,速率控制步骤转变为产物层扩散(D-机理)。
虽然缩核模型可快速评估矿化反应动力学,但基于无孔的假设使得该模型不适用于多孔颗粒的场景。AHN等[96]指出,仅当反应由内扩散控制时,缩核模型才能适用于多孔颗粒场景。
4.2 表面覆盖模型
表面覆盖模型首先由LIU等[97]用于评估低温下熟石灰 (Ca(OH)2) 的碳酸化和脱硫动力学。表面覆盖模型的假设包括[97]:① 反应产物沉积在固体反应物表面;② 反应只发生在未被反应产物覆盖的未反应表面位点;③ 未被反应产物覆盖的活性表面位点的比例随反应时间变化,具体取决于反应速率;④ 吸附剂的反应表面完全被产物覆盖时,反应转化率最大。
由于与脱硫反应过程相似,表面覆盖模型也用于评估碱性固废的CO2矿化动力学[87,98]。在表面覆盖模型中,反应产物矿化过程中在固体颗粒的活性表面上连续沉积。颗粒表面结构随反应变化。该模型认为随反应进行,颗粒表面产物层不断形成,反应物从内部未反应颗粒通过产物层的扩散将是矿化反应速率控制步骤。PAN等[85]采用表面覆盖模型(图15)。通过测定不同操作条件下碱性炉渣矿化的反应动力学和速率常数,揭示了碱性炉渣CO2矿化的反应动力学和机理。

图15 基于表面覆盖模型假设的矿化机理示意[85]
Fig.15 Schematic representation of the mineralization mechanism based on the assumptions of the surface coverage model[85]
表面覆盖模型的局限性在于仅考虑周围扩散受限边缘的单层,在实际情况下,矿化过程中的产物层和活性物种耗尽层(即收缩核模型中的灰层)可能共存而不是简单的单层。
经典动力学模型为简化计算,通常基于单个扩散阻力描述矿化过程。一些学者为更好地表征矿化过程,结合经典的动力学模型并进行改良,如LEE等[99]将收缩核模型中的化学反应机制与扩散机制相结合,以预测脱硫反应的动力学。由于脱硫反应在较低温度下的气固(固液)非催化反应与矿化反应相似,同样适用于矿化反应[84]。
经典的反应动力学模型如缩核模型和表面覆盖模型能对矿化反应进行快速评估(表4)。
表4 粉煤灰CO2矿化机理总结
Table 4 Overview of CO2 mineralization mechanism of coal fly ash

续表

然而,由于粉煤灰的组分特性和物理性质(不同煤种粉煤灰的颗粒粒径和球型度)会随反应时间动态变化,未来研究方向应利用原位高分辨率设备识别反应颗粒的动态形貌,以更准确描述矿化反应动力学。
5 结 语
相较传统天然矿化原料,粉煤灰显示出矿化CO2的巨大潜力。利用粉煤灰矿化封存CO2,不仅可以实现低成本的CO2矿化,还有望解决粉煤灰处理难题。虽然CO2矿化已经取得了长足的发展,但目前采用的直接或间接矿化工艺流程相对复杂,部分反应条件较苛刻,能耗高,成本高,难以有效实现工业化。不同煤种的粉煤灰物理化学性质差异很大,导致其矿化CO2反应历程也存在差异,在实际应用时需根据情况优化工艺参数。此外,在粉煤灰矿化CO2未来的研究中建议关注以下方面:
1)生产高附加值产品。目前CO2矿化实现工业化应用瓶颈是经济效益。如果矿化反应产物创造的价值可弥补整个矿化工艺的经济成本,有望成为解决CO2封存问题的重要途径。如间接矿化工艺在适当操作条件可生产出具有适当纯度规格的CaCO3产品。此外,粉煤灰中Al、Fe和Ti等价值金属在矿化过程中回收也能弥补经济成本甚至盈利。
2)废水的处理。矿化过程中用水成本在总成本中占一定比例。燃煤发电厂产生大量废水,如果将发电厂废水作为矿化反应的反应溶剂,实现发电厂中气-液-固废的协同处理,将对火力发电行业可持续发展具有重大意义。
3)多参数耦合分析。目前研究主要集中在单一因素(温度、压力、粒径和液固比等)对矿化过程的影响;然而,多因素协同效应鲜见报道。因此,有必要研究各参数对反应的协同作用,以确定较佳反应条件。
4)粉煤灰进行矿化反应后残渣性质的研究。以往研究集中在矿化反应过程,不重视反应后残渣。这是CO2矿化发展到工业应用阶段的挑战。
[1] PARK A H A, JADHAV R, FAN L S. CO2 mineral sequestration: Chemically enhanced aqueous carbonation of serpentine [J]. Canadian Journal of Chemical Engineering, 2003, 81(3/4): 885-890.
[2] LI J, HITCH M. Mechanical activation of magnesium silicates for mineral carbonation: A review [J]. Minerals Engineering, 2018, 128: 69-83.
[3] HO H J, IIZUKA A, SHIBATA E, et al. Circular indirect carbonation of coal fly ash for carbon dioxide capture and utilization [J]. Journal of Environmental Chemical Engineering, 2022, 10(5): 108269.
[4] 阳平坚,彭栓,王静,等.碳捕集、利用和封存(CCUS)技术发展现状及应用展望[J].中国环境科学,2024,44(1):404-416.
YANG Pingjian, PENG Shuan, WANG Jing,et al. Carbon Capture, Utilization and Storage (CCUS) technology development status and application prospects [J].China Environmental Science,2024,44(1):404-416.
[5] 朱磊, 古文哲, 宋天奇, 等.煤基固废矿化封存CO2技术研究进展[J/OL].煤炭科学技术:1-21[2024-01-30].http://kns.cnki.net/kcms/detail/11.2402.TD.20231110.1748.002.html.
ZHU Lei, GU Wenzhe, SONG Tianqi,et al.Research progress of CO2 storage technology by mineralization of coal-based solid waste [J/OL].Coal Science and Technology:1-21[2024-01-30].http://kns.cnki.net/kcms/detail/11.2402.TD.20231110.1748.002.html.
[6] ORR Jr F M. Carbon capture, utilization, and storage: An update [J]. SPE Journal, 2018, 23: 2444-2455.
[7] 李琦, 蔡博峰, 陈帆, 等. 二氧化碳地质封存的环境风险评价方法研究综述[J].环境工程,2019,37(2):13-21.
LI Qi,CAI Bofeng,CHEN Fan, et al.Review of environmental risk assessment methods for carbon dioxide geological storage [J].Environmental Engineering,2019,37(2):13-21.
[8] SEIFRITZ W. CO2 disposal by means of silicates [J]. Nature, 1990, 345: 486-486.
[9] MENG J, LIAO W, ZHANG G. Emerging CO2 mineralization technologies for co-utilization of industrial solid waste and carbon resources in China [J]. Minerals, 2021, 11(3): 274.
[10] 许鑫, 蒋建国, 陈懋喆,等.加速碳酸化技术对城市垃圾焚烧飞灰重金属稳定性影响研究[J].环境科学,2007,28(7):1644-1648.
XU Xin,JIANG Jianguo,CHEN Maozhe,et al.Investigation of the sequestration of CO2 and carbonation process for the stabilization of MSW fly ash [J].Environmental Science,2007,28(7):1644-1648.
[11] 王雷, 金宜英, 聂永丰. 高钙特征焚烧飞灰的加速碳酸化处理及对重金属浸出特性的影响[J].环境科学,2009,30(11):3399-3404.
WANG Lei,JIN Yiying,NIE Yongfeng.Accelerated carbonation of high ca content municipal solid waste incineration fly ash and impact on leaching of heavy metal [J].Environmental Science,2009,30(11):3399-3404.
[12] 王成艳. 加速碳酸化对焚烧飞灰重金属浸出特性及高温迁移特性的影响[D].沈阳:沈阳航空工业学院,2010.
[13] BOBICKI E R, LIU Q, XU Z, et al. Carbon capture and storage using alkaline industrial wastes [J]. Progress in Energy and Combustion Science, 2012, 38(2): 302-320.
[14] WANG N, SUN X, ZHAO Q, et al. Leachability and adverse effects of coal fly ash: A review [J]. Journal of Hazardous Materials, 2020, 396: 122725.
[15] 尉子夜, 张鸿波. “双碳”目标下粉煤灰综合利用路径分析:以内蒙古自治区为例[J].应用能源技术,2022(10):1-5.
YU Ziye,ZHANG Hongbo.Analysis of the comprehensive utilization path of fly ash under the goal of "Double Carbon": Take Inner Mongolia Autonomous Region as an example [J].Applied Energy Technology,2022(10):1-5.
[16] 苗贺朝,王海, 王晓东,等.粉煤灰基防渗注浆材料配比优选及其性能试验研究[J].煤炭科学技术,2022,50(9):230-239.
MIAO Hechao,WANG Hai,WANG Xiaodong,et al.Study on ratio optimization and performance test of fly ash-based impermeable grouting materials[J].Coal Science and Technology,2022,50(9):230-239.
[17] 王吉凤, 付恒毅, 闫晓彤,等.钢渣综合利用研究现状[J].中国有色冶金,2021,50(6):77-82.
WANG Jifeng,FU Hengyi,YAN Xiaotong,et al.Research status of comprehensive utilization ofsteel slag [J].China Nonferrous Metallurgy,2021,50(6):77-82.
[18] LI J, ZHUANG X G, QUEROL X, et al. A review on the applications of coal combustionproducts in China [J]. International Geology Review, 2018, 60(5/6): 671-716.
[19] 肖域, 王晓辉, 马淑花,等.循环流化床粉煤灰中钙的赋存状态[J].建筑材料学报, 2021,24(3):663-670.
XIAO Yu,WANG Xiaohui,MA Shuhua,et al.Occurrence of calcium in fly ash from circulating fluidized bed [J].Journal of Building Materials,2021,24(3):663-670.
[20] 武飞乐,李世春.“双碳”目标下粉煤灰中有价金属回收技术研究[J/OL].中国有色冶金:1-12[2024-01-29].http://kns.cnki.net/kcms/detail/11.5066.TF.20221009.1902.004.html.
WU Feile,LI Shichun.Research on recovery technology of valuable metals from coal fly ash under the Double Carbon target [J/OL]. China Nonferrous Metallurgy:1-12 [2024-01-29].http://kns.cnki.net/kcms/detail/11.5066.TF.20221009.1902.004.html.
[21] UKWATTAGE N L, RANJITH P G, YELLISHETTY M, et al. A laboratory-scale study of the aqueous mineral carbonation of coal fly ash for CO2 sequestration [J]. Journal of Cleaner Production, 2015, 103: 665-674.
[22] UKWATTAGE N L, RANJITH P G, WANG S H. Investigation of the potential of coal combustion fly ash for mineral sequestration of CO2 by accelerated carbonation [J]. Energy, 2013, 52: 230-236.
[23] SUN Y, PARIKH V, ZHANG L. Sequestration of carbon dioxide by indirect mineralization using Victorian brown coal fly ash [J]. Journal of Hazardous Materials, 2012, 209/210: 458-466.
[24] JI L, YU H, ZHANG R, et al. Effects of fly ash properties on ca-rbonation efficiency in CO2 mineralisation [J]. Fuel Processing Technology, 2019, 188: 79-88.
[25] LIU W, SU S, XU K, et al. CO2 sequestration by direct gas-solid
carbonation of fly ash with steam addition [J]. Journal of Cleaner Production, 2018, 178: 98-107.
[26] 李琴, 杨岳斌, 刘君,等.我国粉煤灰利用现状及展望[J].能源研究与管理,2022(1):29-34.
LI Qin,YANG Yuebin,LIU Jun,et al.Present status and prospect of fly ash utilization in China [J].Energy Research and Management,2022(1):29-34.
[27] 姜龙. 燃煤电厂粉煤灰综合利用现状及发展建议[J].洁净煤技术,2020,26(4):31-39.
JIANG Long.Comprehensive utilization situation of fly ash in coal-fired power plants and its development suggestions [J].Clean Coal Technology,2020,26(4):31-39.
[28] 高佼, 刘娜, 王浩. “无废城市”背景下粉煤灰资源化利用途径研究进展[J].能源研究与信息,2022,38(3):150-154,160.
GAO Jiao,LIU Na,WANG Hao.Research process on resource utilization of coal fly ash under the context of zero-waste city [J].Energy Research and Information,2022,38(3):150-154,160.
[29] HE Y, LUO Q, HU H. Situation analysis and countermeasures of China′s fly ash pollution prevention and control [J]. Procedia Environmental Sciences, 2012, 16: 690-696.
[30] 赵仲霖. 粉煤灰制备4A沸石分子筛的研究[J].煤炭加工与综合利用,2008(2):48-51.
ZHAO Zhonglin. Preapring 4A zeolite from coal ash [J]. Coal Processing &Comprehensive Utilization,2008(2):48-51.
[31] ZHANG X, LI C, ZHENG S, et al. A review of the synthesis and application of zeolites from coal-based solid wastes [J]. International Journal of Minerals Metallurgy and Materials, 2022,29(1): 1-21.
[32] QIU B, DENG N, ZHANG Y, et al. Application of industrial solid wastes in catalytic pyrolysis [J]. Asia-Pacific Journal of Chemical Engineering, 2018, 13(1):e2150.
[33] BALAKRISHNAN M, BATRA V S, HARGREAVES J S J, et al. Waste materials - catalytic opportunities: An overview of the application of large scale waste materials as resources for catalytic applications [J]. Green Chemistry, 2011, 13(1): 16-24.
[34] 赵航航, 杨阳, 黄训荣,等.低温改性粉煤灰对土壤镉的钝化修复研究[J].农业环境科学学报,2018,37(8):1642-1650.
ZHAO Hanghang, YANG Yang, HUANG Xunrong, et al. Remediation effects of a new type of low-temperature-modified fly ash on Cd-contaminated soil [J]. Journal of Agro-Environment Science, 2018, 37(8):1642-1650.
[35] LEI C, CHEN T, ZHANG Q Y, et al. Remediation of lead polluted soil by active silicate material prepared from coal fly ash [J]. Ecotoxicology and Environmental Safety, 2020, 206:111409.
[36] 吴宇,张英,李小康,等.燃煤飞灰资源高附加值利用研究进展[J/OL].矿产综合利用:1-21[2024-01-29].http://kns.cnki.net/kcms/detail/51.1251.TD.20231120.1724.016.html.
WU Yu,ZHANG Ying,LI Xiaokang,et al.Research progress of high value-added utilization of coal combustion fly ash resources [J/OL].Multipurpose Utilization of Mineral Resources:1-21[2024-01-29].http://kns.cnki.net/kcms/detail/51.1251.TD.20231120.1724.016.html.
[37] PEI S L, PAN S Y, GAO X, et al. Efficacy of carbonated petroleum coke fly ash as supplementary cementitious materials in cement mortars [J]. Journal of Cleaner Production, 2018, 180: 689-697.
[38] TIAN S, JIANG J, CHEN X, et al. Directgas-solid carbonation kinetics of steel slag and the contribution to in situ sequestration of flue gas CO2 in steel-making plants [J]. ChemSusChem, 2013, 6(12): 2348-2355.
[39] REVATHY T D R, RAMACHANDRAN A, PALANIVELU K. Carbon capture and storage using coal fly ash with flue gas [J]. Clean Technologies and Environmental Policy, 2022, 24(4): 1053-1071.
[40] MONTES-HERNANDEZ G, POMMEROL A, RENARD F, et al. In situ kinetic measurements of gas-solid carbonation of Ca(OH)2 by using an infrared microscope coupled to a reaction cell [J]. Chemical Engineering Journal, 2010, 161(1/2): 250-256.
[41] PRIGIOBBE V, POLETTINI A, BACIOCCHI R. Gas-solid carbonation kinetics of air pollution control residues for CO2 storage [J]. Chemical Engineering Journal, 2009, 148(2): 270-278.
[42] YUAN Q, ZHANG Y, WANG T, et al. Mineralization characteristics of coal fly ash in the transition from non-supercritical CO2 to supercritical CO2 [J]. Fuel, 2022, 318: 123636.
[43] MAZZELLA A, ERRICO M, SPIGA D. CO2 uptake capacity of coal fly ash: Influence of pressure and temperature on direct gas-solid carbonation [J]. Journal of Environmental Chemical Engineering, 2016, 4(4): 4120-4128.
[44] BACK M, KUEHN M, STANJEK H, et al. Reactivity of alkaline lignite fly ashes towards CO2 in water [J]. Environmental Science &Technology, 2008, 42(12): 4520-4526.
[45] BACIOCCHI R, COSTA G, DI BARTOLOMEO E, et al. Carbonation of stainless steel slag as a process for CO2 storage and slag valorization [J]. Waste and Biomass Valorization, 2010, 1(4): 467-477.
[46] ANJALI G, BHAVYA M, KUMAR N A. CO2 sequestration potential of construction and demolition alkaline waste material in Indian perspective [J]. International Journal of Envivonmental and Ecological,2011,78:947-952.
[47] DANANJAYAN R R T, KANDASAMY P, ANDIMUTHU R. Direct mineral carbonation of coal fly ash for CO2 sequestration [J]. Journal of Cleaner Production, 2016, 112: 4173-4182.
[48] BACIOCCHI R, COSTA G, POLETTINI A, et al. Comparison of different reaction routes for carbonation of APC residues [J]. Energy Procedia,2009, 1(1): 4851-4858.
[49] SOONG Y, FAUTH D L, HOWARD B H, et al. CO2 sequestration with brine solution and fly ashes [J]. Energy Conversion and Management, 2006, 47(13): 1676-1685.
[50] NYAMBURA M G, MUGERA G W, FELICIA P L, et al. Carbonation of brine impacted fractionated coal fly ash: Implications for CO2 sequestration [J]. Journal of Environmental Management, 2011, 92(3): 655-664.
[51] CHEN Z Y, O′CONNOR W K, GERDEMANN S J. Chemistry of aqueous mineral carbonation for carbon sequestration and explanation of experimental results [J]. Environmental Progress, 2006, 25(2): 161-166.
[52] JI L, YU H, WANG X, et al. CO2 sequestration by direct mineralisation using fly ash from Chinese Shenfu coal [J]. Fuel Processing Technology, 2017, 156: 429-437.
[53] YUAN Q, ZHANG Y, WANG T, et al. Mechanochemical stabilization of heavy metals in fly ash from coal-fired power plants via dry milling and wet milling [J]. Waste Management, 2021, 135: 428-436.
[54] ZHANG Y, MEI D, WANG T, et al. In-situ capture of mercury in coal-fired power plants using high surface energy fly ash [J]. Environmental Science &Technology, 2019, 53(13): 7913-7920.
[55] YUAN Q, YANG G, ZHANG Y, et al. Supercritical CO2 coupl-ed with mechanical force to enhance carbonation of fly ash and heavy metal solidification [J]. Fuel, 2022, 315: 123154.
[56] SARMAH M, BARUAH B P, KHARE P. A comparison between CO2 capturing capacities of fly ash based composites of MEA/DMA and DEA/DMA [J]. Fuel Processing Technology, 2013, 106: 490-497.
[57] LEE J, HAN S J, WEE J H. Synthesis of dry sorbents for carbon dioxide capture using coal fly ash and its performance [J]. Applied Energy, 2014, 131: 40-47.
[58] MAROTO-VALER M M, LU Z, ZHANG Y, et al. Sorbents for CO2 capture from high carbon fly ashes [J]. Waste Management, 2008, 28(11): 2320-2328.
[59] ALTINER M. Use of direct gas-solid carbonation process for fixation of CO2 as mineral carbonates in Turkish fly ashes [J]. International Journal of Coal Preparation and Utilization, 2021, 41(9): 661-677.
[60] GONZ LEZ A, MORENO N, NAVIA R. CO2 carbonation under aqueous conditions using petroleum coke combustion fly ash [J]. Chemosphere, 2014, 117: 139-143.
LEZ A, MORENO N, NAVIA R. CO2 carbonation under aqueous conditions using petroleum coke combustion fly ash [J]. Chemosphere, 2014, 117: 139-143.
[61] EBRAHIMI A, SAFFARI M, MILANI D, etal. Sustainable tra-nsformation of fly ash industrial waste into a construction cement blend via CO2 carbonation [J]. Journal of Cleaner Production, 2017, 156: 660-669.
[62] MAYORAL M C, ANDRÉS J M, GIMENO M P. Optimization of mineral carbonation process for CO2 sequestration by lime-rich coal ashes [J]. Fuel, 2013, 106: 448-454.
[63] JI L, YU H, WANG X, et al. CO2 sequestration by direct mineralisation using fly ash from Chinese Shenfu coal [J]. Fuel Processing Technology, 2017, 156: 429-437.
[64] YU C, CAI L, JIANG G, et al. Mineral carbonation of CO2 with utilization of coal gasification slags based on chemical looping [J]. Asia-Pacific Journal of Chemical Engineering, 2021, 16(4): e2636.
[65] TEIR S, KUUSIK R, FOGELHOLM C J, et al. Production of magnesium carbonates from serpentinite for long-term storage of CO2 [J]. International Journal of Mineral Processing, 2007, 85(1): 1-15.
[66] PUNDSACK F L, SOMERVILLE N J. Recovery of silica, iron oxide and magnesium carbonate from the treatment of serpentine with ammonium bisulphate:U.S. Patent 3338667[P].1967-08-29.
[67] KODAMA S, NISHIMOTO T, YAMAMOTO N, et al. Development of a new pH-swing CO2 mineralization process with a recyclable reaction solution [J]. Energy, 2008, 33(5): 776-784.
[68] WANG X, MAROTO-VALER M M. Dissolution of serpentine using recyclable ammonium salts for CO2 mineral carbonation [J]. Fuel, 2011, 90(3): 1229-1237.
[69] HE L, YU D, LV W, et al. A novel method for CO2 sequestrat-ion via indirect carbonation of coal fly ash [J]. Industrial &Engineering Chemistry Research, 2013, 52(43): 15138-15145.
[70] ZHANG J, ZHANG R, GEERLINGS H, et al. A novel indirect wollastonite carbonation route for CO2 sequestration [J]. Chemical Engineering &Technology, 2010, 33(7): 1177-1183.
[71] BALDYGA J, HENCZKA M, SOKOLNICKA K. Mineral carbonation accelerated by dicarboxylic acids as a disposal process of carbon dioxide [J]. Chemical Engineering Research and Design, 2011, 89(9): 1841-1854.
[72] ZHENG X, LIU J, WEI Y, et al. Glycine-mediated leaching-mineralization cycle for CO2 sequestration and CaCO3 production from coal fly ash: Dual functions of glycine as a proton donor and receptor [J]. Chemical Engineering Journal, 2022, 440: 135900.
[73] LI Y, DUAN X, SONG W, et al. Reaction mechanisms of carbon dioxide capture by amino acid salt and desorption by heat or mineralization [J]. Chemical Engineering Journal, 2021, 405:126938.
[74] JEON J, KIM M J. CO2 storage and CaCO3 production using seawater and an alkali industrial by-product [J]. Chemical Engineering Journal, 2019, 378:122180.
[75] HAN S J, IM H J, WEE J H. Leaching and indirect mineral carbonation performance of coal fly ash-water solution system [J]. Applied Energy, 2015, 142: 274-282.
[76] RAGIPANI R, SREENIVASAN K, ANEX R P, et al. Direct air capture and sequestration of CO2 by accelerated indirect aqueous mineral carbonation under ambient conditions [J]. ACS Sustainable Chemistry &Engineering, 2022, 10(24): 7852-7861.
[77] 马佳慧,王毅斌,冯敬武,等.工业含钙固废矿化CO2的实验研究[J/OL].化工进展:1-12[2024-01-29].https://doi.org/10.16085/j.issn.1000-6613.2023-0822.
MA Jiahui, WANG Yibin, FENG Jingwu,et al.Experimental study of CO2 mineralization by industrial containing calcium solid wastes [J/OL]. Chemical Industry and Engineering Progress:1-12[2024-01-29].https://doi.org/10.16085/j.issn.1000-6613.2023-0822.
[78] HE L L, YU D, LV W, et al. CO2 Sequestration by indirect carbonation of high-calcium coal fly ash [J]. Advanced Materials Research,2013, 726/731: 2870-2874.
[79] CHANG E E, PAN S Y, YANG L, et al. Accelerated carbon-ation using municipal solid waste incinerator bottom ash and cold-rolling wastewater: Performance evaluation and reaction kinetics [J]. Waste Management, 2015, 43: 283-292.
[80] HOSSEINI T, SELOMULYA C, HAQUE N, et al. Indirect carbonation of victorian brown coal fly ash for CO2 sequestration: Multiple-cycle leaching-carbonation and magnesium leaching kinetic modeling [J]. Energy &Fuels, 2014, 28(10): 6481-6493.
[81] 王中辉, 苏胜, 尹子骏,等. CO2矿化及吸收-矿化一体化(IAM)方法研究进展[J]. 化工进展, 2021,40(4):2318-2327.
WANG Zhonghui,SU Sheng,YIN Zijun,et al.Research progress of CO2 mineralization and integrated absorption-mineralization (IAM) method [J].Chemical Industry and Engineering Progress,2021,40(4):2318-2327.
[82] WANG L, LIU W, HU J, et al. Indirect mineral carbonation of titanium-bearing blast furnace slag coupled with recovery of TiO2 and Al2O3 [J]. Chinese Journal of Chemical Engineering, 2018, 26(3): 583-592.
[83] PAN S Y, LING T C, PARK A H A, et al. An overview: Reaction mechanisms and modelling of CO2 utilization via mineralization [J]. Aerosol and Air Quality Research, 2018, 18(4): 829-848.
[84] WEI C, DONG J, ZHANG H, et al. Kinetics model adaptability analysis of CO2 sequestration process utilizing steelmaking slag and cold-rolling wastewater [J]. Journal of Hazardous Materials, 2021, 404.
[85] PAN S Y, CHIANG P C, CHEN Y H, et al. Kinetics of carbonation reaction of basic oxygen furnace slags in a rotating packed bed using the surface coverage model: Maximization of carbonation conversion [J]. Applied Energy, 2014, 113: 267-276.
[86] CHANG E E, CHEN C H, CHEN Y H, et al. Performance evaluation for carbonation of steel-making slags in a slurry reactor [J]. Journal of Hazardous Materials, 2011, 186(1): 558-564.
[87] CHANG E E, CHIU A C, PAN S Y, et al. Carbonation of basic oxygen furnace slag with metalworking wastewater in a slurry reactor [J]. International Journal of Greenhouse Gas Control, 2013, 12: 382-389.
[88] CHEN T L, JIANG W, SHEN A L, et al. CO2 mineralization and utilization using various calcium-containing wastewater and refining slag via a high-gravity carbonation process [J]. Industrial &Engineering Chemistry Research, 2020, 59(15): 7140-7150.
[89] LI Y, PEI S, PAN S Y, et al. Carbonation and utilization of basic oxygen furnace slag coupled with concentrated water from electrodeionization [J]. Journal of CO2 Utilization, 2018, 25: 46-55.
[90] PAN S Y, LING T C, PARK A H A, et al. An overview: Reaction mechanisms and modelling of CO2 utilization via mineralization [J]. Aerosol and Air Quality Research, 2018, 18(4): 829-848.
[91] BENEDETTI A. Investigation of the CO2 carbonation reaction:
Kinetic models, CFD simulations and thermogravimetric data analysis[D].Padova:University of Padua,2014.
[92] BALDYGA J, HENCZKA M, SOKOLNICKA K. Mineral carbonation accelerated by dicarboxylic acids as a disposal process of carbon dioxide [J]. Chemical Engineering Research &Design, 2011, 89(9): 1841-1854.
[93] LEKAKH S N, RAWLINS C H, ROBERTSON D G C, et al. Kinetics of aqueous leaching and carbonization of steelmaking slag [J]. Metallurgical and Materials Transactions B:Process Metallurgy and Materials Processing Science, 2008, 39(1): 125-134.
[94] ZHONG Y, SHI T, CHEN Q, et al. Leaching calcium from phosphogypsum desulfurization slag by using ammonium chloride solution: Thermodynamics and kinetics study [J]. Chinese Journal of Chemical Engineering, 2020, 28(1): 208-215.
[95] MIAO E, DU Y, ZHENG X, et al. Kinetic analysis on CO2 sequestration from flue gas through direct aqueous mineral carbonation of circulating fluidized bed combustion fly ash [J]. Fuel, 2023, 342: 127851.
[96] AHN H, CHOI S. A comparison of the shrinking core model and the grain model for the iron ore pellet indurator simulation [J]. Computers &Chemical Engineering, 2017, 97: 13-26.
[97] LIU C F, SHIH S M. Kinetics of the reaction of iron blast furnace slag/hydrated lime sorbents with SO2 at low temperatures: Effects of the presence of CO2, O2, and NOx[J]. Industrial &Engineering Chemistry Research, 2009, 48(18): 8335-8340.
[98] CHANG E E, PAN S Y, CHEN Y H, et al. CO2 sequestration by carbonation of steelmaking slags in an autoclave reactor [J]. Journal of Hazardous Materials, 2011, 195: 107-114.
[99] LEE K T, KOON O W J C E J. Modified shrinking unreacted-co-re model for the reaction between sulfur dioxide and coal fly ash/CaO/CaSO4 sorbent [J]. Chemical Engineering Journal,2009, 146(1): 57-62.
[100] MIAO E, DU Y, ZHENG X, et al. CO2 sequestration by direct mineral carbonation of municipal solid waste incinerator fly ash in ammonium salt solution: Performance evaluation and reaction kinetics [J]. Separation and Purification Technology, 2023, 309: 123103.
[101] CHANG E E, PAN S Y, CHEN Y H, et al. Accelerated carbonation of steelmaking slags in a high-gravity rotating packed bed [J]. Journal of Hazardous Materials, 2012, 227/228: 97-106.
[102] MIAO E, DU Y, WANG H, et al. Evaluation of the kinetics of direct aqueous mineral carbonation of wood combustion ash using modified shrinking core models [J]. Environmental Science and Pollution Research, 2023, 30(12): 34009-34021.
[103] CHEN T L, PEI S L, CHIANG P C. Integrated leaching-carbonation kinetic model on CO2 mineralization of alkaline solid wastes in a high-gravity rotating packed bed [J]. Reaction Chemistry &Engineering, 2020, 5(10): 1929-1938.
Research progress of coal fly ash for CO2 mineralization process

移动阅读