含膦多孔有机聚合物负载氧化镁的制备及其CO2吸附性能
0 引 言
随着世界经济和工业飞速发展,人类活动产生的CO2对地球生态环境产生重大影响,如海平面上升、冰川融化及地球温度上升等,因此减少CO2排放迫在眉睫。据联合国政府间气候变化专门委员会(IPCC)报道,到2100年全球气温会上升1.9 ℃[1],其中CO2对全球气温上升贡献55%[2]。而化石燃料电厂是最大的人为排放CO2源头,在CO2总排放量中占近1/3[3]。因此,为应对气候变化,有效降低CO2排放量,习近平总书记在第七十五届联合国大会上郑重承诺:中国将采取有力的政策和措施,二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。
目前,为减少碳排放,积极发展新能源,短期内不可能完全摒弃化石能源的使用。因此,最有利的CO2减排策略为碳捕获、利用与储存技术(Carbon Capture, Utilization and Storage, CCUS)。CCUS技术不仅具有环保和经济优势,而且对未来世界能源结构将会产生重大影响。CO2排放源不同,CCUS技术各不同。根据CO2排放来源,碳捕获技术主要分为燃烧前捕获,燃烧后捕获及富氧燃烧捕获。燃烧前捕获相关技术包括煤气化联合循环发电厂(IGCC)、水合物及吸附技术,燃烧后捕获技术包括吸收法、吸附法、低温分离法及膜分离法[4-5]。
在工业上化学吸收法即液胺捕集CO2技术已普遍应用,但仍面临严重的设备腐蚀、成本高、再生过程易氧化及分解等问题,因此研究人员致力于设计和开发新型材料及技术用于燃煤电厂排放烟道气中CO2捕集。如胺修饰的介孔材料[6]、分子筛[7-8]、水滑石[9]、金属有机骨架(MOFs)[5,10]、金属氧化物[11]及多孔碳[12-14]等。而受限于烟气高温,这些材料无法实现普及应用。如胺修饰的介孔材料易挥发和热分解,分子筛和水滑石在高温下CO2捕获能力较差。同样,几乎没有MOFs材料能在高温常压下吸附CO2。在高温下最常用的CO2吸附剂为含碱金属和碱土金属的固体吸附剂。然而,锂基材料价格昂贵,且需较高的再生温度分解LiCO3[15]。钙基吸附剂同样需高再生温度。MgO因其具有适当的表面碱度,可产生氧空位,是一类非常有前景的CO2吸附剂。在较宽温度(473~673 K)范围内,CO2理论吸附容量高达24.8 mmol/g[16]。但纯MgO因比表面积较低、吸附反应速率较慢且CO2进入MgO吸附剂内部孔道受限,导致CO2吸附容量大幅降低[17]。
目前研究人员尝试采用多种方法提高MgO基吸附剂的比表面积以暴露更多的吸附活性位点,进而提高其吸附容量及吸附速率。如GAO等[18]使用水热合成法制备得到一种类似叶子结构纳米片状的MgO吸附剂,因其具有高比表面积(321.3 m2/g)及丰富的表面活性位点,300 ℃时,CO2吸附容量高达0.96 mmol/g,而工业应用的MgO吸附剂吸附容量通常小于0.06 mmol/g。LI等[19]以醋酸镁为前驱体,椰壳衍生的活性炭为载体,采用浸渍-煅烧法制得MgO/AC吸附剂,在100 ℃、105 Pa条件下,CO2吸附容量为0.19 mmol/g。WANG等[20]以H3PO4为活化剂,核桃壳衍生的活性炭,构筑活性炭基MgO或MgO/Al2O3复合吸附剂,用于CO2捕获。25 ℃,105 Pa下,10% CO2,PAC4(核桃壳基活性炭,4为H3PO4与水热炭质量比)/10% MgO-5%Al2O3吸附剂上获得最优CO2吸附量达4.5 mmol/g。HAN等[21]采用凝胶法制备了一系列不同镁铝物质的量比的MgO@Al2O3吸附剂,并研究了镁铝物质的量比对其吸附性能的影响,结果表明镁铝物质的量比为1∶1时,吸附剂对CO2吸附能力最佳达0.5 mmol/g。LI等[22]采用浸渍法将MgO负载于Al2O3载体上,在不存在和存在水汽的情况下,CO2吸附容量分别达0.95和1.36 mmol/g。因此为提高MgO基吸附剂对CO2吸附性能,研究重点主要集中在制备多孔结构的MgO吸附剂、减小MgO吸附剂粒径或将MgO分散在具有高比表面积的多孔材料上以提高其比表面积。
多孔有机聚合物(Porous Organic Polymer, POPs)因具有高比表面积、多级孔结构及高热稳定性常被用于气体吸附领域[23]。特别是对于含有N、P杂原子的多孔有机聚合物,不仅具有高比表面积,还可提供丰富的碱性位点,更有利于CO2吸附。如LI等[24]采用溶剂热聚合法合成含有季鏻盐和ZnX2-PPh3成分的多孔有机聚合物,在273 K、常压下,P Br-@POPs吸附剂上CO2吸附容量最佳达1.98 mmol/g。GUO等[25]采用傅克酰基化反应制备了一种胺基功能化的卟啉基多孔有机聚合物,在273 K、105 Pa CO2压力下,CO2吸附容量高达3.91 mmol/g。因此,笔者选用具有高比表面积、多级孔结构、富含碱性位点、已实现工业化生产的疏水性含膦多孔有机聚合物POL-PPH3为载体,Mg(OAc)2为前驱体,采用浸渍或超声-煅烧法,制备得到高比表面积的MgO/POL-PPH3吸附剂用于CO2捕获。探究制备方法、煅烧温度、煅烧时间等因素对于MgO/POL-PPH3吸附剂上CO2吸附容量的影响。结合N2物理吸附、傅里叶变换红外(FT-IR)、热重、XRD等表征手段,探究MgO/POL-PPH3吸附剂结构及其CO2吸附性能的对应关系,为MgO基吸附剂的设计合成提供一种研究思路,并且为其工业化生产奠定基础。
1 试 验
1.1 试剂与仪器
乙酸镁(质量分数为98%),无水乙醇(AR),上海麦克林生化科技有限公司;含膦多孔有机聚合物(POL-PPH3),中国科学院大连化学物理研究所。
OTF-1200X型管式炉,合肥科晶材料技术有限公司;HTG-1型热重分析仪,衡州市沃德仪器有限公司;DF-101S型恒温加热磁力搅拌器,巩义市予华仪器有限公司;2XZ-2型旋片式真空泵,临海市谭式真空泵设备有限公司;ASAP2460型物理吸附仪,上海麦克默瑞提克仪器有限公司;PerkinElmer SPECTRUM 3型傅立叶红外光谱,上海珀金埃尔默企业管理有限公司;CJ-040SD型超声清洗机,深圳市超洁科技实业有限公司。
1.2 试验方法
1.2.1 POL-PPH3载体制备
POL-PPH3是已实现工业化生产的聚合物小球,其作为载体,合成路线如图1所示。

图1 POL-PPH3载体的合成技术路线
Fig.1 Schematic representation for synthetic protocol of POL-PPH3 support
1.2.2 MgO/POL-PPH3吸附剂制备
MgO/POL-PPH3吸附剂分别采用浸渍-煅烧法和超声-煅烧法合成。合成路线如图2所示。

图2 MgO/POL-PPH3吸附剂的合成路线
Fig.2 Schematic flow chart of the MgO/POL-PPH3 adsorbents
浸渍-煅烧法:在氮气气氛下,将适量醋酸镁固体溶于一定量无水乙醇中,再加入一定量POL-PPH3,其中Mg负载量为10%,室温搅拌24 h。得到的混合物使用布氏漏斗过滤,无水乙醇洗涤3次。粗产物于75 ℃抽真空4 h去除溶剂,得到白色小球状样品。在研钵中研磨为粉末,之后在氮气气氛下,管式炉中以2 ℃/min升温速率分别升温至不同温度,煅烧一定时间以后,得到的样品命名为MgO/POL-PPH3。根据煅烧温度的不同,样品分别命名为MgO/POL-PPH3-300、MgO/POL-PPH3-350、MgO/POL-PPH3-380。根据煅烧时间不同,样品命名为MgO/POL-PPH3-300-1、MgO/POL-PPH3-300-2、MgO/POL-PPH3-300-3。
超声-煅烧法:氮气气氛下,将适量的醋酸镁固体溶于一定量无水乙醇中,加入一定量POL-PPH3,其中Mg负载量为10%,转入超声清洗机中,室温下超声4 h。得到的混合物使用布氏漏斗过滤,无水乙醇洗涤3次。粗产物于75 ℃抽真空4 h去除溶剂,得到白色小球状样品。在研钵中研磨为粉末,之后在氮气气氛下,管式炉中以2 ℃/min升温速率分别升温至不同温度,煅烧一定时间后,得到样品命名为MgO/POL-PPH3-cs。根据煅烧温度不同,将样品分别命名为MgO/POL-PPH3-cs-300、MgO/POL-PPH3-cs-350、MgO/POL-PPH3-cs-380。
1.3 材料表征与性能测试
利用Empyrean型X射线衍射仪(XRD,Malvern Panalytical B.V.)分析MgO/POL-PPH3材料的晶体结构及物相信息,放射源为Cu Kα(λ=0.154 06 nm),扫描范围为5°~80 °,扫描步长为2 (°)/min,工作电压为40 kV,工作电流为40 mA。利用ASAP 2460型氮气物理吸附仪(BET,Micromeritics Instrument Corp)分析MgO/POL-PPH3材料的比表面积、孔容及孔径分布等。样品测试前,在120 ℃脱气处理12 h,在77 K下得到氮气吸附-脱附曲线。利用BET法计算材料的比表面积,利用BJH方法计算材料的孔径和孔体积。利用Spectrum 3型傅里叶变换红外光谱仪(FT-IR,Perkinelmer LLC)分析MgO/POL-PPH3材料的骨架结构及Mg-O、Mg-P相互作用,分辨率为4.0 cm-1,32次扫描累加,扫描范围4 000~500 cm-1。利用扫描电镜-X射线能谱(SEM-EDX,蔡司Sigma500场发射,Bruker60双探头能谱仪)分析材料的形貌、结构及功能元素分布、含量等信息。样品热稳定性能在HTG-1型热分析仪(TGA,北京恒久实验设备有限公司)上测试,样品用量约10 mg。具体测试过程如下:在流速20 mL/min的N2气氛下,将一定量样品以10 ℃/min升温速率由30 ℃加热至800 ℃,升温同时记录样品质量随温度的变化情况。
MgO/POL-PPH3样品的CO2吸附性能在热重分析仪上(HTG-1,北京恒久实验设备有限公司)进行。具体操作步骤如下:准确称量10 mg样品平铺至陶瓷坩埚内,小心置于加热炉样品架上。加热炉内空气使用N2流(20 mL/min)置换40 min。之后从室温加热至200 ℃保持1 h,脱去样品中吸附的水分及其他杂质。其次,将气路切换为纯CO2(99%),200 ℃吸附30 min。最后以10 ℃/min升温速率N2气氛下加热至400 ℃进行脱附。与此同时,通过分析仪随时记录过程中样品质量变化。CO2吸附容量(Va, mmol/g)计算为

(1)
式中,m0为吸附前吸附剂质量,mg;m1为吸附后吸附剂质量,mg。
2 结果与讨论
2.1 CO2吸附性能
2.1.1 不同制备条件MgO/POL-PPH3样品CO2捕集性能
通过改变制备方法、煅烧温度、煅烧时间等条件获得MgO/POL-PPH3样品的CO2捕获性能(图3)及其CO2吸附容量计算值(表1)。由表1可知,采用浸渍-煅烧法(编号1~3)制备的MgO/POL-PPH3吸附剂,随煅烧温度升高,吸附剂上CO2吸附容量呈下降趋势,即较低的煅烧温度有利于获得高CO2吸附容量。采用超声-煅烧法(编号4~6)制备的MgO/POL-PPH3吸附剂,随煅烧温度升高,吸附剂上CO2吸附容量先升高后下降,煅烧温度为350 ℃时,MgO/POL-PPH3-cs-350吸附剂上获得较高CO2吸附容量,达0.06 mmol/g。浸渍-煅烧法(编号1~3)与超声-煅烧法(编号4~6)制备的MgO/POL-PPH3吸附剂对比,较低的煅烧温度,采用浸渍-煅烧法有利于获得高CO2吸附容量。煅烧温度300 ℃、煅烧时间4 h时,MgO/POL-PPH3-300吸附剂上获得的CO2吸附容量最高达0.07 mmol/g。由图3(a)可知,MgO/POL-PPH3-300吸附剂仅需18 min CO2吸附容量就可达到最高值的93%,说明该吸附剂上活性位点可及性好、吸附速率快。因此从低能耗角度采用浸渍-煅烧法,煅烧温度300 ℃时更有利于获得高效MgO/POL-PPH3吸附剂。煅烧时间对于MgO/POL-PPH3吸附剂吸附CO2性能有重要影响。由表1(编号7~9)可知,随煅烧时间增加,MgO/POL-PPH3吸附剂上CO2吸附容量逐渐降低,特别是煅烧时间由1 h延长至4 h,CO2吸附容量由0.55 mmol/g降至0.07 mmol/g,这可能是由于煅烧时间太长,导致MgO/POL-PPH3吸附剂上暴露的碱性活性位点减少。
表1 不同制备条件MgO/POL-PPH3吸附剂上CO2吸附容量
Table 1 CO2 adsorption capacity on MgO/POL-PPH3 adsorbent at different calcination temperatures and times by different methods


图3 不同制备条件MgO/POL-PPH3的CO2捕获性能
Fig.3 CO2 adsorption of MgO/POL-PPH3 with different preparation conditions
由图3可知,比较浸渍-煅烧与超声-煅烧法获得的MgO/POL-PPH3吸附剂,煅烧温度、煅烧时间相同时,超声-煅烧法比浸渍-煅烧法获得的MgO/POL-PPH3吸附剂上吸附CO2速率慢且暴露的活性位点少,即活性位点可及性差。煅烧时间减少时,虽然吸附容量大幅上升,但对于MgO/POL-PPH3-300-1、MgO/POL-PPH3-300-2、MgO/POL-PPH3-300-3三种吸附剂约需55min才能达到最高值,吸附速率明显减慢。
此外,本研究中MgO/POL-PPH3吸附剂与文献报道的其他MgO基吸附剂对CO2的捕集能力对比见表2。可知MgO/POL-PPH3吸附剂在常压下CO2吸附容量高于低成本的MgO/C吸附剂,略低于高成本的MgO/MCM-41吸附剂上CO2吸附量,因此有望实现工业化应用。
表2 MgO基吸附剂CO2捕集性能对比
Table 2 Comparison of CO2 adsorption capacities of MgO adsorbents

2.1.2 MgO/POL-PPH3吸附剂上CO2吸附动力学
MgO吸附CO2的反应是典型的气固相非催化反应。而MgO/POL-PPH3吸附剂因含有化学吸附位点MgO,也有物理吸附位点含膦多孔有机聚合物POL-PPH3,因此为阐明MgO/POL-PPH3吸附剂上哪种吸附占主导地位及其CO2吸附机理,选择合适的动力学模型,借助试验数据拟合确定合适的吸附动力学参数至关重要。Lagergren动力学模型是普遍接受的基于吸附能力描述的吸附动力学的模型[28]。主要包含准一级模型和准二级模型,这2种模型涉及吸附的所有步骤,如外扩散、内扩散和表面吸附。在准一级模型中,吸附速率被认为与空吸附位点的数量成正比,且吸附剂和吸附质间进行可逆吸附作用。因此准一级模型适合描述物理吸附过程[29],其方程表达式[30]为
ln(qe-qt)=ln qe- k1t,
(2)
式中,qe、qt分别为达到平衡时饱和吸附容量和t时刻的吸附容量,mg/g;k1为准一级平衡速率常数,min-1。
相反,准二级动力学模型被认为是吸附速率与空吸附位点数量的平方成正比,吸附剂和吸附质间通过强键力发生作用,因此准二级模型适合描述化学吸附[31],其方程表达式[32]为

(3)
其中,k2为准二级平衡速率常数,g/(mg·min)。
k1、k2、qe可分别从ln(qe-qt)-t曲线、t/qt-t曲线斜率和截距中求得。
准一级和准二级动力学模型拟合的不同煅烧温度和煅烧时间的MgO/POL-PPH3样品上CO2平衡吸附曲线如图4所示,对浸渍煅烧法制备的不同煅烧温度和不同煅烧时间的MgO/POL-PPH3样品的CO2吸附曲线进行准一级和准二级动力学模型拟合,分别作出ln(qe-qt)-t或t/qt-t曲线,并根据模型对动力学参数进行计算,结果见表3。对于浸渍煅烧法制备的3种不同煅烧温度的MgO/POL-PPH3样品,准一级模型动力学曲线与试验曲线匹配良好(图4(a)),说明准一级模型可较准确描述不同煅烧温度的MgO/POL-PPH3样品的吸附过程,即主要以物理吸附为主,所以高温吸附量较低。而对于不同煅烧时间的MgO/POL-PPH3样品,煅烧时间为1、2和3 h时,准二级模型动力学曲线与试验曲线匹配良好(图4(d)),且R2较高。因此,准二级动力学模型更适合描述不同煅烧时间的MgO/POL-PPH3样品上的CO2吸附行为,可以推断出不同煅烧时间的MgO/POL-PPH3样品上的CO2吸附主要以化学吸附为主。由表3可知,采用准一级动力学模型描述不同煅烧温度的MgO/POL-PPH3样品,吸附动力学常数k1由0.250 min-1增至0.284和0.270 min-1,这种定量改变反映煅烧温度对MgO/POL-PPH3样品上CO2吸附速率的影响,与图3(a)结果相符。采用准二级动力学模型描述不同煅烧时间的MgO/POL-PPH3样品,吸附动力学常数k2由0.009 min-1增至0.015 min-1后降至0.006 min-1,这种定量改变反映煅烧时间对MgO/POL-PPH3样品上CO2吸附速率的影响,煅烧时间为2 h时,动力学吸附速率常数最大,吸附速率最快,达平衡所需时间最短。
表3 不同煅烧温度和煅烧时间的MgO/POL-PPH3样品对CO2的吸附动力学模型参数
Table 3 Fitting parameters of kinetic model for CO2 adsorption by different MgO/POL-PPH3 samples


图4 准一级和准二级动力学模型拟合的不同煅烧温度和煅烧时间的MgO/POL-PPH3样品上CO2平衡吸附曲线
Fig.4 Pseudo-first-order and pseudo-second-order plots of CO2 equilibrium adsorption on the different MgO/POL-PPH3 samples
2.1.3 MgO/POL-PPH3吸附剂上模拟烟气及循环使用性能
对于固体吸附剂捕集实际燃煤烟气中CO2能力及其循环使用性能是其实现工业化应用的2个重要评价指标。因此,探究了MgO/POL-PPH3-300-1吸附剂对于模拟烟气中CO2的捕集性能及其在模拟烟气中捕集CO2的循环使用性能(200 ℃吸附60 min,370 ℃脱附15 min),具体如图5所示。由图5(a)可知,12% CO2浓度下,MgO/POL-PPH3-300-1样品上CO2吸附容量最高达0.02 mmol/g,约需45 min吸附达到饱和。与纯CO2吸附对比,该样品对低浓度CO2的吸附容量降低,但吸附速率未见明显下降。

图5 12% CO2浓度下MgO/POL-PPH3-300-1吸附剂的CO2捕集性能和循环使用性能
Fig.5 CO2 adsorption capacity and recyclability (5 runs) of MgO/POL-PPH3-300-1 adsorbent in 12% CO2
由图5(b)可以看出,整体来说,12% CO2浓度下,MgO/POL-PPH3-300-1样品循环使用5次后,CO2吸附量相对稳定。循环使用1~3次,吸附容量由0.02 mmol/g逐渐升高至0.035 mmol/g,到第5次后,仍可保持较高的CO2吸附容量(0.02 mmol/g),可能是由于在MgO/POL-PPH3-300-1样品上有些碱性吸附位点处于休眠状态,活性位点需要诱导,也可能是由于CO2与MgO/POL-PPH3-300-1样品上的活性位点反应首先生成碳酸盐,未来得及脱附分解又进一步与CO2作用生成碳酸氢盐,所以CO2吸附容量先上升后下降。表明该吸附剂在低浓度CO2下具有良好的循环使用性能,应用前景可观。与Li基、Ca基金属氧化物吸附剂对比,MgO/POL-PPH3-300-1吸附剂在370 ℃便可再生,再生能耗低,具有推广应用优势。
2.2 MgO/POL-PPH3材料的结构表征
利用氮气物理吸附分析不同制备条件MgO/POL-PPH3材料中几个代表样品的比表面积及孔道结构,结果如图6、表4所示。
表4 不同制备条件MgO/POL-PPH3材料的比表面积及孔容
Table 4 Specific surface area and pore volume of MgO/POL-PPH3 materials with different preparation conditions


图6 不同制备条件MgO/POL-PPH3样品的氮气等温吸脱附曲线及孔径分布曲线
Fig.6 N2 adsorption-desorption isotherms and pore size distribution diagrams of MgO/POL-PPH3 adsorbents with different preparation conditions
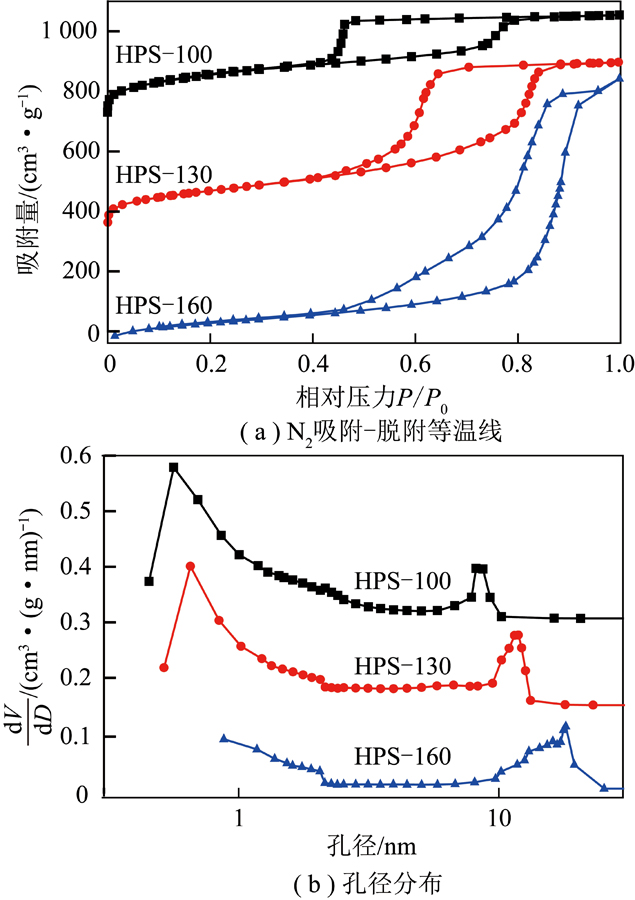
不同煅烧温度及煅烧时间的MgO/POL-PPH3材料的氮气等温吸脱附曲线(图6(a))表明其为典型的I和IV型等温线。在较低压力范围内(P/P0<0.05),可以观察到氮气吸附量陡增,证实材料中存在微孔。在中等压力范围内(0.1 <P/P0<1.0),发现有明显回滞环,表明材料中存在介孔。
从孔径分布曲线(图6(b))可以看出,3种材料孔径分布主要集中在1.26、1.46、2.72、5.02及9.29~50.11 nm,多级孔道结构特别有利于CO2迁移扩散及吸附,进而提高CO2吸附速率。
由表4可知,采用浸渍-煅烧法获得的3种MgO/POL-PPH3材料的比表面积和孔容均小于载体POL-PPH3相应值,但远高于MgO相应值,表明MgO成功分散负载于POL-PPH3载体上,且高比表面积有利于更多碱性活性位点的暴露,再加上多级孔道结构有利于CO2迁移扩散及吸附,使得MgO/POL-PPH3材料可获得高CO2吸附容量及吸附速率。另外,随煅烧温度增加,含膦多孔有机聚合物表面的MgO可能聚集,堵塞孔道,进而减小比表面积,导致CO2吸附容量降低。煅烧温度为300 ℃时,随煅烧时间延长,比表面积增加,孔容增加,表明MgO/POL-PPH3-300-1样品上分散的MgO较多,即POL-PPH3载体内部孔道上进入的MgO多,暴露的碱性活性位点多,故MgO/POL-PPH3-300-1样品可获得较高的CO2吸附容量。
利用SEM表征观察MgO/POL-PPH3-300-1样品的形貌、孔结构及Mg物种分散情况,如图7所示。

图7 MgO/POL-PPH3-300-1样品的SEM及SEM-EDX图
Fig.7 SEM image and elemental distribution in MgO/POL-PPH3-300-1 determined by SEM-EDX
由图7(a)可以看出,MgO/POL-PPH3-300-1样品表面粗糙,存在多级孔道结构。SEM-EDX表征证实MgO/POL-PPH3-300-1样品中所有功能元素(Mg、O、P、C)均高度分散。另外,EDX结果显示在MgO/POL-PPH3-300-1样品中C占78.28%、O占12.45%、Mg占1.86%、P占7.42%。
为进一步获得MgO/POL-PPH3样品结构信息,测试了MgO/POL-PPH3和POL-PPH3样品的FT-IR谱图,如图8所示。

图8 MgO/POL-PPH3-300-1和POL-PPH3样品的FTIR谱图
Fig.8 FTIR spectra of MgO/POL-PPH3-300-1 and POL-PPH3 sample
由图8可以看出,载体POL-PPH3与MgO/POL-PPH3-300-1的红外结构谱图基本类似,其中2 927和1 404 cm-1处归属为—CH—CH2的伸缩振动和弯曲振动,1 599和1 497 cm-1处峰则归属于芳环中的C—C伸缩振动[34]。另外,437和473 cm-1时的振动与MgO有关[35-36],这表明醋酸镁已经被成功负载到载体POL-PPH3上,并且煅烧后转化为MgO。
吸附剂的热稳定性也非常重要。高热分解温度有利于吸附剂脱附CO2,不至于发生骨架分解及坍塌。POL-PPH3载体和MgO/POL-PPH3-300-1样品热重分析如图9所示。

图9 MgO/POL-PPH3-300-1和POL-PPH3样品的TG谱图
Fig.9 TG analysis of MgO/POL-PPH3-300-1 and POL-PPH3 sample
由图9可以看出,载体POL-PPH3和MgO/POL-PPH3样品在100 ℃左右质量下降大约3%,这可能是由于载体和吸附剂表面吸附的水分子及其他杂质气体。另外,载体POL-PPH3和MgO/POL-PPH3样品在大约410 ℃开始分解,这表明其热稳定性很好。
不同制备条件MgO/POL-PPH3样品的XRD图如图10所示。

图10 不同制备条件MgO/POL-PPH3样品的XRD图
Fig.10 XRD pattern of MgO/POL-PPH3 sample
由图10可以看出,MgO/POL-PPH3-380-4、MgO/POL-PPH3-350-4、MgO/POL-PPH3-300-4样品谱图中可观察到2θ=12°~35°宽衍射峰,其对应于无定形的POL-PPH3。而MgO/POL-PPH3-300-1样品谱图中可看到2θ=16°~36°宽衍射峰,也与无定形POL-PPH3有关。未出现MgO明显衍射峰,这说明MgO在POL-PPH3载体表面高度分散,这是因为一些盐类和氧化物在载体表面具有自发单层分散倾向,并且10%负载量未达到载体材料阈值,所以未出现MgO衍射峰[37]。
3 结 论
1)浸渍-煅烧法优于超声-煅烧法,随煅烧温度升高,CO2吸附容量下降,随煅烧时间增加,CO2吸附容量下降,煅烧温度300 ℃、煅烧时间1 h时,MgO/ POL-PPH3-300-1吸附剂上CO2吸附容量高达0.55 mmol/g。12% CO2浓度下,MgO/POL-PPH3-300-1吸附剂循环使用5次后,CO2吸附量仍保持0.02 mmol/g。
2)结合多种表征手段证明,MgO/POL-PPH3-300-1吸附剂具有高CO2吸附容量可归因于其具有较高的比表面积和多级孔道结构,有利于暴露更多的碱性活性位点并强化CO2在孔道内的迁移扩散及吸附。MgO在载体上高度分散也有利于增强与CO2的接触,以加快吸附速率。
3)动力学模型显示浸渍煅烧法不同煅烧温度的3个吸附剂上CO2吸附行为以物理吸附为主,而不同煅烧时间包括MgO/POL-PPH3-300-1吸附剂主要以化学吸附为主。
4)本文制备的MgO/POL-PPH3材料为MgO基吸附剂捕集CO2提供一种新思路,由于来源广泛、再生相对容易,结合了多孔材料的高比表面积、多级孔道等优良特性,具有良好的应用场景。
[1] GBEE J L K, RAVI K, SINGH M, et al. Hierarchical porous nitrogen-doped carbon supported MgO as an excellent composite for CO2 capture at atmospheric pressure and conversion to value-added products [J]. Journal of CO2 Utilization, 2022, 65: 1-12.
[2] IPCC 2014.Climate change 2014: Synthesis report. Contribution of working groups I, II and III to the fifth assessment report of the intergovernmental panel on climate change[EB/OL].(2014-01-01)[2024-03-01].http://www.ipcc.ch.
[3] CHOI S, DRESE J H, JONES C W. Adsorbent materials for ca-rbon dioxide capture from large anthropogenic point sources [J]. ChemSusChem, 2009, 2(9): 796-854.
[4] YAN J, ZHANG Z. Carbon capture, utilization and storage (CCUS) [J]. Applied Energy, 2019, 235: 1289-1299.
[5] SUN Z, LIAO Y, ZHAO S, et al. Research progress in metal-organic frameworks (MOFs) in CO2 capture from post-combustion coal-fired flue gas: Characteristics, preparation, modification and applications [J]. Journal of Materials Chemistry A, 2022, 10: 5174-5211.
[6] OUYANG H, SONG K, DU J, et al. A novel amine-impregnated porous organic polymer with chemisorption sites for highly efficient CO2 chemical conversion under ambient conditions [J]. SSRN Electronic Journal, 2022,5:3574-3584.
[7] BAN Y, LI Z, LI Y, et al. Confinement of ionic liquids in nanocages: Tailoring the molecular sieving properties of ZIF-8 for membrane-based CO2 capture [J]. Angewandte Chemie International Edition, 2015, 54(51): 15483-15487.
[8] 皇甫林,尚波,罗中秋,等.含钛渣制备多孔沸石分子筛吸附剂及其CO2吸附性能[J/OL].精细化工,1-14[2024-04-16].https://doi.org/10.13550/j.jxhg.20230795.
HUANGFU Lin, SHANG Bo, LUO Zhongqiu, et al. Preparation and CO2 adsorption performance of porous zeolite molecular sieve adsorbents using titanium-bearing slag[J/OL].Fine Chemicals,1-14[2024-04-16].https://doi.org/10.13550/j.jxhg.20230795.
[9] KIM S, YOON H J, LEE C H, et al. Effects of alkali-metal nitrate salts on hydrotalcite-based sorbents for enhanced cyclic CO2 capture at high temperatures [J]. Journal of CO2 Utilization, 2023, 77: 102610.
[10] 王焕君, 靳归, 李野, 等. 基于不同粒径ZIF-8多孔液体的二氧化碳捕集性能 [J]. 精细化工, 2023, 40(3): 572-583.
WANG Huanjun, JIN Gui, LI Ye, et al. Carbon dioxide capture performance of porous liquids based on ZIF-8 with different particle sizes [J]. Fine Chemicals, 2023, 40(3): 572-583.
[11] CHANG R, WU X, CHEUNG O, et al. Synthetic solid oxide sorbents for CO2 capture: State-of-the art and future perspectives [J]. Journal of Materials Chemistry A, 2022, 10(4): 1682-1705.
[12] SHEN Y. Preparation of renewable porous carbons for CO2 capture:A review [J]. Fuel Processing Technology, 2022, 236: 107437.
[13] 王秀, 郝健, 郭庆杰. 多孔碳结构调控及其在二氧化碳吸附领域的应用[J]. 洁净煤技术, 2021, 27(1): 135-143.
WANG Xiu, HAO Jian, GUO Qingjie. Porous carbon structure control and its application in the field of carbon dioxide adsorption [J]. Clean Coal Technology, 2021, 27(1): 135-143.
[14] 俞泽涛, 曾光华, 周雅彬, 等. 中药固废制备多孔碳及其CO2吸附性能 [J]. 洁净煤技术, 2022, 28(10): 203-211.
YU Zetao, ZENG Guanghua, ZHOU Yabin, et al. Preparation of porous carbon from traditional Chinese medicine residue and its CO2 adsorption performance [J]. Clean Coal Technology, 2022, 28(10): 203-211.
[15] 胡希璇,潘登,薛天山,等.Li4SiO4基CO2吸附材料研究进展与趋势, 洁净煤技术, 2022, 28(9):11-29.
HU Xixuan, PAN Deng, XUE Tianshan, et al. Recent advances and trend of Li4SiO4-based CO2 adsorbents[J]. Clean Coal Technology, 2022, 28(9):11-29.
[16] GAO W,ZHOU T,GAO Y,et al.Molten salts-modified MgO-based adsorbents for intermediate-temperature CO2 capture: A review[J].Journal of Energy Chemistry,2017,26:830-838.
[17] LI P, CHEN R, LIN Y, et al. General approach to facile synthesis of MgO-based porous ultrathin nanosheets enabling high-efficiency CO2 capture [J]. Chemical Engineering Journal, 2021, 404: 126459.
[18] GAO W,ZHOU T, LOUIS B,et al. Hydrothermal fabrication of high specific surface area mesoporous MgO with excellent CO2 adsorption potential at intermediate temperatures [J].Catalysts, 2017, 7: 1-15.
[19] LI Y Y,HAN K K, LIN W G, et al. Fabrication of a new MgO/C sorbent for CO2 capture at elevated temperature [J].Journal of Materials Chemistry A, 2013, 1: 12919-12925.
[20] PU Q, WANG Y, WANG X, et al. Biomass-derived carbon/MgO-Al2O3 composite with superior dynamic CO2 uptake for post combustion capture application [J]. Journal of CO2 Utilization, 2021, 54: 1-9.
[21] HAN S J, BANG Y, KWON H J, et al. Elevated temperature CO2 capture on nano-structured MgO-Al2O3 aerogel: Effect of Mg/Al molar ratio [J]. Chemical Engineering Journal, 2014, 242: 357-363.
[22] LI L, WEN X, FU X,et al. MgO/Al2O3 sorbent for CO2capture [J]. Energy &Fuels, 2010, 24: 5773-5780.
[23] WANG W, ZHOU M, YUAN D. Carbon dioxide capture in amorphous porous organic polymers [J]. Journal of Materials Chemistry A, 2017, 5(4): 1334-1347.
[24] LI C, WANG W, YAN L,et al. Phosphonium salt and ZnX2-PPh3 integrated hierarchical POPs: Tailorable synthesis and highly efficient cooperative catalysis in CO2 utilization [J]. Journal of Materials Chemistry A, 2016, 4: 16017-16027.
[25] GUO Jiangfei, WANG Lizhi, DU Zhang, et al Amino-functionalized porphyrin-based porous organic polymers for CO2 capture and Hg2 removal [J]. Energy &Fuels, 2020, 34: 9771-9778.
[26] RUHAIMI A H, AZIZ M A A, JALIL A A. Magnesium oxide-based adsorbents for carbon dioxide capture: Current progress and future opportunities [J]. Journal of CO2 Utilization, 2021, 43: 101357.
[27] HANIF A, SUN M, TAO Z, et al. Silica supported MgO as an adsorbent for precombustion CO2 capture [J]. ACS Applied Nano Materials,2019, 2: 6565-6574.
[28] DING Y, ZHAO X, CHEN L,et al. Hydration activation of MgO pellets for CO2 adsorption [J]. Industrial &Engineering Chemistry Research,2021,60:5310-5318.
[29] SONG G,ZHU X,CHEN R,et al. An investigation of CO2 adsorption kinetics on porous magnesium oxide[J].Chemical Engineering Journal,2016,283:175-183.
[30] D EZ N,
EZ N,  LVAREZ P, GRANDA M, et al .CO2 adsorption capacity and kinetics in nitrogen-enriched activated carbon fibers prepared by different methods[J]. Chemical Engineering Journal, 2015, 281:704-712.
LVAREZ P, GRANDA M, et al .CO2 adsorption capacity and kinetics in nitrogen-enriched activated carbon fibers prepared by different methods[J]. Chemical Engineering Journal, 2015, 281:704-712.
[31] LOGANATHAN S, TIKMANI M, EDUBILLI S, et al. CO2 adsorption kinetics on mesoporous silica under wide range of pressure and temperature[J]. Chemical Engineering Journal, 2014, 256: 1-8.
[32] ROTTE N K, YERRAMALA S, BONIFACE J, et al. Equilibri-um and kinetics of Safranin O dye adsorption on MgO decked multi-layered graphene [J]. Chemical Engineering Journal, 2014, 258: 412-419.
[33] DING J, ZHANG J, ZHANG C, et al. Effects of La doping and preparation conditions on magnesia-based adsorption materials prepared by salicylic acid complex-combustion method for CO2 capture [J]. Journal of Environmental Chemical Engineering, 2023, 11(109391): 1-12.
[34] SONG J, ZHANG K, HUANG Z, et al.A porous organic polymer supported Pd/Cu bimetallic catalyst for heterogeneous oxidation of alkynes to 1,2-diketones [J]. Catalysis Science &Technology, 2022, 12: 722-727.
[35] LIU G L, ZHU Y M, MA Z J, et al. Mechanism analysis of FTIR absorption characteristic of MgO nano-powder[J]. Advanced Materials Research, 2010, 158: 145-158.
[36] SELVAM N C S, KUMAR R T, KENNEDY L J, et al. Comparative study of microwave and conventional methods for the preparation and optical properties of novel MgO-micro and nano-structures [J]. Journal of Alloys and Compounds, 2011, 509: 9809-9815.
[37] 王珏,赵壁英,谢有畅, MgO/HZSM-5中MgO分散状态和催化性能的关系[J].物理化学学报,2001, 11(17): 966-971.
WANG Jue, ZHAO Biying, XIE Youchang. Correlations between the dispersion state of MgO and Catalytic behavior of MgO/HZSM-5 [J].Acta PhySico-Chimica Sinica, 2001, 11(17): 966-971.
Preparation and CO2 adsorption performance of a phosphine-containing porous organic polymer supported magnesium oxide

移动阅读