铬掺杂铝基载氮体的化学链合成氨特性及机理
0 引 言
氨是一种重要的化工原料,也是一种潜在的无碳清洁能源,极具发展潜力。目前,世界上90%的氨通过Haber-Bosch法生产,即借助催化剂作用,在高温高压条件下使氮氢混合气生成氨[1];该过程单程转化率在20%左右,且能耗较高。我国煤炭资源丰富,Haber-Bosch法合成氨工艺主要以煤为原料,利用煤与烃类加热并与水蒸气反应制得合成氨所需氢气造成大量CO2排放[2]。随着“碳达峰、碳中和”政策的施行,国家要求合成氨工业制定碳减排方案,加强节能降碳技术改造,进一步提高了合成氨生产成本[3]。因此,开发一种绿色、低能耗、可持续发展的合成氨工艺势在必行。
相比之下,化学链合成氨(Chemical Looping Ammonia Generation,CLAG)技术借助载氮体将合成氨反应分为氮化和氨化2个步骤生产NH3,避免了N2和H2在催化剂表面的竞争性吸附,提高了单程转化率[4-5];同时其碳元素以CO形式输出,降低CO2排放,实现用炭而不排放CO2。
该方法最早由GALVEZ等[6-8]提出,此后,该团队从热力学、动力学、经济性、循环性等多个角度对该工艺进行分析,证明了其工业应用的可行性。FANG等[9-10]建立了一套CLAG集成系统,模拟结果表明其能耗、CO2排放量均远低于传统氨合成工艺。对于CLAG技术,改善载氮体Al2O3性质,使其具有优异的氮化氨化反应活性及循环稳定性是载氮体优化的核心问题之一。研究表明,在载氮体中引入Y2O3或CaF2作为添加剂,可降低AlN合成温度[11-14]。同时,有学者指出在合成过程中掺杂碱土金属氧化物Ba[15]或Sr[16]或稀土氧化物La[17-18]可提高Al2O3比表面积与热稳定性,减少烧结。由于目前氮化反应温度超过了γ-Al2O3向α-Al2O3相变的温度[19],随着化学链合成氨循环反应的进行,铝基载氮体会缓慢转化为活性较低的α-Al2O3,导致反应效率降低。载氮体优化的另一种思路是降低其晶格氧的稳定性[20],SAID等[21]系统研究锰基载氮体的化学链合成氨性能时发现,Fe、Co、K、Li等共金属的存在能有效提高锰的氮化物的氮转移性能。MICHALSKY等[22-23]提出,过渡金属Cr的氮化物同样可作为化学链合成氨载氮体,且相较于其他载氮体,Cr2N很容易继续氮化生成CrN。王占考等[24]研究Cr-Al涂层中发现,Cr的存在会加速涂层中Al的选择性氧化,在Al含量较低的情况下仍能促进Al2O3薄膜生成。
先前研究炭源对铝基载氮体化学链合成氨过程的影响,发现炭的理化结构会显著影响氮化铝的生成速率和转化率,无序化程度高的炭源更易参与反应[25]。以生物炭为炭源进行试验,发现碱金属K可促进氮化反应的进行[26]。此外发现载氮体存在稳定性较差的问题,于是将Si原子掺杂进入Al2O3晶格中,成功提高其比表面积和热稳定性[27]。对于氨化反应,首先探明铝基载氮体的氨化反应特性及机理,提出羟基介导质子转移理论,开发了TiO2负载的载氮体[28]。针对氨分解问题,提出了NH3分子吸附理论,发现ZrO2表面富含的Lewis酸位点能对产物NH3进行分子吸附,进而减少氨分解,提高合成氨产率[29]。为进一步提高Al2O3/AlN作为载氮体在CLAG过程中反应活性,从降低晶格氧稳定性的思路出发,利用共沉淀法合成了一种Cr掺杂Al2O3,有效提高了Al2O3/AlN载氮体的合成氨性能。运用XRD、XPS等对载氮体结构进行表征分析,结合密度泛函理论深入探究了Cr原子引入对载氮体氮化反应的促进机理。最后验证了Cr掺杂Al2O3的CLAG循环稳定性。
1 试 验
1.1 载氮体的制备
采用共沉淀法制备了一系列Cr掺杂铝基载氮体。具体制备步骤:① 称取一定比例的金属硝酸盐(Al(NO3)3·9H2O、Cr(NO3)3·9H2O),倒入去离子水中充分搅拌,完全溶解后得到混合溶液A。② 取一定量碳酸氨((NH4)2CO3)晶体,倒入去离子水中充分溶解,向溶液中加入一定比例丙三醇,搅拌,得到混合溶液B。③ 在持续搅拌状态下,用滴管将溶液B缓慢滴加到溶液A中,使其沉淀完全。继续搅拌直至成凝胶状,然后在室温下充分老化24 h。④ 将老化后的沉淀物用无水乙醇充分抽滤、洗涤,然后置于80 ℃干燥箱中干燥10 h,取出烘干的样品研磨均匀。⑤ 将干燥后的固体放入马弗炉中,以10 ℃/min升温至800 ℃煅烧4 h,继续以10 ℃/min升温至1 300 ℃煅烧1 h。得到一系列Cr、Al物质的量比为x%(x=0、2.5、5.0、7.5、10.0)的载氮体,记为CA-x%。
1.2 试验装置及方法
1.2.1 化学链合成氨固定床试验系统
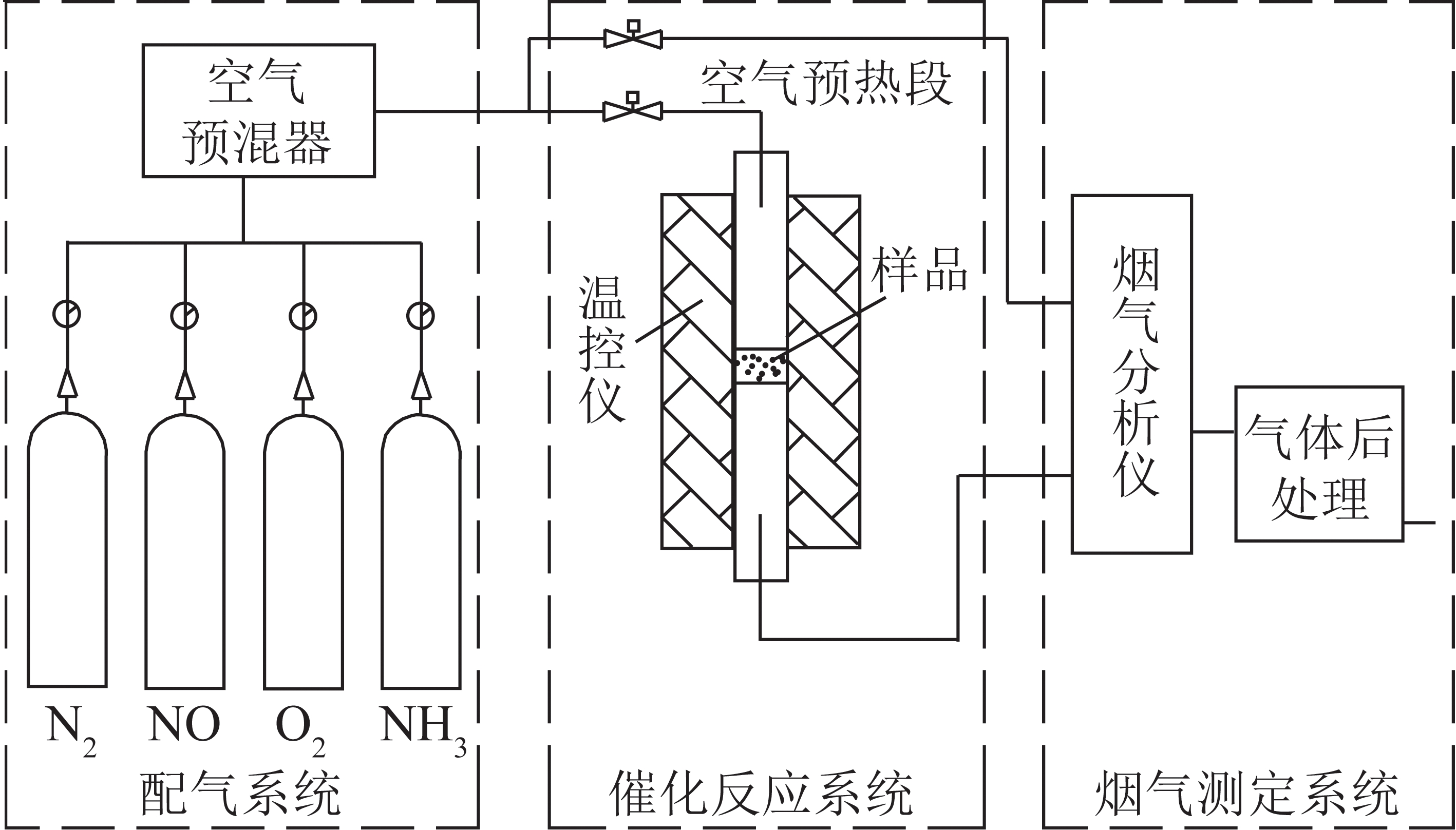
使用固定床试验台进行氮化-氨化反应试验,探究载氮体的合成氨特性。试验装置如图1所示,主要由供气系统、固定床反应器、尾气收集系统3部分组成。其中,供气系统可精准供给氮化反应所需N2和氨化反应所需Ar、水蒸气。固定床反应器主体为管式炉,其内部温度通过电加热系统精确控制,最高反应温度1 800 ℃。马弗炉用于去除氮化反应后残余的炭,分析天平用于称量记录各反应前后样品质量变化。尾气收集系统主要通过氨气吸收瓶收集氨化反应产生的氨气并借助自动电位滴定仪中和滴定计算氨气收集量。具体试验步骤如下:

图1 固定床试验台
Fig.1 Fixed bed test bench
1)氮化反应试验。用天平称取0.52 g铝基载氮体与0.184 g活性炭(铝源与炭源物质的量比为1∶3)置于研钵中,充分研磨均匀。将混合后样品平铺在耐高温的刚玉载舟上,置于300 ℃干燥箱中干燥1 h以去除其中吸收的水分,称量干燥后的样品质量。将载舟送入管式炉中央(管外径60 mm,内径50 mm),设置反应温度由室温升温至1 400 ℃,升温速率10 ℃/min,升温过程通入Ar清除管路中的空气。温度升至预定反应温度时,将Ar切换为N2,保持气体流速为100 mL/min,反应时长1 h。反应结束后,将N2切换回Ar。待管式炉冷却至室温后,取出载舟称量并记录反应前后样品质量变化。
2)氨化反应试验。首先,将氮化反应产物置于马弗炉中在800 ℃下通入空气加热30 min,除去氮化反应产物中残余炭,记录质量变化。再次将样品送入氨化管式炉中,设置反应温度由室温升温至1 000 ℃,升温速率10 ℃/min。升温过程通入Ar,当温度升至预定的反应温度时,调节水蒸气和Ar的流速分别为400和100 mL/min,使蒸汽发生器加热蒸发所得水蒸气和作为载气的Ar以流速比4∶1均匀混合后送入管式炉中与样品反应,时长1 h。尾气通入盛有150 mL H2SO4溶液(浓度1.5×10-5 mol/L)的吸收瓶中。反应结束后,待管式炉冷却至室温,取出载舟称量记录反应前后样品质量变化。向吸收瓶中加入3~5滴甲基红试剂,通过自动电位滴定仪用0.2 mol/L的NaOH溶液对吸收瓶内液体进行滴定。吸收瓶内液体的颜色由品红变为浅红时停止滴定,记录滴定过程中消耗的NaOH溶液体积,计算得到所收集的NH3量。循环试验中,将完成反应的样品再次与炭源充分混合进行下一组循环。
1.2.2 载氮体性能评价指标
铝基载氮体化学链合成氨基本反应原理如下:
氮化:
Al2O3 3C N2![]() 2AlN 3CO,
2AlN 3CO,
(1)
氨化:
2AlN 3H2O![]() Al2O3 2NH3。
Al2O3 2NH3。
(2)
炭转化率x、氮化铝产量nAl为
x=3MC(m0-m1)/(ΔM1mC),
(3)
nA1=2(m0-m1)/ΔM1,
(4)
式中,MC为碳的摩尔质量,12 g/mol;mC为氮化反应前样品中炭的质量;m0、m1分别为氮化反应前后样品质量,g;ΔM1为式(1)的摩尔质量差,56 g/mol。
NH3收集量nN为
nN=2qHVH-qOHΔVOH,
(5)
式中,qH为稀硫酸吸收液浓度,1.5×10-5 mol/L;VH为使用的稀硫酸吸收液体积,150 mL;qOH为滴定用标准NaOH溶液的浓度,0.2 mol/L;ΔVOH为滴定过程中消耗的NaOH溶液体积,mL。
氮化铝反应量nA2为
nA2=2(m2-m3)/ΔM2,
(6)
式中,m2、m3分别为氨化反应前后的样品质量,g;ΔM2为式(2)的摩尔质量差,20 g/mol。
氮化铝反应率λ为
λ=(nA2/nA1)×100%。
(7)
氨气收集率s为
s=(nN/nA2)×100%。
(8)
1.3 密度泛函(DFT)计算方法
模拟计算采用Material Studio软件中的CASTEP[30]模块。Al2O3模型空间群为R-3C,晶格参数为a=b=0.475 9 nm,c=1.299 1 nm,α=β=90°,γ=120°。选择Al2O3(001)表面进行切面,建立3×3×1超胞,设置真空层为1.5 nm以减少原子之间的相互作用力。结构优化采用BFGS(Broyden-Fletcher-Goldfarb-Shanno)算法;在结构优化过程中,对体系内全部原子全部放开优化;赝势采用OTFG-ultrasoft,泛函采用GGA-PBE(广义近似泛函);为保证计算的准确性和效率,设置截断能为450 eV。自洽场精度收敛标准、能量精度收敛标准、最大应力、最大应变、最大位移收敛标准分别设为2.0×10-6 eV/atom,5.0×10-6 eV/atom,0.001 eV/nm,0.02 GPa 和0.000 2 nm。过渡态搜索采用LST/QST方法确定。
采用原子替换法[31]构建Cr掺杂的氧化铝模型,进行结构优化后得到Cr-Al2O3(001)表面模型。由于试验中氮化反应所涉及的温度较高(1 400 ℃),该温度下煤炭等炭源的挥发分早已析出(450~500 ℃),反应时炭源基本以焦炭形式与载氮体反应,结合文献对焦炭模型的研究,以含有6个碳环的多环芳烃模型模拟焦炭分子[32-33],如图2所示。

图2 Al2O3基材料表面模型及炭模型示意
Fig.2 Schematic diagram of surface model of Al2O3-based material and carbon model
通过吸附能、活化能评估掺杂前后载氮体模型的反应活性,计算公式为
Eads=EA/slab-(EA Eslab),
(9)
Ea=ETS-EIS,
(10)
Er=EFS-EIS。
(11)
其中,Eads为吸附能,反映吸附分子与吸附质之间吸附的可能性及程度,吸附能为负表示吸附过程放出热量,吸附反应能自发进行,其绝对值越大,表明吸附作用越强,吸附越稳定;Eslab为晶面板层模型的能量;EA/slab为气体分子A单独吸附于晶体表面时板层模型的能量;EA为气体分子A的能量;Ea为反应活化能;ETS为过渡态能量;EIS为初态能量,反应能垒越大说明反应越不易发生;Er为反应能;EFS为终态能量,反应能为正,说明反应吸收热量,反之说明反应放出热量。
2 结果与讨论
2.1 表征分析
通过X射线衍射仪(XRD)分别对5种CA-x%载氮体样品进行物相分析,以确定载氮体的晶体结构,结果如图3(a)所示。由图3(a)可以发现,5种载氮体的XRD均呈现α-Al2O3的衍射峰,而未发现铬或铬氧化物的衍射峰,表明Cr原子均匀进入氧化铝骨架中。另一方面,与未掺杂的CA-0%载氮体样品相比,Cr掺杂样品的(001)面衍射峰位置逐渐向低角度方向偏移,这主要是Cr原子成功掺杂进入氧化铝晶体骨架中引起;同时样品衍射峰强度逐渐减弱,这说明Cr元素掺杂降低了氧化铝的晶格稳定性。

图3 不同新鲜载氮体XRD、XPS谱图
Fig.3 XRD and XPS spectra of different fresh nitrogen carriers
为进一步探究载氮体的元素组成,对CA-x%样品进行X射线光电子能谱(XPS)分析。各元素结合能的位置见表1。各载氮体的O1s图谱如图3(b)所示,可知OⅠ的峰值位置约530.5 eV,代表晶格氧(O2-),OⅡ的峰值位置约532 eV,代表空位氧。通过分析晶格氧与空位氧的占比可表征氧化铝材料的氧活性。与其他样品相比,CA-5%的载氮体样品具有最高的空位氧比例(25.17%),表明该样品具有最高的反应活性。
表1 不同样品XPS分峰后各元素结合能位置及OⅠ、OⅡ比例
Table 1 Binding energy position of each element and the ratio of O I and O II after XPS peak separation of different samples

Cr2p的XPS图谱如图3(c)所示,可以观察到结合能分别为576.5~577.2 eV和586.3~586.5 eV处Cr2p3/2和Cr2p1/2两个主峰,表明Cr在样品中以Cr3 的形式存在。Cr2p3/2轨道的结合能均高于纯Cr2O3的结合能(576 eV),说明掺杂样品中Cr原子取代了部分Al原子,Cr原子进入Al2O3晶格中[34]。
Al2p图谱如图3(d)所示,可知掺杂样品的Al2p轨道的结合能均低于纯α-Al2O3的结合能(74.0 eV),同样表明Cr原子成功进入Al2O3晶格中。
综合上述XRD和XPS分析结果,可推断Cr原子成功进入载氮体的晶格骨架中且分散较为均匀。Cr掺杂在一定程度上提高了载氮体的氧活性,这将有利于提高其氮化-氨化性能。
2.2 载氮体氮化-氨化反应活性
在不添加反应助剂(Y2O3、CaF2等)情况下,将所制得的不同浓度Cr掺杂载氮体用于氮化-氨化反应试验,进而判断不同浓度的Cr掺杂对铝基载氮体反应活性的影响,结果如图4所示。

图4 不同载氮体的氮化-氨化反应试验
Fig.4 Nitridation-amination reaction experiments of different nitrogen carriers
引入Cr原子后,随掺杂比例提高,载氮体总体合成氨性能先升高后缓慢降低。5种CA-x%载氮体氨收集量最后分别为0.55、1.28、1.62、1.52和1.48 mmol,对应的氨产率分别为0.53、1.23、1.56、1.46、1.42 mmol/(g·h);Cr掺杂量为Al原子数的5.0%时,NH3收集量最多,产率最高,约为未掺杂时的3倍。Cr掺杂首先提高了氮化反应的炭转化率x,CA-0%和CA-5.0%载氮体的炭转化率分别为42.0%和69.0%,显著提高了27个百分点,且炭转化率先升高后略微降低。另一方面,CA-0%和CA-5%载氮体氨化反应中氮化铝的反应率λ分别为62.2%和85.4%,提高了23.2个百分点。随着Cr掺杂量进一步提高,氮化铝反应率逐渐降低,这可能是由于Cr掺杂量提高后,氮化反应后载氮体中Cr—N键比例随之增多,而氮化铬相比氮化铝不易水解,从而降低了氨化反应效率。
对氮化、氨化反应前后CA-5.0%的载氮体样品进行XRD分析,判断其物相变化,并与氮化反应后的CA-0%样品进行对比,如图5所示。氮化反应前CA-5.0%载氮体样品的XRD谱峰为标准的α-Al2O3衍射峰,氮化反应后出现明显的AlN衍射峰,说明氮化反应确有AlN生成。对比CA-0%样品氮化后的XRD,AlN的衍射峰强度明显增强,表明5.0%的Cr掺杂有效促进了氮化反应的进行。此外,氨化反应后,AlN的衍射峰几乎全部消失,只留下α-Al2O3的衍射峰,无其他晶相衍射峰出现,表明循环后的载氮体样品物相并未发生明显变化。2种载氮体样品反应前的孔隙结构信息(平均值)见表2,可知CA-0%与CA-5.0%载氮体的比表面积、孔容和孔径基本一致,Cr掺杂并未影响铝基载氮体的孔隙结构,仅提高了其化学反应活性。
表2 新鲜CA-0%、CA-5.0%样品的孔隙信息
Table 2 Pore information of fresh CA-0% and CA-5.0% samples


图5 CA-5.0%载氮体反应前后的XRD谱图
Fig.5 XRD patterns of CA-5.0% nitrogen carrier before and after reaction
2.3 载氮体表面氮化过程的DFT计算
载氮体表面的氮化反应过程即为氧化铝的碳热还原氮化过程,根据文献报道,该过程可分为2个阶段:碳热还原阶段和氮化阶段[35-36]。为探究Cr掺杂对载氮体氮化反应性能的影响,分别对氧化铝表面碳热还原生成CO及N2吸附解离过程进行模拟计算,如图6所示,可知Cr掺杂对氮化反应的促进机理。

图6 载氮体表面CO生成、N2吸附结构示意
Fig.6 Structure diagram of CO formation and N2 adsorption on nitrogen carrier surface
未掺杂与Cr掺杂载氮体氮化反应的结构及能量变化如图7所示。从第1个CO的生成过程来看,Cr-Al2O3与C反应由初态到过渡态所需活化能为1.75 eV,相比未掺杂Al2O3的2.62 eV,该步反应的能垒降低了0.87 eV。且Cr-Al2O3与未掺杂Al2O3第1个CO生成整体所需的能量分别为0.42和-0.27 eV,整体反应的能量为正说明需要从外界吸收能量,为负则说明向外界放出能量。Cr-Al2O3表面再次脱离氧生成第二CO从初态到过渡态所需活化能为2.01 eV,该步反应的能垒相比未掺杂Al2O3的3.32 eV降低了1.31 eV,从反应物到过渡态的能量明显降低。同时,该步反应整体所需能量表现为-0.61 eV,相比未掺杂Al2O3的1.40 eV,较大幅降低了2.01 eV。对于载氮体表面脱离2个氧后N2吸附过程,Cr-Al2O3表面N2的吸附能为-0.55 eV,而未掺杂Al2O3表面N2的吸附能为-0.08 eV,表明Cr掺杂后N2更易吸附。最后,对于N2解离过程,N2分子在Cr-Al2O3表面解离过程由初态到过渡态所需活化能为1.80 eV,而在未掺杂Al2O3表面解离过程由初态到过渡态所需活化能为2.35 eV。此外,Cr-Al2O3表面N2解离整体所需能量为-3.31 eV,而未掺杂Al2O3的仅为-0.05 eV,大幅降低了3.26 eV。

图7 2种载氮体氮化反应的体系结构及能量
Fig.7 Structure and energy of nitridation reaction of two nitrogen carriers
综合可知,Cr掺杂首先降低了铝基载氮体的晶格稳定性,提高其表面的氧活性,使得其更易与炭反应生成CO,2个CO的生成步骤活化能均有一定程度降低,且Cr掺杂后的整体反应能量均为负值,其产物相比反应物更稳定。另外,Cr掺杂同样可促进N2的吸附与解离过程,在未掺杂Al2O3表面N2吸附能仅-0.08 eV,几乎无法吸附,Cr掺杂后N2吸附明显增强。N2在Cr-Al2O3解离过程的活化能同样更低,最明显的,N2解离后的产物能量大幅降低,表明Cr能有效促进氮化反应产物氮化铝的生成。
2.4 Cr掺杂载氮体的循环反应性能
采用CA-5.0%载氮体进行了10次循环氮化-氨化反应试验,以考察掺杂后的载氮体应用于化学链合成氨的稳定性,试验结果如图8所示。可知10次循环中,CA-5.0%载氮体的氮化-氨化反应性能基本保持稳定,氮化反应的炭转化率x在67%~72%,而氨化反应氮化铝的转化率λ在78%~86%,氨收集率s稳定在44%左右。这一结果表明,在短期循环内,CA-5.0%载氮体的氮化-氨化反应性能没有显著变化,说明其具有进行循环化学链合成氨的可行性。但另一方面,由于氨收集率较低,大量生成的NH3分解为N2和H2,导致最后总体收集的氨气量较少,这可能与试验时氨化反应温度较高有关,后续可进一步从抑制氨分解,提高氨收集率的角度展开研究。

图8 CA-5.0%载氮体的氮化-氨化循环试验
Fig.8 Nitridation-amination cycle experiment of CA-5.0% nitrogen carrier
CA-5.0%载氮体样品10次循环前后的整体结构和元素分布情况如图9所示。对比左侧SEM图可知,10次循环后CA-5.0%载氮体样品表面存在一定程度的烧结现象,其孔隙结构规整度下降,由原本相对均匀孔径演变为大小不一的复杂孔隙结构。对比右侧EDS图可知,Al、Cr和O元素三者分布区域重叠,表明Cr元素均匀分布在载氮体表面,且在循环后并未出现Cr元素聚集情况,进一步验证了Cr掺杂铝基载氮体的循环可行性。

图9 循环前后载氮体的表面形貌及元素分布
Fig.9 Surface morphology and element distribution of nitrogen carrier before and after cycling
新鲜CA-5.0%载氮体与10次循环后的载氮体样品的孔隙结构信息见表3。虽然SEM图表明载氮体表面存在烧结现象,但10次循环后CA-5.0%载氮体的平均比表面积由4.254 6 m2/g略增至5.460 3 m2/g,载氮体的孔容由0.007 663 cm3/g扩大至0.016 372 cm3/g,孔径由6.993 0 nm增长至11.290 6 nm,均提高了近1倍,表明10次循环后载氮体表面大孔增多,这可能是由于氮化-氨化反应过程中炭源的参与起到扩大孔隙结构的作用。
表3 新鲜CA-5.0%样品与10次循环后样品的孔隙信息
Table 3 Pore information of fresh CA-5.0% samples and samples after 10 cycles

3 结 论
1)采用共沉淀法制备了一系列Cr、Al物质的量比为x%(x=0、2.5、5.0、7.5、10.0)的载氮体样品用于化学链合成氨试验。所有载氮体样品的XRD谱图均呈现α-Al2O3衍射峰,说明Cr均匀掺杂进入Al2O3内部,进一步结合XPS谱图表明Cr掺杂可以提高铝基载氮体的氧活性。
2)在不添加反应助剂的情况下开展氮化-氨化反应试验,结果表明,CA-5.0%载氮体的反应活性最佳,相较未掺杂的载氮体,其最终NH3收集量提升约3倍。DFT计算结果表明,Cr掺杂可显著降低氮化反应过程各阶段的活化能及最终产物能量。
3)选择CA-5.0%载氮体进行10次合成氨循环试验,发现样品的反应活性较稳定。微观形貌分析表明样品未出现明显烧结现象且Cr元素并未聚集,具有循环反应的可行性。试验中发现氨分解较严重,后续可进一步从抑制氨分解的角度展开研究。
[1] ERISMAN Jan Willem, SUTTON Mark A, GALLOWAY James, et al. How a century of ammonia synthesis changed the world[J]. Nature Geoscience, 2008, 1(10): 636-639.
[2] 刘化章. 传统合成氨工业转型升级的几点思考[J]. 化工进展, 2015, 34(10): 3509-3520.
LIU Huazhang.Transformation-upgrading and energy-saving of ammonia synthesis industry[J]. Chemical Industry and Engineering Progress, 2015, 34(10): 3509-3520.
[3] 侯建国,单彤文,张超,等. 小型橇装天然气制氢技术现状与发展趋势分析[J]. 天然气化工(C1化学与化工), 2021, 46(3): 1-6.
HOU Jianguo, SHAN Tongwen, ZHANG Chao, et al. Current situation and development trend analysis of small skid mounted natural gas hydrogen production technology[J]. Natural Gas Chemical Industry, 2021, 46(3): 1-6.
[4] WU Ye, JIANG Guodong, ZHANG Hongbo, et al. Fe2O3, a cost effective and environmentally friendly catalyst for the generation of NH3-a future fuel-using a new Al2O3-looping based technology.[J]. Chemical Communications, 2017, 53(77): 10664-10667.
[5] BURROWS Laron, GAO Puxian, BOLLAS George M. Thermodynamic feasibility analysis of distributed chemical looping ammonia synthesis[J]. Chemical Engineering Journal, 2021, 426: 131421.
[6] GALVEZ M E, HALMANN M, STEINFELD A. Ammonia production via a two-step Al2O3/AlN thermochemical cycle. 1. Thermodynamic, environmental, and economic analyses[J]. Industrial &Engineering Chemistry Research, 2007, 46(7): 2042-2046.
[7] GALVEZ M E, FREI A, HALMANN M, et al. Ammonia produc-tion via a two-step Al2O3/AlN thermochemical cycle. 2. Kinetic analysis[J]. Industrial &Engineering Chemistry Research, 2007, 46(7): 2047-2053.
[8] GALVEZ M E, HISCHIER I, FREI A, et al. Ammonia production via a two-step Al2O3/AlN thermochemical cycle. 3. Influence of the carbon reducing agent and cyclability[J]. Industrial &Engineering Chemistry Research, 2008, 47(7): 2231-2237.
[9] FANG Jing, XIONG Chuhao, FENG Mingqian, et al. Utilization of carbon-based energy as raw material instead of fuel with low CO2 emissions: Energy analyses and process integration of chemical looping ammonia generation[J]. Applied Energy, 2022, 312: 118809.
[10] WANG Xiaoyu, SU Mingze, ZHAO Haibo. Process design and exergy cost analysis of a chemical looping ammonia generation system using AlN/Al2O3 as a nitrogen carrier[J]. Energy, 2021, 230: 120767.
[11] KUME Shoichi, YASUOKA Masaki, LEE Sang-Kee, et al. Dielectric and thermal properties of AlN ceramics[J]. Journal of the European Ceramic Society, 2006, 27(8): 2967-2971.
[12] WANG Qi, GE Yiyao, CUI Wei, et al. Carbothermal synthesis of micro-scale spherical aln granules with CaF2 additive[J]. Journal of Alloys and Compounds, 2016, 663: 823-828.
[13] ANDRÉ L Molisani, HÉLIO Goldenstein, HUMBERTO Yosh-imura N. Second-phase evolution and densification behavior of AIN with CaO-Y2O3-C multicomponent additive system[J]. Ceramics International, 2022, 48(5): 6615-6626.
[14] WANG Qi, GE Yiyao, KUANG Jianlei, et al. Effects of additives on the synthesis of spherical aluminum nitride granules by carbothermal reduction-nitridation process[J]. Journal of Alloys and Compounds, 2017, 696: 220-225.
[15] 王敬先. 添加剂对氧化铝的高温改性作用及改性后Pd/Al2O3的催化活性研究[D]. 上海:复旦大学, 2001.
[16] 刘勇. 碱土金属氧化物对氧化铝及其负载的单钯催化剂的高温热稳定性研究[D]. 上海:复旦大学, 2000.
[17] LIN Qingquan, QIAO Botao, HUANG Yanqiang, et al. La-doped Al2O3 supported Au nanoparticles: Highly active and selective catalysts for prox under pemfc operation conditions[J]. Chemical Communications, 2014, 50(21): 2721-2724.
[18] 刘晓军. 耐高温高比表面积活性氧化铝的制备与性能研究[D]. 沈阳:东北大学, 2009.
[19] BUSCA Guido. Structural, surface, and catalytic properties of aluminas[J]. Advances in Catalysis, 2014, 57: 319-404.
[20] YOSUKE Goto, ANGELA Daisley, JOANNA Hargreaves. Towar-ds anti-perovskite nitrides as potential nitrogen storage materials for chemical looping ammonia production: Reduction of Co3ZnN, Ni3ZnN, Co3InN and Ni3InN under hydrogen[J]. Catalysis Today, 2021, 364: 196-201.
[21] SAID Laassiri, CONSTANTINOS Zeinalipour-Yazdi, RICHARD Catlow. The potential of manganese nitride based materials as nitrogen transfer reagents for nitrogen chemical looping[J]. Applied Catalysis B: Environmental, 2018, 223: 60-66.
[22] MICHALSKY Ronald, AVRAM A M , PETERSON B A,et al. Chemical looping of metal nitride catalysts: Low-pressure ammonia synthesis for energy storage[J]. Chemical Science, 2015, 6(7): 3965-3974.
[23] MICHALSKY Ronald, PFROMM Peter H. Chromium as reactant for solar thermochemical synthesis of ammonia from steam, nitrogen, and biomass at atmospheric pressure[J]. Solar Energy, 2011, 85(11): 2642-2654.
[24] 王占考,许振华,郑洪,等. 单晶高温合金铬改性铝化物涂层的高温氧化行为研究[J]. 真空, 2015, 52(3): 1-5.
WANG Zhankao, XU Zhenhua, ZHENG Hong, et al. High temperature oxidation behavior of Cr modified aluminide coating on the single crystal superalloy[J]. Vacuum, 2015, 52(3): 1-5.
[25] FENG Mingqian, ZHANG Quan, WU Ye, et al. Using coal coke for N-sorption with an Al-based nitrogen carrier during chemical looping ammonia generation[J]. Energy &Fuels, 2020, 34(10): 12527-12534.
[26] XIONG Chuhao, WU Jin, JI Zhengang, et al. Unraveling the role of alkali metal in the biochar for enhancing the chemical looping ammonia generation efficiency[J]. Renewable Energy, 2024, 220: 119690.
[27] XIONG Chuhao, WU Ye, FENG Mingqian, et al. High thermal stability Si-Al based N-carrier for efficient and stable chemical looping ammonia generation[J]. Applied Energy, 2022, 323: 119519.
[28] GAO Yuan, WU Ye, ZHANG Quan, et al. N-desorption or NH3 generation of TiO2-loaded al-based nitrogen carrier during chemical looping ammonia generation technology[J]. International Journal of Hydrogen Energy, 2018, 43(34): 16589-16597.
[29] WU Ye, GAO Yuan, ZHANG Quan, et al. Promising zircon-ia-mixed Al-based nitrogen carriers for chemical looping of NH3: Reduced NH3 decomposition and improved NH3 yield[J]. Fuel, 2020, 264: 116821.
[30] CLARK Stewart J, SEGALL Matthew D, PICKARD Chris J, et al. First principles methods using CASTEP[J]. Zeitschrift Für Kristallographie-Crystalline Materials, 2005, 220(5/6): 567-570.
[31] ALI Ahmadi Peyghan, RASTEGAR F Somayeh, NASSER L Hadipour DFT study of NH3 adsorption on pristine, Ni- and Si-doped graphynes[J]. Physics Letters A, 2014, 378(30/31): 2184-2190.
[32] MATTISSON Tobias, LYNGFELT Anders, LEION Henrik. Ch-emical-looping with oxygen uncoupling for combustion of solid fuels[J]. International Journal of Greenhouse Gas Control, 2008, 3(1): 11-19.
[33] ROBERTS Mokone J, EVERSON Raymond C, GEORGE Domazetis, et al. Density functional theory molecular modelling and experimental particle kinetics for CO2 char gasification[J]. Carbon, 2015, 93: 295-314.
[34] JEAN Maria Fernandes, SURESH G, MUNIRAMAIAH Reddi-vari, et al. Effect of anionic bromine doping on the structural, optical and electrical properties of spray-pyrolyzed SnO2 thin films[J]. Materials Science &Engineering B, 2022, 282: 115756.
[35] ZHOU Zhiqiang, XU Youli, CHEN Xiumin, et al. Preparation of AlN under vacuum by the alumina carbothermal reduction nitridation method[J]. Ceramics International, 2020, 46(4): 4095-4103.
[36] XU Youli, ZHOU Zhiqiang, CHEN Xiumin, et al. Ultrafine aln synthesis by alumina carbothermal reduction under vacuum: Mechanism and experimental study[J]. Powder Technology, 2021, 377: 843-846.
Characteristics and mechanism of chemical looping ammonia generation by chromium-doped aluminum-based N-carrier

移动阅读