以1,2-丙二醇为循环剂的尿素醇解合成碳酸二甲酯催化反应精馏研究
0 引 言
在国家“双碳”战略大方向的指引下,碳酸酯产业将迎来新一轮的发展机遇。碳酸二甲酯(DMC)作为一种重要的绿色化学品,因其独特的化学和物理性质被广泛应用于各个领域,如可替代光气、硫酸二甲酯、氯甲烷及氯甲酸甲酯等有毒物质进行羰基化、甲基化及酯交换等反应[1-3],作为电解液的主要溶剂应用于电池领域。此外,由于其含氧量高、毒性低、生物降解性好,也是一种潜在的汽油添加剂[4]。在“双碳”背景下,锂电池作为清洁能源,其市场需求会进一步扩充,DMC的需求也会随之增加。
DMC的合成方法包括光气法[5]、酯交换法[6]、尿素醇解法[7]、甲醇与CO2直接合成法[8]和甲醇的氧化羰基化法[9]。其中,碳酸丙烯酯(PC)与甲醇的酯交换反应,因其DMC产率高、反应条件温和、设备投资小等优点而成为我国工业生产DMC的主要方法。然而,PC来源于石油,且在其生产过程中会伴生大量1,2-丙二醇(PG),导致原料利用率偏低,这与我国“富煤少油”的能源现状相悖。尿素醇解法根据反应历程不同可分为直接法和间接法[10],该方法的主要原料为煤炭,故大力发展尿素醇解合成DMC,既有利于节约化石燃料,又可为延伸我国传统煤化工产业链起到引领和示范作用。但直接法制备DMC,受热力学限制使得DMC收率较低;间接法虽DMC收率较高,但后续产物分离能耗大大增加[11]。
为了解决上述问题,笔者课题组于2004年提出了以脂肪族二元醇为循环剂的尿素醇解合成DMC的思路[12],包括以PG为循环剂的尿素醇解合成DMC的集成反应路线[13]。该过程不仅可以解决酯交换法中PG利用率低的问题,而且可以降低PC供应对石化行业的依赖。此外,反应中释放的氨气可被循环利用于与CO2反应生产尿素。然而,上述专利和后续大部分研究都只涉及其中一个或两个单独的反应[14-20]。WANG等[21]制备了ZnO-Y2O3催化剂用于催化尿素、乙二醇和甲醇两步法合成DMC的反应中,并考察了其对2个独立反应的催化性能。在第1步中,以尿素和乙二醇为原料合成PC,产物收率为94%;第2步,PC与甲醇酯交换生成DMC,DMC收率为71%。分步反应过程不可避免存在中间产物分离、操作复杂以及成本高等问题,多步反应的整合对于解决分离纯化操作问题具有重要意义[22]。笔者课题组以Ca-Zn-Al氧化物为催化剂,在配有垂刺分馏柱的四口烧瓶装置上实现了尿素、甲醇和PG“一锅法”制备DMC的反应过程,即先进行尿素与PG合成PC的反应,之后在不经产物分离和更换催化剂的情况下引入甲醇,主要进行PC和甲醇酯交换合成DMC的反应,DMC收率高达84.7%[13,23]。
为实现以PG为循环剂的尿素醇解合成DMC反应的连续化,便于反应过程中PG的循环,笔者拟在反应精馏装置上,先分别对Zn-Al氧化物催化尿素与PG合成PC及Ca-Al氧化物催化PC和甲醇酯交换合成DMC的2个反应进行考察;在此基础上,构建尿素和PG合成PC与PC和甲醇酯交换合成DMC的反应集成体系,建立以PG为循环剂的尿素醇解合成DMC的连续化新工艺,并考察反应条件的影响,以期改善尿素醇解合成DMC的反应效果。
1 试验部分
1.1 催化剂制备
采用共沉淀法制备Ca-Al和Zn-Al氧化物催化剂。以Ca-Al氧化物催化剂为例,制备过程如下:首先称取一定量硝酸钙和硝酸铝(n(Ca2 )∶n(Al3 )=1.5∶1.0),加入蒸馏水并搅拌均匀制备成溶液A;按比例称取一定量碳酸钠和氢氧化钠,加入蒸馏水并搅拌均匀制备成溶液B;搅拌条件下,将溶液A和B同时滴加到烧杯中,控制混合液的pH为9.5;滴加完毕,在40 ℃的水浴中老化24 h,再经过滤、洗涤、干燥后得到Ca-Al催化剂的前驱体粉末。
将制备好的Ca-Al催化剂前驱体粉末和田菁粉(助挤剂)以质量比20∶1混合均匀,加入质量分数4%的稀硝酸润湿后挤条成型,干燥后放入马弗炉中于950 ℃下焙烧4 h得到Ca-Al催化剂。
采用与Ca-Al催化剂类似的方法制备Zn-Al催化剂,其中,n(Zn2 )∶n(Al3 )=3∶1,焙烧温度为500 ℃。
1.2 反应操作过程
尿素与PG醇解合成PC反应、PC与甲醇酯交换合成DMC反应、以及以PG为循环剂的尿素醇解合成DMC反应均在催化精馏塔中进行。玻璃精馏塔的结构参数为:内径20 cm,高度150 cm。催化剂装填在精馏塔的中间,塔中除催化剂段外,其余位置装填直径3 mm的θ环不锈钢填料。
1.2.1 尿素与PG醇解合成PC反应
尿素与PG醇解反应的操作过程如下:采用催化剂与θ环混合装填方式(体积比为10∶1)在塔内装填Zn-Al催化剂,装填总体积为50 mL,用进料泵从催化剂段的上端通入尿素与PG的混合物,从塔釜通入N2,将副产的NH3带出塔。待反应稳定后,收集釜液进行定量分析。
1.2.2 PC与甲醇酯交换合成DMC反应
PC与甲醇酯交换合成DMC反应的操作过程如下:在塔内装填50 mL Ca-Al催化剂,甲醇和PC分别在催化剂装填段下端和上端进料,待反应稳定后,分别定时收集塔顶馏出液和釜液进行气相色谱分析。
1.2.3 以PG为循环剂的尿素醇解合成DMC反应
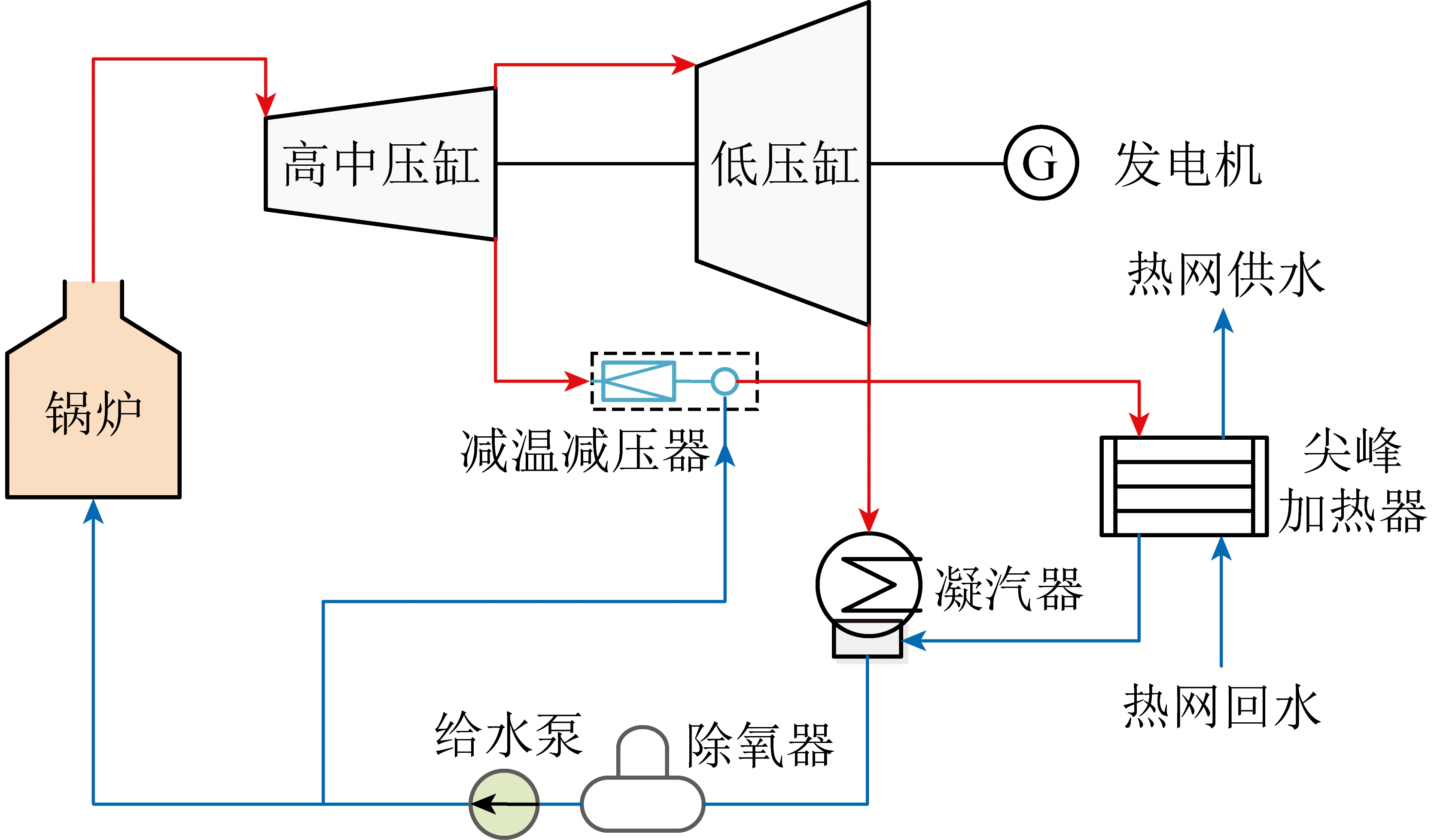
以PG为循环剂的尿素醇解合成DMC反应的操作过程如下:塔内催化剂段的上半部分和下半部分分别装填Ca-Al催化剂和Zn-Al催化剂,2者的装填量和装填方式与2个分步反应相同,从塔釜通入N2,将副产的NH3带出塔;先在Zn-Al催化剂段进行一段时间尿素与PG合成PC的反应,为塔釜提供一定量PC与PG混合液;然后,开始以PG为循环剂的尿素醇解合成DMC反应,利用进料泵实现原料尿素和甲醇混合液在2个催化剂段中间进料,同时利用另一台进料泵实现塔釜PC和PG混合液的循环,其进料位置为Ca-Al催化剂的上端,釜液循环过程中管路设有70 ℃保温措施,整个反应过程示意如图1所示。

图1 以PG为循环剂强化尿素醇解
合成DMC操作示意
Fig.1 Schematic diagram of urea alcoholysis to
DMC intensified by a circulating agent PG
1.3 产物分析
反应产物的定量分析在北京北分瑞利分析仪器(集团)有限责任公司生产的SP3420A型气相色谱仪上进行。采用PEG20M型色谱柱实现产物中各组分的分离。分析塔顶采出液时:柱温先在50 ℃下保持3 min,然后以15 ℃/min升至200 ℃;气化室和氢火焰检测器的温度均控制在180 ℃;利用正丙醇作为内标物进行定量。分析塔釜液时:柱温先在100 ℃下保持2 min,然后以10 ℃/min升至220 ℃,并保持10 min;气化室和氢火焰检测器的温度均控制在220 ℃;利用正丁醇作为内标物进行定量。
2 结果与讨论
2.1 尿素与PG醇解合成PC反应
2.1.1 反应温度的影响
反应温度对PC合成反应影响的考察结果如图2所示(反应条件:PG与尿素物质的量比为2,尿素与PG混合进料的液时空速为0.3 h-1,氮气速率为150 mL/min)。随着反应温度从150 ℃升至170 ℃,PC的收率逐渐升高,在170 ℃时取得最大值,此时PC收率为69.3%。反应温度较低时,由于尿素与PG的反应速率较慢,导致反应进行不充分,从而影响产物PC的收率;升温可以提高反应速率,而且尿素与PG合成PC为吸热反应,故升温有利于产物PC的生成[24]。继续提高反应温度至180 ℃,PC的收率由69.3%降为63.2%。反应温度过高,一方面会促进PG缩聚生成一缩二丙二醇等副反应的发生,同时也会加速尿素本身的分解,从而导致产物收率降低[24-25]。因此,确定适宜的反应温度为170 ℃。

图2 反应温度对PC合成反应的影响
Fig.2 Effect of reaction temperature on the
PC synthesis reaction
2.1.2 PG与尿素物质的量比的影响
PG与尿素物质的量比对PC合成反应影响的试验结果如图3所示(反应条件:尿素与PG混合进料的液时空速为0.3 h-1,氮气速率为150 mL/min,反应温度170 ℃)。在PG与尿素物质的量比为3时,PC收率为69.3%;随着2者物质的量比的增加,PC收率持续增加,当物质的量比为5时,PC收率为77.9%;继续提高PG与尿素物质的量比,PC收率基本保持不变。从资源节约的角度出发,选定PG与尿素适宜的物质的量比为5。

图3 PG与尿素物质的量比对PC合成反应的影响
Fig.3 Effect of molar ratio of PG/urea on the PC
synthesis reaction
2.1.3 进料液时空速的影响
尿素与PG混合进料的液时空速对PC收率影响的考察结果如图4所示(反应条件:PG与尿素进料的物质的量比为5,氮气速率为150 mL/min,反应温度为170 ℃)。伴随进料液时空速从0.3 h-1增加至0.6 h-1,PC收率从76.8%增至82.4%;继续提高进料的液时空速,产物PC收率下降明显。分析原因为进料液时空速较低时,尿素与PG在催化剂段的停留时间较长,容易加剧PG缩聚等副反应的发生;而进料液时空速过高,又会因为停留时间短,导致反应进行不充分,使得中间产物羟丙基氨基甲酸酯不能完全转化为PC[24],从而影响PC收率。因此,尿素与PG反应合成PC需要适宜的进料液时空速,现有条件下确定为0.6 h-1。

图4 进料液时空速对PC合成反应的影响
Fig.4 Effect of feed liquid hourly space velocity on the PC
synthesis reaction
2.1.4 氮气流速的影响
考察氮气流速对PC合成反应的影响,结果如图5所示(反应条件:PG与尿素进料的物质的量比为5,进料的液时空速为0.6 h-1,反应温度170 ℃)。在PC合成反应中,氮气流速由50 mL/min增加至150 mL/min过程中,PC收率一直呈增加趋势。氮气的作用在于及时将反应过程中生成的氨气带离反应体系,故随着氮气流速的逐渐增加,排氨效果逐渐改善,PC收率也随之增加;氮气速率为150 mL/min时,PC收率达到最高,为82.4%。然而氮气流速过高,虽然有利于氨气及时排出,但同时也会带来填料塔中雾沫夹带的问题,导致部分反应液无法与催化剂层有效接触,从而不利于PC合成反应的进行。因此,确定150 mL/min为PC合成反应中适宜的氮气流速。

图5 氮气流速对PC合成反应的影响
Fig.5 Effect of nitrogen flow rate on the PC synthesis reaction
2.2 PC与甲醇酯交换反应合成DMC反应
2.2.1 反应温度的影响
反应温度对PC与甲醇酯交换反应的影响如图6所示(反应条件:甲醇与PC物质的量比为12,PC进料的液时空速为0.051 h-1,回流比为9)。随着DMC合成过程中反应温度的不断提高,PC转化率和DMC收率均逐渐升高,然而,DMC的选择性基本保持不变。说明反应温度较低时,PC转化率和DMC收率较低主要是因为反应速率较慢所致。当反应温度为70 ℃时,PC转化率和DMC收率同时达到最大,分别为95.4%和90.6%。继续提高反应温度,反应效果基本保持不变,表现为PC转化率、DMC收率和选择性均基本不变。从节约能源角度出发,确定70 ℃为甲醇与PC酯交换合成DMC适宜的反应温度。

图6 反应温度对PC与甲醇酯交换反应的影响
Fig.6 Effect of reaction temperature on
transesterification of PC with methanol
2.2.2 回流比的影响
在常压下考察了回流比对PC与甲醇酯交换反应的影响,结果如图7所示(反应条件:甲醇与PC物质的量比为12,PC进料的液时空速为0.05 h-1,反应温度为70 ℃)。PC转化率和DMC收率随回流比的增大而逐渐升高,回流比为9时,PC转化率与DMC收率达到最高,分别为95.4%和90.6%。再继续增大回流比,DMC收率明显下降。这是因为酯交换法合成DMC是一个平衡限制反应,回流比较大时,大量含有DMC的液体流回塔内,使得DMC无法及时移出反应体系,从而抑制反应的正向进行。因此,选取适宜的回流比为9。

图7 回流比对PC与甲醇酯交换反应的影响
Fig.7 Effect of reflux ratio on transesterification of
PC with methanol
2.2.3 甲醇与PC物质的量比的影响
考察了甲醇与PC进料物质的量比对产物DMC收率的影响,结果如图8所示(反应条件:PC的进料液时空速0.05 h-1,回流比为9,反应温度为70 ℃)。由于反应生成的DMC与甲醇以共沸物的形式从塔顶蒸出,故试验中甲醇与PC的物质的量比较大。当甲醇与PC的物质的量比由10增加到14时,PC转化率与DMC收率均有较大提升;继续增加甲醇与PC的物质的量比,PC转化率与DMC收率变化不大。从反应平衡的角度来看,增加甲醇的量,有利于PC的转化和DMC的生成;但如果甲醇的量过大,则会增加塔釜的热负荷,同时增加后续分离能耗。综合考虑,选择甲醇与PC适宜的物质的量比为14,此时DMC收率为96.4%。

图8 甲醇与PC物质的量比对PC与甲醇酯交换反应的影响
Fig.8 Effect of molar ratio of methanol/PC on
transesterification of PC with methanol
2.2.4 PC的液时空速的影响
固定甲醇和PC的物质的量比,考察了进料流量的变化对PC与甲醇酯交换反应的影响,以PC的液时空速表示进料流量的大小,结果如图9所示(反应条件:回流比为9,进料中甲醇与PC的物质的量比为14,反应温度为70 ℃)。PC液时空速的增大,导致PC在催化剂层的停留时间变短,故其转化率逐渐下降。当PC液时空速增大至0.100 h-1时,DMC收率达到最大,为98.1%;此时PC转化率和DMC选择性分别为98.4%和99.7%。而当PC液时空速增加到0.150 h-1时,DMC收率显著下降,只有91.0%。当PC液时空速大于0.100 h-1,可能是由于反应物在催化剂上的停留时间过短,反应尚未达到平衡,从而导致PC转化率和DMC收率下降。因此,选定PC适宜的进料液时空速为0.1 h-1。

图9 PC液时空速对PC与甲醇酯交换反应的影响
Fig.9 Effect of liquid hourly space velocity on transesterification
of PC with methanol
2.3 以PG为循环剂的尿素醇解合成DMC反应
综合2个分步反应的适宜操作条件确定在反应精馏装置上进行以PG为循环剂的尿素醇解合成DMC反应的初始操作条件为:甲醇与尿素的物质的量比14∶1,甲醇与尿素混合液的进料液时空速0.6 h-1(以Zn-Al催化剂体积计),釜液循环的液时空速0.1 h-1(以Ca-Al催化剂体积计),氮气速率150 mL/min,回流比9,Zn-Al催化剂段温度170 ℃,Ca-Al催化剂段温度70 ℃。反应稳定后,DMC的收率为51.6%,此时循环液中的PC与PG的物质的量比稳定在1.0∶4.1左右。在此基础上,重点考察了原料甲醇和尿素的物质的量比以及进料流速对反应效果的影响。
2.3.1 甲醇与尿素物质的量比的影响
甲醇与尿素物质的量比对DMC收率的影响结果如图10所示(反应条件:甲醇与尿素混合液的进料液时空速0.6 h-1,釜液循环的液时空速0.1 h-1,氮气速率150 mL/min,回流比9,Zn-Al催化剂段温度170 ℃,Ca-Al催化剂段温度70 ℃)。由图10可知,甲醇与尿素物质的量比为14时,DMC收率为51.6%。增加甲醇与尿素的物质的量比,DMC收率随之升高。当甲醇与尿素物质的量比增至17时,DMC收率可达56.7%。继续增加甲醇与尿素的物质的量比,DMC收率基本保持不变。故选定甲醇与尿素进料适宜的混合物质的量比为17。

图10 甲醇与尿素物质的量比对以PG为循环剂
强化尿素醇解合成DMC的影响
Fig.10 Effect of molar ratio of methanol/urea on
urea alcoholysis to DMC intensified by PG
2.3.2 甲醇与尿素混合进料液时空速的影响
固定釜液循环的液时空速为0.1 h-1,改变尿素与甲醇混合液的进料流速,考察其液时空速对DMC合成反应的影响,结果如图11所示(反应条件:甲醇与尿素的物质的量比17,釜液循环的液时空速0.1 h-1,氮气速率150 mL/min,回流比9,Zn-Al催化剂段温度170 ℃,Ca-Al催化剂段温度70 ℃)。甲醇与尿素混合进料液时空速为0.4 h-1时,DMC收率为57.9%。随着进料液时空速增加到0.5 h-1,DMC收率达到最高值58.2%。然而,随着进料液时空速的进一步增大,原料在催化剂装填段停留时间变短,导致未进行充分反应便离开催化剂层,从而导致DMC收率下降。故选定甲醇与尿素混合进料适宜的液时空速为0.5 h-1。

图11 液时空速对以PG为循环剂强化尿素
醇解合成DMC的影响
Fig.11 Effect of liquid hourly space velocity on
urea alcoholysis to DMC intensified by PG
在以PG为循环剂的尿素醇解合成DMC的反应过程中,DMC收率最高为58.2%。尽管与在催化精馏装置上进行酯交换法合成DMC反应结果无法相提并论,然而本文是在同一装置上进行尿素和PG合成PC与酯交换法合成DMC的反应集成,从而实现以PG为循环剂的尿素醇解合成DMC的新反应工艺,在这一反应过程中,除尿素和甲醇外不再补充其他原料(图1),相当于与尿素直接醇解合成DMC工艺的原料相同。从文献[26-27]中给出的ZnO和ZnO-CeO2催化尿素直接醇解合成DMC研究结果可知,产物的收率最高在28.9%~30.0%,而且反应温度为190 ℃。对比可知,采用PG为循环剂促进了尿素醇解合成DMC的反应过程,无论是反应结果还是反应条件,均有明显优势。
3 结 论
1)在催化精馏塔中,对以PG为循环剂的尿素醇解合成DMC的2个分步反应——尿素与PG反应合成PC和PC与甲醇酯交换合成DMC的研究,确定了各自适宜的操作条件,PC和DMC收率最高分别为82.4%和98.1%;同时也可为构建以PG为循环剂的尿素醇解合成DMC的操作条件提供参考。
2)在催化精馏塔中分段装填Zn-Al与Ca-Al催化剂,实现了以PG为循环剂、尿素与甲醇为原料合成DMC的连续化新工艺。在甲醇与尿素物质的量比为17、甲醇与尿素混合液的进料液时空速0.6 h-1、釜液循环的液时空速0.1 h-1、氮气速率150 mL/min、回流比9、Zn-Al催化剂段温度170 ℃和Ca-Al催化剂段温度70 ℃的条件下,DMC收率达58.2%,明显优于尿素直接醇解制DMC的文献值。
[1] ONO Y. Catalysis in the production and reaction of DMC,an environmentally benign building block[J]. Applied Catalysis A:General,1997,155(2):133-166.
[2] TIAN J,WANG J,CHEN J,et al. One-pot synthesis of dimethyl carbonate catalyzed by n-Bu4NBr/n-Bu3N from methanol,epoxides,and supercritical CO2[J]. Applied Catalysis A:General,2006,301(2):215-221.
[3] DING X,DONG X,KUANG D,et al. Highly efficient catalyst PdCl2-CuCl2-KOAc/AC@Al2O3 for gas-phase oxidative carbonylation of methanol to dimethyl carbonate:Preparation and reaction mechanism[J]. Chemical Engineering Journal,2014,240:221-227.
[4] PACHECO M A,MARSHALL C L. Review of dimethyl carbonate (DMC) manufacture and its characteristics as a fuel additive[J]. Energy & Fuels,1997,11(1):2-29.
[5] BABAD H,ZEILER A G. Chemistry of phosgene[J]. Chemical Reviews,1973,73(1):75-91.
[6] DURANLEAU R G,NIEH E C Y,KNIFTON J F. Process for production of ethylene glycol and dimethyl carbonate:US4691041A [P]. 1987-09-01.
[7] SALEH R Y,MICHAELSON R C,SUCIU E N,et al. Process for manufacturing dialkyl carbonate from urea and alcohol:US 5565603A[P]. 1996-10-15.
[8] CHOI J C,HE L N,YASUDA H,et al. Selective and high yield synthesis of dimethyl carbonate directly from carbon dioxide and methanol[J]. Green Chemistry,2002,4(3):230-234.
[9] ROMANO U,TESEL R,MAURI M M,et al. Synthesis of dimethyl carbonate from methanol,carbon monoxide,and oxygen catalyzed by copper compounds[J]. Industrial & Engineering Chemistry Product Research & Development,1980,19(3):396-403.
[10] 叶少春. 碳酸二甲酯合成工艺发展状况研究[J]. 中国盐业,2020(17):30-33.
YE Shaochun. Research on the development status of dimethyl carbonate synthesis technology[J]. China National Salt Industry,2020(17):30-33.
[11] 王锦玉,张宗飞,刘佳,等. 碳酸二甲酯的生产技术及市场分析[J]. 化肥设计,2021,59(5):1-5,45.
WANG Jinyu,ZHANG Zongfei,LIU Jia,et al. Production technologies and analysis of dimethyl carbonate[J]. Chemical Fertilizer Design,2021,59(5):1-5,45.
[12] 赵新强,张艳,陈英,等. 以脂肪族二元醇为循环剂的尿素醇解合成碳酸二甲酯方法:CN1569810A[P]. 2004-05-08.
[13] AN H,ZHANG G,ZHAO X,et al. Preparation of highly stable Ca-Zn-Al oxide catalyst and its catalytic performance for one-pot synthesis of dimethyl carbonate[J]. Catalysis Today,2018,316:185-192.
[14] GAO Z,WANG S,XIA C. Synthesis of propylene carbonate from urea and 1,2-propanediol[J]. Chinese Chemical Letters,2009,20(2):131-135.
[15] WU D,GUO Y,SHU G,et al. Synthesis of propylene carbonate from urea and 1,2-propylene glycol in a monolithic stirrer reactor[J]. Advances in Fine Petrochemicals,2013,52(3):1216-1223.
[16] ZHAO X,JIA Z,WANG Y. Clean synthesis of propylene carbonate from urea and 1,2-propylene glycol over zinc-iron double oxide catalyst[J]. Journal of Chemical Technology & Biotechnology Biotechnology,2010,81(5):794-798.
[17] LI Q,NING Z,WEI W,et al. Catalytic performance of metal oxides for the synthesis of propylene carbonate from urea and 1,2-propanediol[J]. Journal of Molecular Catalysis A:Chemical,2007,270(1/2):44-49.
[18] 王慧,刘水刚,张文郁,等. 高稳定性CaO-ZrO2固体碱催化剂的表征和催化性能[J]. 化学学报,2006,64(24):2409-2413.
WANG Hui,LIU Shuigang,ZHANG Wenyu,et al. Characterization and catalytic properties of highly stable CaO-ZrO2 Catalysts[J]. Acta Chimica Sinica,2006,64(24):2409-2413.
[19] KUMAR P,SRIVASTAVA V C,MISSHRA I M. Synthesis and characterization of Ce-La oxides for the formation of dimethyl carbonate by transesterification of propylene carbonate[J]. Catalysis Communications,2015,60:27-31.
[20] HOLTBRUEGGE J,LEIMBRINK M,LUTZE P,et al. Synthesis of dimethyl carbonate and propylene glycol by transesterification of propylene carbonate with methanol:Catalyst screening,chemical equilibrium and reaction kinetics[J]. Chemical Engineering Science,2013,104:347-360.
[21] WANG P,LIU S,ZHOU F,et al. Two-step synthesis of dimethyl carbonate from urea,ethylene glycol and methanol using acid-base bifunctional zinc-yttrium oxides[J]. Fuel Processing Technology,2014,126:359-365.
[22] 王延吉,胡洁,薛伟,等. 催化反应过程绿色集成系统[J]. 化工学报,2007,58(11):2689-2696.
WANG Yanji,HU Jie,XUE Wei,et al. Green integrated system of catalytic reaction[J]. CIESC Journal,2007,58(11):2689-2696.
[23] ZHANG G,AN H,ZHAO X,et al. Preparation of Ca-Zn-Al oxides and their catalytic performance in the one-pot synthesis of dimethyl carbonate from urea,1,2-propylene glycol,and meth-anol[J]. Industrial & Engineering Chemistry Research,2015,54(13):3515-3523.
[24] AN H,MA Y,ZHAO X,et al. Preparation of Zn-Al oxide catalyst and its catalytic performance inpropylene carbonate synthesis from urea and propylene glycol on a fixed-bed reactor[J]. Catalysis Today,2016,264:136-143.
[25] 张光洁. 尿素、1,2-丙二醇和甲醇“一锅法”合成碳酸二甲酯反应研究[D]. 天津:河北工业大学,2015.
[26] WANG M,ZHAO N,WEI W,et al. Synthesis of dimethyl carbonate from urea and methanol over ZnO[J]. Industrial & Engineering Chemistry Research,2005,44(19):7596-7599.
[27] JOE W,LEE H J,HONG U,et al. Synthesis of dimethyl carbonate from urea and methanol over ZnO(X)-CeO2(1-X) catalysts prepared by a sol-gel method[J]. Journal of Industrial and Engineering Chemistry,2012,18(3):1018-1022.
Synthesis of dimethyl carbonate by urea alcoholysis using propylene glycol as a circulating agent in a reactive distillation column

AN Hualiang,QU Yaqi,LIU Zhen,et al.Synthesis of dimethyl carbonate by urea alcoholysis using propylene glycol as a circulating agent in a reactive distillation column[J].Clean Coal Technology,2022,28(1):122-128.