碳中和
双碳目标下以煤炭为基础的氨合成与清洁利用的未来与挑战
0 引 言
氨是关系国计民生的化工原料,也是一种潜在的零碳能源。从1908年哈伯提出Haber-Bosch法合成氨以来,一个多世纪的氨化工对人类生产生活产生巨大影响,氨从生产到储存运输已形成较完备产业链。目前,全球每年生产1.8亿t氨,其中约70%用于氮肥生产[1]。其次,氨被许多大型工业系统用作制冷剂,制冷量大,对臭氧层无破坏且泄漏易发现。此外,在制造炸药、硝酸及大部分有机材料如纤维、塑料、染料、尿素等过程中也涉及氨。近年来,氨富氢无碳的性质,使氨能源化利用备受关注。作为储能介质,氨具有能量密度高、无碳排放、安全性高等优点。加拿大研究人员分析了氨作为汽车发动机燃料的经济性[2],并将其与其他常规燃料(汽油、天然气、液化石油气、甲醇)及氢气进行对比。结果表明,氨是所有研究对象中最经济的燃料。氨还可作为发动机和空调的制冷剂,进一步降低成本。VALERA-MEDINA等[3]综述了氨作为潜在燃料的最新研究及未来展望,从生产、分配、利用、安全、法律及经济等方面对氨作为燃料的可行性进行全面剖析,并预测氨将在未来成为主要的能源参与者。在我国,随着“碳达峰、碳中和”目标提出,《高耗能行业重点领域节能降碳改造升级实施指南(2022年版)》《“十四五”新型储能发展实施方案》等政策相继推出,氨作为一种绿色无碳能源展现出巨大发展潜力。
笔者论述了双碳目标下,以煤炭为基础的氨化工技术,包括氨合成、氨燃烧及氨利用等方面的研究进展。氨合成方面概述了传统哈伯法合成氨工艺的发展历程,总结了近年来新型合成氨技术的发展,包括化学链技术、可再生能源驱动的光催化、电催化及等离子体技术等。介绍了氨作为燃料在能源化利用方面的研究,包括掺混燃烧、催化燃烧、化学链燃烧等。最后,综述了氨作为化工原料在氨制氢、氨法碳捕集以及氨法脱硫脱硝方面的研究进展,以期为未来清洁高效的氨化工提供参考。
1 合成氨工艺
1911年,BOSCH设计完成世界上第1台高压合成氨反应器,至今已有一百多年历史,是催化合成氨历史的里程碑,采用的合成氨方法由犹太人FRITZ Haber发明,并沿用至今。
19世纪前,科学家指出为获取足够多的粮食,必须实现大气固氮。因此,合成氨成为20世纪初研究课题,HABER首先发现N2和H2在1 020 ℃常压条件下便可合成少量氨,启发其通过热力学计算得到合成氨最优反应条件。经不断计算和试验,HABER在600 ℃、20 MPa并以锇为催化剂的条件下,合成氨产率达8%,并在1911年成功制造了第1台合成氨反应器;1913年,世界上第1台合成氨装置投产,日产氨量5 t,此后,合成氨工业迅速发展,不仅解决了人口增长带来的粮食需求问题,还带动了许多化工产品的发展。
近年来,随着氨的无碳富氢属性被发掘,各国再次将氨研究作为一项战略目标。关于氨合成,澳大利亚正利用自身光伏和天然气资源丰富的优势,将电解水制取的绿氢和天然气制取的蓝氢液化成氨,运输到日本、韩国等主要需求地。沙特阿拉伯的NEOM绿氢公司也考虑将绿氢合成零碳排放的绿氨,并由空气产品公司出口至全球市场。目前项目的工程设计和采购工作已正式启动,预计工厂将于2026年投产。近日,我国大安风光制绿氢合成氨一体化示范项目已在吉林西部大安清洁能源化工产业园启动。该项目总投资63.32亿元,规划建设700 MW风电项目、100 MW光伏项目、配套建设40 MW/80 MW时储能装置,同时还将新建制氢、储氢及18万t合成氨装置。尽管氨已发展一个世纪,目前仅Haber-Bosch法合成氨满足工业生产条件。
1.1 Haber-Bosch法合成氨
1.1.1 合成氨催化剂
20世纪初,世界上第1座以Haber-Bosch法为基础的合成氨装置正式开工,主要工序与现今无太大差异:首先将煤等固体燃料和烃类加热,并与水蒸气反应形成以CO和H2为主的水煤气,并在生产过程中通入适量空气,其中O2被燃烧消耗生成CO并放出热量,留下的N2与水煤气组成原料气;将原料气中CO转变为CO2,再进行净化,脱除原料气中硫与CO2,最后压缩得到氨合成所需净化合成气,并送入氨合成塔进行催化反应。由于当时这一过程产率仅8%,进一步提高合成氨效率的关键在于找到合适的氨合成催化剂。HABER、BOSCH为此对2 500种催化剂进行了6 500次试验,最终选择了含助剂的铁基催化剂。自Haber-Bosch法出现以来,催化剂研究从未中断,20世纪80年代,英国BP公司发明了钌基催化剂[4],刘化章等[5]研发了Fe1-xO基催化剂。目前Haber-Bosch法合成氨催化剂基本以Fe3O4催化剂体系、Ru催化剂体系以及Fe1-xO催化剂体系3条路线发展。
随着人们对合成氨机理认识不断加深,催化剂研究不断深入。多相催化能提高化学反应速率,对所需产物具有选择性,在化工产业中发挥重要作用[6]。Haber-Bosch法合成氨领域,针对大部分元素的多相催化合成氨活性研究较多,发现过渡金属的合成氨活性呈典型的火山型曲线[7],其表面N的吸附能EN与N2解离吸附能垒EN-N及NHx物种吸附能之间的线性关系如图1所示(r为反应速率,F为转化频率)。由图1可知,VIII族元素Fe和Ru等位于火山型曲线顶端附近,具有适中的解离吸附能,催化合成氨活性良好。含多种助剂的熔铁催化剂在目前工业应用最广泛。

图1 合成氨反应中过渡金属的火山型曲线[7]
Fig.1 Volcano plot in transition metal-catalyzed ammonia synthesis[7]
传统Fe基催化剂具有活性高、寿命长和成本较低等优点,但是在高浓度NH3下反应率会下降,其活性受到严重影响,且仍然需要苛刻的反应条件(15~25 MPa,400~500 ℃)[8]。Ru基催化剂具有高活性、高氨浓度以及宽H2/N2范围等特点[4],可以在低温低压条件下操作,被视为温和条件下氨合成最有希望的催化剂之一[9]。HATTORI等[10]采用钙结合氢和氟并与钌(Ru)纳米颗粒组成复合材料(Ru/CaFH),在低于50 ℃下成功合成氨。在接近室温条件下,氢原子从CaFH中逸出,而CaFH则会向Ru强力提供电子,N2与该状态下的Ru接触后,立即分解为N原子。在Ru表面,H2分解生成H原子,氮原子与氢原子直接反应生成氨。WANG等[11]开发了一种碱(土)金属钌基三元氢化物催化剂材料,通过在氮还原活性金属中添加新的活性位点,利用负氢作为质子和电子载体以及碱金属/碱土金属阳离子中间物种的稳定作用,实现了温和条件下氨的催化合成。LI等[12]通过控制前驱体类型和负载量制备了一系列不同粒子尺度的Ru基催化剂,包括单原子催化剂、原子团簇催化剂、亚纳米簇催化剂、纳米颗粒催化剂。发现Ru粒子尺寸降至亚纳米范围,氨合成速率急剧增加。通过调节Ru粒子尺寸,实现了较温和条件下合成氨。此外,福州大学于2017年和2019年陆续开发的年产3万t和20万t“铁钌接力”低温低压合成氨装置,已经平稳运行超过4 a,后者为国际首套以煤为原料的装置,且涉及的Ru基催化剂有望进一步应用于可再生能源绿色合成氨。
为满足新时代节能降耗工艺要求,各种温和条件下的合成氨催化剂相继提出,目前铁基催化剂工业应用最广泛,钌基催化剂逐渐成熟,部分低温低压催化剂已进入产业化试用阶段,其他种类催化剂也在实验室取得较好结果。未来进一步优化催化剂性能、降低合成氨压力,如仿照生物固氮等,实现常温常压下高效合成氨,将是固氮技术最终突破。
1.1.2 化石燃料合成氨工艺
除单程转化率较低外,传统Haber-Bosch法合成氨的潜在问题是需化石能源作为基础。我国富煤少气,煤炭是合成氨工业的主要原料[13-15]。对于我国目前煤基氨生产,主要技术路线有2种[16]:① 采用传统技术,以无烟煤为原料,流程包括固定床间歇煤气化、双核磺化酞菁化合物(PDS)脱硫、中低温变换、热钾碱脱碳及铜氨液精制等(图2路线1);② 采用先进技术,以水煤浆或干粉煤为原料,流程包括气流床加压气化、宽温变换、甲醇洗、液氮洗精制等(图2路线2)。据统计,2021年全国合成氨产能合计为6 488万t/a,其中采用先进煤气化技术的产能为3 284万t/a[17]。

图2 我国煤基氨生产技术路线[16]
Fig.2 Technical route of coal-based ammonia production
in China[16]
1935年,我国首次引进以焦炭为原料的常压固定床间歇煤气化技术用于生产氨[18]。随着经验积累及技术发展,气化炉生产规模不断提高,并于20世纪七八十年代成功开发了以无烟块煤(煤棒、煤球)为原料的固定床间歇煤气化工艺,在全国推广,并沿用至今[19-20]。然而,该工艺存在明显劣势:使用原料单一价格高,生产流程能耗高、成本高,无组织废气排放量大,造成污染[20]。因此,2018年以来,国家部门及各省政府出台一系列政策要求限制或淘汰一批固定床间歇式煤气化工艺设备,鼓励发展更节能环保型的煤气化工艺[21]。先进的水煤浆加压气化技术于20世纪90年代被我国引进,目前是工业制氨中广泛采用的洁净煤气化技术之一[22]。该技术以来源广泛的煤粉代替无烟煤作为原料,具有进料灵活、焦油含量低、燃料转化率高等优点,适用于灰熔融温度较低的原材料[23]。
20世纪50年代,天然气开始作为制氨原料投入使用,得益于天然气合成氨设备投资成本低、能耗小等优势,国外大部分合成氨厂均以天然气取代煤炭作为原料,而国内在20世纪70年代才逐渐采用天然气合成氨,由于煤储量远高于天然气,煤制氨仍受到重视[24]。2种方法的主要区别在于原料气制备不同,天然气合成氨首先将天然气脱硫,利用蒸汽与压缩空气进行二次转化,再进行CO变换与CO2脱除等工序[25]。“十一五”期间,为达到节能降耗要求,以天然气为原料的合成氨推广了一段炉烟气余热回收技术,并进行蒸汽系统改造。近年来,天然气重整制氢技术不断改进,除传统天然气蒸汽重整外,逐渐开发了低温蒸汽重整、低温等离子体重整等技术[26]。
先进煤气化、天然气重整制氨工艺主要通过改良原料、反应炉,加强余热回收等方式优化整个合成氨工艺,无法避开以化石燃料生产H2过程中CO2排放。因此,为满足国家双碳政策要求,以可再生能源电解水制氢,为合成氨提供绿色原料,再通过Haber-Bosch合成氨成为目前最切实可行的方案。
1.1.3 可再生能源制氢—Haber-Bosch合成氨
近年来,新能源领域得到快速发展,也为Haber-Bosch法合成氨工艺带来新机遇。利用风电、光电等可再生能源电解水制氢,不仅可减少化石燃料使用,降低CO2排放,还可缓解可再生能源电力消耗过程中产生的弃风、弃光问题。SMITH等[27]证明利用可再生能源电解水制氢并驱动Haber-Bosch法合成氨在技术上可行,关键在于提高产氢效率和开发小规模、分布式和灵活流程。高阳等[28]对我国浙江沿海地区可再生能源制氢成本进行分析,结果表明采用风电、光伏制氢成本分别为34.18~36.56元/kg和41.07~42.82元/kg,同时指出光伏结合谷电制氢具有较好的经济性。李志军等[29]分析了可再生能源转化为氨氢能源体系的经济可行性,结果表明采用可再生能源制绿氨 氨运输体系 分布式氨裂解制氢,电价为0.1元/kWh,每千克H2利润可达近50%,利用可再生能源弃水、弃风、弃光先天优势,合成氨生产成本优于传统方式。以可再生能源电解水制氢,再通过Haber-Bosch合成氨,组建可再生能源、氢能、氨能等多种清洁能源体系,是促进我国能源结构转型的重要手段。另外,该方式无需对传统的合成氨工厂进行大改造,原合成氨设备可继续使用,因此,该技术可行性很高,是可预见阶段中最有可能规模化应用的绿色合成氨工艺技术。
国内外对于可再生能源制氢—Haber-Bosch合成氨研究很早。荷兰凭借其丰富的可再生资源正大力推广绿色合成氨工艺,说明通过海上太阳能与风能进行氨合成可行,且随电价降低,通过海上可再生能源电解水合成氨的成本比天然气更低。目前,荷兰能源公司(NUON)、天然气公司(Gasunie)及挪威石油公司(Statoil)等多家大型企业均参与布局,并制定了未来战略目标[30]。日本可再生能源研究所建造了一座50 kW风光电合成氨示范基地;同时,还在积极筹备从澳大利亚进口可再生氨港口的建设。澳大利亚方面则完成了利用澳洲沙漠的太阳能生产氨燃料并出口日本的技术方案和协作战略的论证工作;国际大型氨生产商雅拉正计划在澳大利亚西部皮尔巴拉建造一座太阳能生产氨气的示范工厂[31]。我国大安风光项目,利用吉林省优质的风、光资源,以绿电生产绿氢,以绿氢生产绿氨,形成电-氢-氨的全产业链,不仅可将弃电化废为宝加以利用,还可为化工工艺提供新的氢源获取途径。2021年立项的国家重点研发计划“氢能技术”重点专项项目中,清华四川能源互联网研究院牵头了“十万吨可再生能源电解水制氢合成氨示范工程”项目,计划仅采用电力作为绿色合成氨的生产原料,助力国家早日实现碳中和。该项目对国家可再生电力创新应用及传统化工行业转型具有重要意义。
各国对于绿氢的布局空前加快,但总体各国可再生能源制氢—Haber-Bosch合成氨项目较小或处于启动阶段,由于可再生能源电力电量存在波动性,难以适配合成氨过程的平稳需求,大规模的可再生能源制氢—Haber-Bosch合成氨系统运行仍存在诸多挑战:首先需优化合成氨工艺,建立柔性调节技术平滑或适配大多数可再生能源的间歇性;同时建立“源-网-氢-氨”耦合系统的动态协同控制技术,完善市场运营机制;此外,电解水效率对氨生产成本影响较大,目前电解水制氢工艺主要有碱性电解(AEL)、质子交换膜(PEM)和固体氧化物电解(SOEC)工艺,碱性电解水制氢是传统工艺,应用较广,后2种技术目前成熟度较低,尚无大规模应用,但有望在将来显著降低可再生能源制氢合成氨的成本。
1.2 化学链合成氨
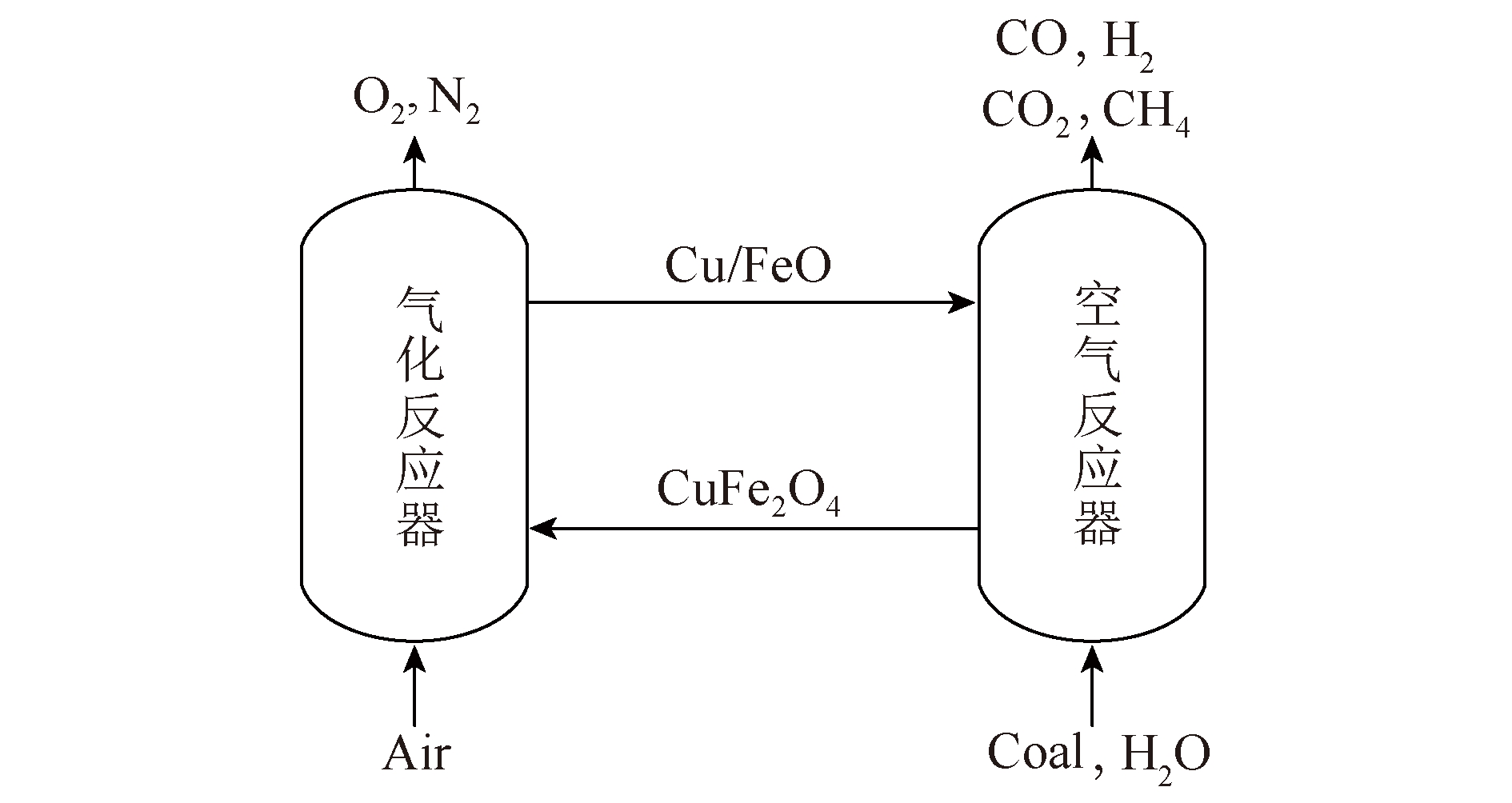
考虑到Haber-Bosch合成氨工艺本身能耗较高、转化率低(10%~15%)[32],探索一种可持续、低能耗且环保的氨合成技术一直是研究目标。近年来,化学链技术因其能源效率、产物的选择和分离等优势得以迅速发展[33]。如化学链燃烧技术具有高燃烧效率、CO2内分离、成本低、几乎不产生NOx等优点。化学链技术的基本原理是将原本的化学反应借助载氧体或载氮体等作用分解为2个或多个反应,各反应可在不同时间、不同容器中进行(图3)。该方法不仅可避免传统氨合成方法中的热力学与动力学的矛盾,还可对各反应单独优化从而提高总反应效率。

图3 化学链合成氨示意
Fig.3 Schematic diagram of chemical looping synthetic ammonia
1.2.1 Haber-Bosch式化学链合成氨
Haber-Bosch式化学链合成氨将传统合成氨过程分解为载氮体氮化和氨化2个过程,通常通过金属氮化物或亚氨基化合物实现。
MICHALSKY等[34]比较几种不同金属氮化物的氮化以及氨化反应性能,发现Cr2N易继续氮化生成CrN,但其加氢氨化反应较困难;而Fe氮化反应困难但氨化较简单。与之相比,Mn4N的氮化及氨化反应热力学均适中,更有利于总体反应进行。以氮化锰为载氮体进行研究,发现载氮体的设计重点在于破坏晶格氮的稳定性;利用电子结构理论发现,通过掺杂过渡金属,载氮体中晶格氮的稳定性可增加或降低至理想值。与未掺杂相比,Fe掺杂增加了氮化锰中氮空位的浓度,有效降低了晶格氮的稳定性。WANG等[35]发现Mn基载氮体在N2还原中表现更好,而Fe基载氮体更易与H2反应释放NH3。因此,将锰和铁氮化物结合负载在氧化铝上,发现混合后的载氮体均表现出较高的反应性能(图4)。

图4 Mn、Fe及其复合载氮体的氮化能力比较[35]
Fig.4 Comparison of nitrogen absorption capacity of Mn,Fe and its compound nitrogen carriers[35]
为研究渗氮过程,AFRAMEHR等[36]开展大量研究工作,将Mn中吸收的N总结为3种:与Mn强键合的原子N、通过共价或离子杂化键结合的原子N、存在于Mn晶格缺陷中的N;其中第1种氮原子难以分离产生NH3,第2种为氨化过程中NH3的主要来源,而缺陷中的氮则可以通过现有氮化物向体相内扩散,一旦遇到可用金属Mn,就会转化为氮化物。
GAO等[37]以碱金属和碱土金属亚氨基化合物为氮载体,通过碱金属或碱土金属氢化物还原N2来固定氮,形成亚氨基化合物,亚氨基化合物氢化以产生氨并再生金属氢化物。热力学计算表明,LiH、BaH2氮化生成相应亚氨基化合物或氮化物的反应易进行。NaH和KH无法形成稳定的亚氨基化合物因而无法实现氮化过程。MgH2、BaH2则因其亚氨基化合物或氮化物反应性能较差难以实现氨化过程。其热力学可行性关系为LiH/Li2NH ≈ BaH2/BaNH > CaH2/CaNH >MgH2/MgNH(Mg3N2)。通过试验验证了LiH、BaH2分别在400、250 ℃可完成氮化反应,而Li2NH、BaNH在300、200 ℃以上时可实现氨化反应。同时研究发现,3d过渡金属如Fe、Co和Ni对氨化反应有一定促进作用,且与热催化反应相反,Ni和Co的催化性能优于Fe。最近,YAN等[38]发现虽然钯(Pd)无法促进氮的活化,但Pd与氢化锂(LiH)反应形成钯氢化锂,如LiPdH0.7和Li2PdH2,Pd的存在可促进氢化锂对N2的固定和加氢氨化反应。结果表明,引入Pd后,在300 ℃和0.1 MPa条件下,氨产量为693 μmol/(g·h),为350 ℃、0.1 MPa时纯LiH/Li2NH氨产量的7倍。
Mn和Li具有较好的合成氨性能,LAASSIRI等[39]探索了掺杂后Mn材料A-Mn-N(A=Fe、Co、K和Li)的合成氨潜力,发现掺杂Li的氮化锰在400 ℃表现出较高的反应活性。FENG等[40]设计了一种氮化锰和碱金属或碱土金属酰亚胺(Li2NH或BaNH)组成的多功能复合载氮体(图5,AH代表LiH或BaH2,ANH代表Li2NH或BaNH),其中氮化锰不仅作为氮载体,还作为催化剂,显著增强了氢化物固定N2形成酰亚胺及酰亚胺随后氢化成氨和氢化物的动力学;另一方面,氢化物也促进N2固定和随后氮化锰氢化的动力学。其氨生产速率分别比纯BaNH和Mn2N的氨生产速率高1个数量级以上,与较高温度和压力下由Cs促进的Ru/MgO催化合成氨速率相当,为设计和开发具有多种组分和功能的新型氮载体提供方向。

图5 MnNx-ANH复合载氮体机理[40]
Fig.5 Mechanism diagram of the MnNx-ANH compound nitrogen carrier[40]
总体来说,Haber-Bosch式化学链合成氨反应条件温和,常压下便可进行,有效避免了传统合成氨工艺热力学与动力学之间的矛盾,且产氨率相对较高。载氮体作为化学链的核心,其在反应过程中的结构、形貌以及组成的变化会对整个循环过程产生很大影响,开发高效稳定载氮体仍是当前工作重点,同时,该技术也需进一步开展综合能效评估和集成优化,以期早日实现工业应用。
1.2.2 碳基化学链合成氨
碳基化学链合成氨在Haber-Bosch式化学链合成氨的基础上以水替代H2作为氢源,并借助煤等碳基原料实现氮化过程,其中副产物CO可以回收利用,有助于进一步降低合成氨过程的CO2排放。该方法以Al2O3/AlN为中间体,在氮化反应和氨化反应间循环,实现了氨的高效合成[41]。这一过程均为非可逆反应,因此能够有效提高氨生成率,反应方程如下:
Al2O3 3C N2![]() 2AlN 3CO,
2AlN 3CO,
(1)
2AlN 3H2O![]() Al2O3 2NH3。
Al2O3 2NH3。
(2)
第1个氮化反应在1 500 ℃以上的N2气氛中进行,碳热还原Al2O3生产AlN,第2个氨化反应是AlN的蒸汽水解以产生NH3并重整Al2O3,后者循环至第1步骤。2个反应步骤均在0.1 MPa下进行,无需添加催化剂,并绕过能源密集型H2的生产,从而显著节省燃料和成本。此外,氮化反应步骤可使用集中太阳能作为高温工艺热源,消除化石燃料工艺产生的CO2排放。
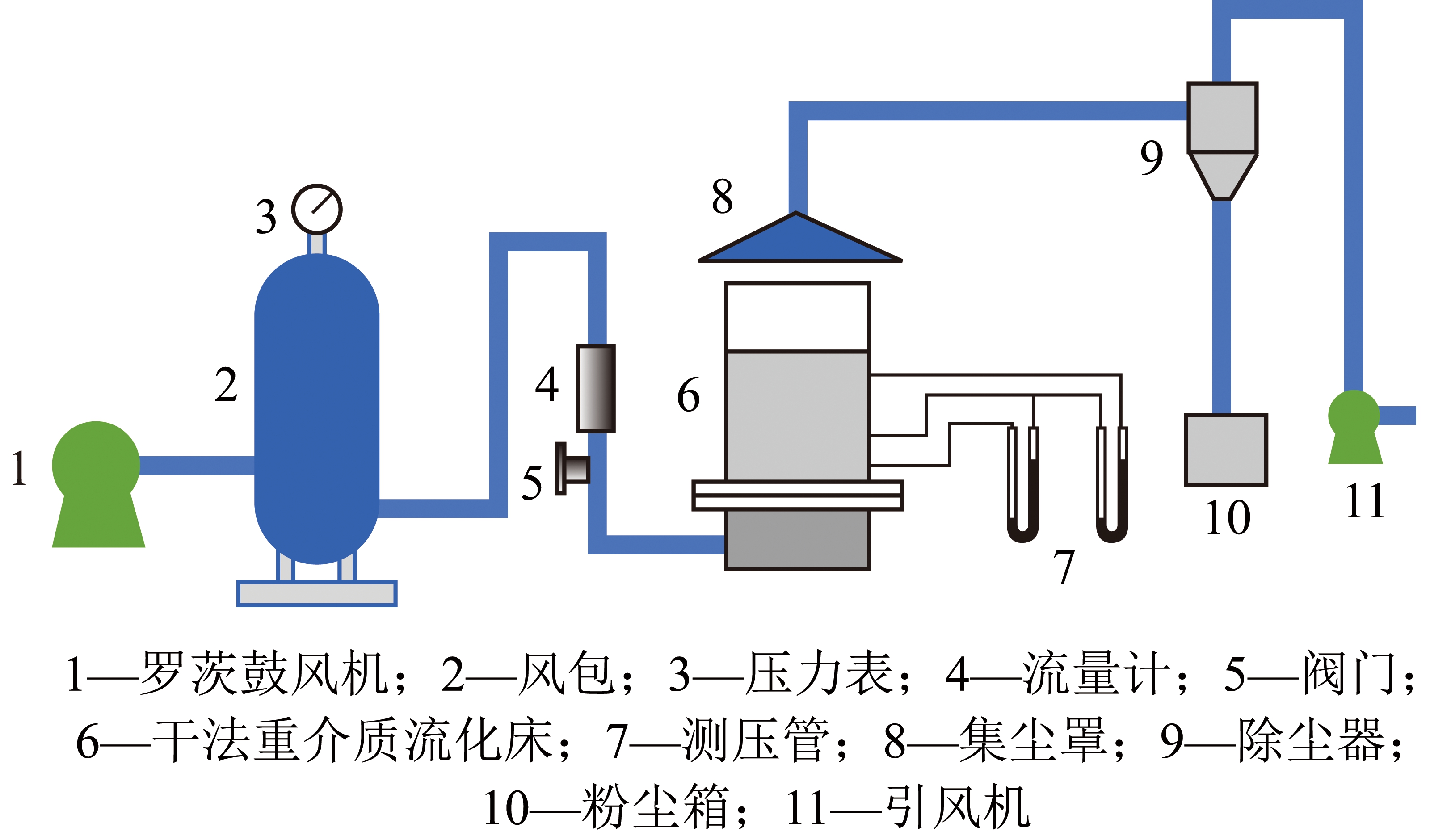
对于氮化反应的影响因素,如Al2O3结构、催化剂、反应条件、碳源类型、纯度及铝源和碳源比例等已有较多研究。Al2O3内部结构会影响氮化反应的速率,TSUGE等[42]发现1 500 ℃下,氧化铝的反应活性为γ-Al2O3>Al(OH)3>α-Al2O3;但使用α-Al2O3进行氮化反应所得氮化铝为颗粒状,而γ-Al2O3制得的氮化铝会聚集成块状;颗粒状氮化铝因其表面积较大更易进行氨化反应[43]。WANG等[44]发现1 500 ℃下,氟化钙粉末能有效促进氮化铝的生成,相对未添加催化剂的样品,加入质量分数3%的氟化钙能显著提高样品中氮化铝产量。ZHANG等[45]发现以碳黑为碳源进行氮化反应远比石墨容易,这是因为石墨中碳具有稳定结构,而碳黑中则存在大量无序化碳。在此基础上,ZHANG等[45]进一步在升温速率10 ℃/min、700 ℃的CO2气氛下将煤炭热解,热解得到的烟煤焦能较高效参与碳基化学链合成氨中的氮化反应,有利于碳基化学链制氨的工业化应用。
对于氨化反应,研究表明化学链制氨过程中氮化铝的水解在1 000℃完成,但NH3热力学稳定性低,1 000 ℃后自身分解加快,因此NH3产率随温度上升逐渐降低。BARTEL等[46]使用密度泛函理论(DFT)研究了AlN水解初始阶段的反应机制后提出,氨化反应主要通过4个步骤完成:水吸附,质子迁移形成NH2和NH3,表面N空位形成与O的结合,NH3解吸附(图6)。羟基能有效促进氮化铝水解,吸附的羟基将质子传输活化势垒降低200 kJ/mol以上催化NH2形成。GAO等[47]发现Fe2O3表面极易解离吸附羟基,但Fe2O3同样会促进氨分解,使氨产量大幅降低。随后将Fe2O3改为TiO2进行试验,成功提高了氮化铝转化率及氨产率。最后,为抑制氨在高温下的分解,WU等[48]通过量子化学计算发现,氨能完整吸附在ZrO2表面。通过选取ZrO2作为负载,大大减少了氨分解量,将氨产率提高了近1倍。

图6 足量H2O时AlN水解过程模拟[46]
Fig.6 Simulation of AlN hydrolysis process with sufficient H2O[46]
碳基化学链合成氨技术是一种节能环保的氨合成技术,其反应原料价格低廉,反应过程绿色无污染,以煤炭作为氮化反应过程中的碳源,可实现用碳而不排碳,符合我国当前国情。将来也可以生物质作为氮化反应的碳源,并与太阳能相结合,进而提供一种更清洁高效无污染的绿色合成氨途径,切实满足低碳环保和可持续发展要求。
1.3 其他新型合成氨技术
目前,由可再生能源驱动,并通过电催化、光催化和化学链等方式进行的绿色合成氨技术[49]主要有2种:利用可再生能源电解水制H2,电解空气制N2,再经过光催化或电催化等方式制氨(图7路线1);利用水与N2反应直接生成氨(图7路线2)。路线2虽然能省去制氢环节,简化步骤,但效率较低,距离工业应用较远。

图7 可再生能源驱动的绿色合成氨过程[49]
Fig.7 Green synthetic ammonia process driven by renewable
energy[49]
1.3.1 电催化合成氨
电化学合成氨可在相对低温、常压条件下进行,具有低工作压力、低能耗、清洁无污染等优点,且该过程无CO2排放,对环境较友好,是近年研究热点[50]。电化学合成氨工艺根据工作温度可分为3类[51],各自优缺点见表1。高温、中温导致NH3分解,以及低温下N2的高稳定性和低溶解度为该方法的主要问题,加入催化剂以抑制NH3分解或加强传热传质被认为是有效的解决措施。
表1 3类电化学合成氨电解质的类型与优缺点
Table 1 Advantages and disadvantages of three types
of electrolytes for electrochemical ammonia synthesis

近年来,随着电催化NRR(Nitrogen Reduction Reaction)工艺的提出,电催化合成氨发展极为迅速。该工艺相当于从潮湿空气中合成氨,低碳无污染。STUART等[52]利用太阳能的高温和产生的电能在纳米Fe2O3的氢氧化物悬浮液中电解空气和水产生氨。该反应在200 ℃下,NaOH/KOH物质的量比为0.5∶0.5的电解液中,库伦效率为35%。QIU等[53]首次发现非金属电催化剂碳化硼纳米片可在常温常压下实现高效、高选择性的人工固氮合成氨,在-0.75 V电压下氨产率高达26.57 μg/(h mg),法拉第效率为15.95%,理论研究表明,硼是催化活性中心。之后该课题组报道了一种硫掺杂碳纳米球作为一种高效的电催化剂,该催化剂在-0.7 V(相对于可逆氢电极,RHE)下获得较高的氨产率(19.07 μg/(h
mg),法拉第效率为15.95%,理论研究表明,硼是催化活性中心。之后该课题组报道了一种硫掺杂碳纳米球作为一种高效的电催化剂,该催化剂在-0.7 V(相对于可逆氢电极,RHE)下获得较高的氨产率(19.07 μg/(h mg)),且法拉第效率高达7.47%,远高于未掺杂硫的碳纳米球(3.70 μg/(h
mg)),且法拉第效率高达7.47%,远高于未掺杂硫的碳纳米球(3.70 μg/(h mg),1.45%),说明硫的引入能大幅提高材料的氮还原性能[54]。ZHAO等[55]通过密度泛函理论(DFT)计算,系统研究了单个过渡金属原子(Sc到Zn、Mo、Ru、Rh、Pd和Ag)负载在具有硼空位的缺陷氮化硼单层上作为N2固定电催化剂的潜力,其计算表明,由缺陷氮化硼纳米片支撑的单个Mo原子在室温下表现出最高的催化活性。LIU等[56]发现通过电化学激发促进N2进入富含硼的共价有机框架可实现高效的氮还原反应。模拟结果表明,在电化学条件下,硼与含氮基团成键,由此形成的非晶态共价有机骨架对N2具有更强的亲和力,从而增强了分子间的碰撞。结果表明,受电化学激发后,催化剂的反应活性显著提高,其法拉第效率可高达45.43%(图8,红色、绿色、蓝色、紫色、黄色和灰色球体分别代表B、C、14N、15N、O和H原子)。
mg),1.45%),说明硫的引入能大幅提高材料的氮还原性能[54]。ZHAO等[55]通过密度泛函理论(DFT)计算,系统研究了单个过渡金属原子(Sc到Zn、Mo、Ru、Rh、Pd和Ag)负载在具有硼空位的缺陷氮化硼单层上作为N2固定电催化剂的潜力,其计算表明,由缺陷氮化硼纳米片支撑的单个Mo原子在室温下表现出最高的催化活性。LIU等[56]发现通过电化学激发促进N2进入富含硼的共价有机框架可实现高效的氮还原反应。模拟结果表明,在电化学条件下,硼与含氮基团成键,由此形成的非晶态共价有机骨架对N2具有更强的亲和力,从而增强了分子间的碰撞。结果表明,受电化学激发后,催化剂的反应活性显著提高,其法拉第效率可高达45.43%(图8,红色、绿色、蓝色、紫色、黄色和灰色球体分别代表B、C、14N、15N、O和H原子)。

图8 N2电还原为NH3[56]
Fig.8 Electroreduction of N2 to NH3[56]
随着电催化NRR工艺的发展,对于该工艺的判断标准也逐渐明确,澳大利亚莫纳什大学SURYANTO[57]从试验方法和催化剂选择性2方面进行综述,提出了严格的试验方案,讨论了催化剂选择性问题以及提高NRR收率的途径。最后,结合各种方法的反应机制以及该领域所追求的关键指标,讨论评估NRR进展的重要基准。该团队也开发了一种以磷盐分子为质子传导体,实现高氨生成速率、高法拉第效率以及较长期稳定运行的电化学NRR体系[58]。结果表明,在20 h电化学NRR测试过程中,NH3产量线性增加,且法拉第效率保持稳定,其氨生成速率和法拉第效率分别达到(53±1)nmol/(s cm)和69%±1%,明显高于文献中最高值,证明此体系长期运行的稳定性。REN等[59]系统综述了NRR的机理、动力学、热力学、电催化剂、反应器设计以及过程耦合和优化等方面的最新进展,并重点总结了抑制析氢和提高NH3选择性的策略:限制质子和电子转移动力学、改变化学平衡、设计电催化剂。
cm)和69%±1%,明显高于文献中最高值,证明此体系长期运行的稳定性。REN等[59]系统综述了NRR的机理、动力学、热力学、电催化剂、反应器设计以及过程耦合和优化等方面的最新进展,并重点总结了抑制析氢和提高NH3选择性的策略:限制质子和电子转移动力学、改变化学平衡、设计电催化剂。
目前来看,电催化合成氨的发展非常迅速,其工艺装置简单,灵活性和可调谐性较好。但该技术目前仍处于实验室研发阶段,法拉第效率约60%,产氨速率较低,需要进一步寻找适合的催化剂或提高现有催化剂的活性、选择性以及稳定性;同时,由于电化学氮还原和析氢反应是竞争关系,且析氢反应占主导作用,因此抑制析氢反应可以有效提高电催化剂合成氨的性能;最后,电化学合成氨是一个复杂的过程,有必要加强理论计算和模型,使其更接近实际电催化剂,进而更好理解该反应机制,为合理设计性能良好的电催化剂提供指导。
1.3.2 光催化合成氨
光催化N2还原合成氨技术被认为是一种极具潜力的替代Haber-Bosch工艺生成氨的方法。与传统的工业Haber-Bosch工艺相比,在常温常压条件下,该技术以N2和水为原料,经太阳能驱动发生氧化还原反应而合成氨,能够实现太阳能向化学能的转化。作为新一代的合成氨工艺,光催化合成氨具有特殊的技术优势:可在常温常压下进行,低能耗,低成本;利用的能源为可再生的太阳能,取代了Haber-Bosch工艺所需的不可再生化石燃料,降低CO2气体排放量,对环境较友好;具有绿色可持续的优点;以水作为氢源,地球上水资源丰富。相比电催化还原制氨,光催化氮还原制氨只需要提供太阳能、水和N2就可以用一步法实现N2的氨转化,而电催化合成氨则需先将其他能源转化为电能,通过电催化过程才能实现固氮过程,因此,光催化制氨成本更低廉。
1977年,SCHRAUZER和GUTH[60]使用天然材料和实验室合成的金属氧化物第一个系统研究了光催化合成氨,发现TiO2具有相当好的固氮活性,且铁掺杂能进一步增强其光催化反应性能。这项工作激发了一系列更全面研究,包括探索TiO2晶相、表面缺陷、利用金属或金属氧化物修饰等。除TiO2外,各种其他半导体氧化物材料(如Fe2O3、WO3、ZnO、Ga2O3)也被证明具有合成氨活性。另外,金属硫化物、卤化铋、碳质材料、双氢氧化物(LDHs)、仿生光催化剂、生物杂化配合物等也被用于光催化合成氨研究。ZHU等[61]发现金刚石表面用特殊纳米膜层处理后,在水中仍具有水下发射电子能力,这一现象彻底颠覆了“电子不下水,离子不上岸”的公认规则。通过激发金刚石表面的电子,在酸性水溶液中,能直接将灌入水中的难溶N2打散成氮离子,并将质子(氢离子)黏贴到氮离子上生成氨分子。该研究为光催化合成氨开辟了新方向。
2015年,LI等[62]首次发现BiOBr纳米片在可见光照射下具有优异的氨合成性能,通过在BiOBr纳米片的{001}面上引入氧空位,可以显著提高对N2的吸附能力。HIRAKAWA等[63]发现具有大量氧空位(Vo)的市售TiO2在紫外光照射下表现出优异的氨合成性能,在48 h内观察到氨产率持续增加。系统研究了TiO2表面Vo对光催化N2还原成NH3的影响,表面氧缺陷存在产生的Ti3 位点充当N2的吸附位点,也充当光生电子的捕获位点,导致N2有效转化为NH3。随反应进行,电子和质子相继转移到吸附的N2分子上,而活性Ti3 位点可以再生,从而保持光催化活性。ZHAO等[64]也报道了一种含有氧空位的超薄LDHs纳米片,其丰富的氧空位促进了N2在可见光下的吸附和活化。同时,通过在LDH片中掺入Cu2 可以稳定Vo并强化CuCr-LDH纳米片与N2之间的相互作用,从而促进NH3生成。ZHANG等[65]发现Mo掺杂可以显著增强富缺陷W18O49超薄纳米线光催化合成氨活性。1% Mo掺杂W18O49样品的氨生成速率为195.5 μmol/(g h),其太阳能转换效率为0.028%,通过理论计算表明,Mo掺杂在促进N2活化和解离方面发挥作用,且Mo掺杂将缺陷带中心向费米能级升高,从而为催化剂中的光激发电子提供更多用于N2还原的能量。这项工作大大提高了对N2活化的理解。近来,HAN等[66]也开发了一种具有高浓度Ti3 活性位点的碳掺杂锐钛矿TiOx(C-TiOx)多孔纳米片材料,表明Ti3 相比Ru具有更好的N2吸附性能,C掺杂TiO2能很好控制Ti3 位点,有利于电子空穴对的有效分离,提高N2还原效率(图9)。
h),其太阳能转换效率为0.028%,通过理论计算表明,Mo掺杂在促进N2活化和解离方面发挥作用,且Mo掺杂将缺陷带中心向费米能级升高,从而为催化剂中的光激发电子提供更多用于N2还原的能量。这项工作大大提高了对N2活化的理解。近来,HAN等[66]也开发了一种具有高浓度Ti3 活性位点的碳掺杂锐钛矿TiOx(C-TiOx)多孔纳米片材料,表明Ti3 相比Ru具有更好的N2吸附性能,C掺杂TiO2能很好控制Ti3 位点,有利于电子空穴对的有效分离,提高N2还原效率(图9)。

图9 C-TiOx光催化合成氨性能[66]
Fig.9 Photocatalytic performance of C-TiOx for ammonia synthesis[66]
光催化氨合成是一种非常有前途的氨合成技术。理想情况下利用太阳能将氮和水转化为氨,而不需要额外的能量输入或牺牲剂。近年来在光催化剂开发方面也取得了许多重大研究进展,光催化反应机制逐渐明晰。但在真正满足工业应用的合成氨速率前,还需克服巨大挑战。目前,光催化合成氨仍受限于N2和水反应的缓慢动力学特征以及不理想的太阳能利用率,在实际氨合成中,应考虑全光谱太阳能作为光源,这需要具有优异的光吸收特性的光催化剂;反应体系方面N2在水中的溶解度、产物氨的及时分离、析氢竞争反应抑制都需要优化;最后,准确的氨定量方法和光催化性能的评估等问题也亟待解决。
1.3.3 等离子体合成氨
等离子体泛指部分或完全电离的气体,整体呈电中性,许多粒子处于激发状态。等离子体合成氨是一种有前途的能代替热催化合成氨的方法,该过程中产生的高能电子和反应性物种,可显著增强反应动力学,使N2活化等热力学不利的反应可在环境条件下进行。另一方面,等离子体固氮可以空气和水为原料,无需使用煤及天然气等其他化石原料,该固氮工艺也可实现CO2零排放。最后,等离子体固氮工艺即开即用,无需预热及稳定过程,非常适合与风电、太阳能等不稳定的可再生能源结合。
近年来,关于等离子体合成氨取得了较多成果。HU等[67]采用Au纳米晶吸收光,选择Ru原子吸附N2分子,并作为活性位点,开发了一种具有广阔光吸收范围和大量活性位点的AuRu核-天线纳米结构进行光催化固氮反应,氨生成率为101.4 μmol/(g h),比裸Au纳米晶高约7.3倍。WINTER等[68]发现等离子体衍生的中间体及其与催化剂表面的相互作用会影响氨产率,从而导致不同的反应途径:Ni/γ-Al2O3能促进等离子体与NH3生成,且有利于表面吸附NHx物种,而Fe/γ-Al2O3则相反。进一步研究了等离子体-催化剂之间的相互作用关系。LI等[69]将等离子体合成氨的过程解耦为2步:首先使用低温等离子体技术将N2有效活化为氮氧化合物,然后通过构造一种表面富硼的镍基催化剂,将NOx高度选择性地转化为NH3。其中,表面富硼特性可以增强NOx吸附、抑制氢析出,而表面镍氧化则是提高活性、选择性和稳定性的关键。最终的氨产量为198.3 μmol/(cm2
h),比裸Au纳米晶高约7.3倍。WINTER等[68]发现等离子体衍生的中间体及其与催化剂表面的相互作用会影响氨产率,从而导致不同的反应途径:Ni/γ-Al2O3能促进等离子体与NH3生成,且有利于表面吸附NHx物种,而Fe/γ-Al2O3则相反。进一步研究了等离子体-催化剂之间的相互作用关系。LI等[69]将等离子体合成氨的过程解耦为2步:首先使用低温等离子体技术将N2有效活化为氮氧化合物,然后通过构造一种表面富硼的镍基催化剂,将NOx高度选择性地转化为NH3。其中,表面富硼特性可以增强NOx吸附、抑制氢析出,而表面镍氧化则是提高活性、选择性和稳定性的关键。最终的氨产量为198.3 μmol/(cm2 h),法拉第效率接近100%。WANG等[70]发现在等离子体催化合成氨中,由催化剂表面的化学性质提供的催化效应相比催化剂的物理效应更占主导地位,过渡金属(如Ni)的存在可使等离子体更均匀放电,且提高了平均电子能量。结果表明,使用Ni/Al2O3作为等离子体催化剂时,NH3合成率最高,为471 μmol/(g
h),法拉第效率接近100%。WANG等[70]发现在等离子体催化合成氨中,由催化剂表面的化学性质提供的催化效应相比催化剂的物理效应更占主导地位,过渡金属(如Ni)的存在可使等离子体更均匀放电,且提高了平均电子能量。结果表明,使用Ni/Al2O3作为等离子体催化剂时,NH3合成率最高,为471 μmol/(g h),比仅使用等离子体时高100%。进一步,采用Ni负载的介孔MCM-41设计的催化剂如图10所示(in为骨架里,out为外表面,both为整个骨架,window-like为孔道入口,a为未经过特殊处理的催化剂;p为等离子体处理的催化剂),在60 kJ/L等离子体条件下,实现了5%的NH3合成率[71]。在MCM-41的外表面负载Ni,可以增强等离子体与催化剂的相互作用,从而提高NH3产率。由于MCM-41介孔中无等离子体放电,即屏蔽保护,因此脱附的氨随后可扩散到MCM-41有序介孔中屏蔽而不被分解,从而有效驱动反应进行。
h),比仅使用等离子体时高100%。进一步,采用Ni负载的介孔MCM-41设计的催化剂如图10所示(in为骨架里,out为外表面,both为整个骨架,window-like为孔道入口,a为未经过特殊处理的催化剂;p为等离子体处理的催化剂),在60 kJ/L等离子体条件下,实现了5%的NH3合成率[71]。在MCM-41的外表面负载Ni,可以增强等离子体与催化剂的相互作用,从而提高NH3产率。由于MCM-41介孔中无等离子体放电,即屏蔽保护,因此脱附的氨随后可扩散到MCM-41有序介孔中屏蔽而不被分解,从而有效驱动反应进行。

图10 Ni负载介孔MCM-41催化剂[71]
Fig.10 Ni supported mesoporous MCM-41 catalyst[71]
目前,国内外学者针对等离子合成氨不同工艺条件及设备、固氮反应机理以及等离子体和催化剂之间的协同固氮机制开展了较多研究。但目前研究成果还不足以实现工业化应用,氨的生成速率与产率有待进一步提高。开发稳定高效、价格低廉的催化剂仍是未来工作重点;等离子体的产生依赖高频高压、放电均匀的反应设备,同时还需保证其强度不被击穿,需优化反应设备;关于等离子体与催化剂间的协同作用机理也有待深入研究。
2 氨的燃烧
作为一种非常高效的储氢介质,氨在能源利用方面具有许多显著优势。首先其能量密度高,理论燃烧热值为317.5 kJ/mol,约为H2的1.5倍,其次液化成本低,储存运输方便,安全性高。由于其清洁无碳的特性,完全燃烧时没有CO2、硫氧化物或颗粒物的排放,是一种环境友好型的燃料。日本政府公布的第6版能源战略计划中,首次将氢能和氨能的燃烧纳入国家能源战略计划中,首先是30% H2 70% 天然气,20% NH3 80%煤粉实现混烧技术,2050年要实现100% NH3和H2的燃烧发电。韩国也在大力推动氢、氨与天然气、煤混合燃烧发电,计划在2050年实现完全零碳氨燃料发电达21.5%,氢能发电13.8%。我国的氨布局也从2018年初见端倪,近日,福州大学、北京三聚环保新材料股份有限公司、紫金矿业集团股份有限公司在福州举行绿色能源重大产业项目战略合作签约成立合资公司,创建国内首家氨-氢能源重大产业创新平台,围绕氨-氢绿色能源重大技术开展深度合作。
氨燃料本身燃点较高,纯氨直接燃烧困难,且燃烧过程中有产生NOx的可能。因此,近年来许多学者对氨燃烧及其污染物控制展开大量工作。氨稳定燃烧主要通过掺混燃烧与催化燃烧实现。
2.1 氨的掺混燃烧
2.1.1 氨与气体燃料混燃
近年来,许多学者提出将NH3与H2混合燃烧。由于H2燃烧的层流火焰燃烧速度较高,与NH3混合燃烧可提高燃烧速度及拓宽可燃性极限[72]。研究表明NH3与H2在空气中混合燃烧的层流火焰燃烧速度随燃料混合物中H2比例升高呈指数增长,且能明显增强火焰对拉伸的敏感性,H2体积分数接近50%的条件下,火焰传播速度达到纯烧CH4的水平。HAN等[73]利用热流燃烧器测定了NH3与H2的火焰燃烧速度,利用3种文献机理对其进行动力学建模,对比发现即使在不同环境压力下,其层流火焰燃烧速度趋势随H2比例的变化相同,层流火焰燃烧速度最大当量比在1.05左右,且通过灵敏度及反应路径分析表明,NH3与H2混合的氧化反应可理解为具有相同自由基池(如H和OH)的单个燃料的平行氧化过程,而火焰最高温度会随压力的降低而增加。NH3/H2混合燃料中H2体积分数大于0.3时,H2对NH3火焰的层流火焰燃烧速度增强效果尤其明显,在高温条件下H2含量和空气温度增加会提高火焰的熄灭极限、自由基浓度及最高温度,但火焰熄灭极限和最高温度会随应变速率增加而降低[74]。KUMAR等[75]对当量比0.5~1.1下的NH3/H2火焰进行研究,发现增加NH3比例后预混火焰速度大幅降低,且熄灭极限、自由基浓度和最高温度显著下降(图11)。对比发现,随NH3增多,火焰速度及相关自由基种类浓度出现差异,通过敏感性分析发现·OH是导致NH3分解的关键自由基,是各个机理预测偏差的可能来源。在尾气排放中,燃料型NOx是氨氢混合燃烧生成NOx的主要来源,而热力型NOx可忽略不计,与纯氢/空气燃烧相比,加氨燃烧后生成的热力型NOx减少。DUYNSLAEGHER等[76]在低压条件下对预混NH3/H2/O2/Ar火焰进行研究,NO形成受初始H2含量轻微影响,而在化学计量条件下,当量比降低会增加NO形成。NH3与H2混合燃烧具有很多优势,但也存在一定危险性,在预混燃烧方式下,H2占比过高将导致火焰出现强烈的回火倾向。

图11 当量比下不同NH3比例的NH3/H2瞬时层流火焰[75]
Fig.11 Instantaneous laminar flame diagrams of NH3/H2
with different NH3 ratios at equivalence ratios[75]
化石燃料仍是目前和未来一段时间主要依赖的能源,由于CH4密度、黏度等理化性质与NH3相似,目前主要研究NH3与CH4的混合燃烧。研究发现,添加CH4后具有强烈的点火增强效应,显著缩短了总点火延迟时间,热释放速率和辐射强度均有所提升[77],且燃料的火焰速度随CH4比例的升高而增大,在贫燃状态下随当量比升高而增大直至当量比为1左右,富燃状态下随当量比增大而逐渐减小,此变化规律与CH4比例无关[78-80],且燃烧速度随未燃烧气体温度升高而增加,随压力升高而降低[81-82]。在尾气排放方面,过氧系数增加会降低CO和NO排放;在O2/CO2环境中,当过氧系数一定,降低氧化剂中的氧浓度会提高CO排放而降低NO排放。二者混合燃烧后可分别减少NH3与CH4单独燃烧产生的NOx与CO2,在混合燃料中NH3比例越高,CO2排放量越低,NH3体积分数达60%时,CO2排放量为CH4单独燃烧产生的50%,而NOx排放量随NH3比例的升高而增加,NH3占比达60%时达到峰值,之后随NH3比例进一步增加而减少[83-85]。在贫燃状态下会产生更多NO,富燃状态下产生更多CO2且由于大量未燃烧的氨会与NOx复合,从而减少NOx排放[86-87],同时较高的压力可有效抑制NOx与CO排放,而较高流量也可降低N2O排放[80,88-91]。目前关于NH3与其他气体混燃的研究仍处于初步阶段,其中NH3量仍较少,因此对于混合气体中NH3为主甚至纯NH3燃烧亟需研究。
总之,氨与气体燃料的掺混燃烧相对简单,且可以有效克服纯氨燃烧放热率低、稳定性差等问题,是促进氨燃料早日实现工业应用的有效方法。氨氢内燃机、燃气轮机以及燃料电池的研发目前均取得了一定成果。清华大学车辆与运载学院先进发动机利用H2点火形成分布式燃气射流引燃氨混合气,实现了氨发动机的稳定运行。与东风商用车公司联手在其龙擎DDi13重型车发动机上实现氨/柴油燃料点火成功,属国内首台氨燃料重型车用发动机。燃气轮机方面,日本株式会社在2 000 kW级燃气轮机中实现了70%液氨作为燃料的零CO2发电,并成功将燃烧过程中产生的温室气体减少99%以上。燃料电池方面,福州大学团队研制了2 kW级氨-氢燃料电池原型机,解决了氨-氢能源转换过程中关键科学技术难题,是国际领先的颠覆性关键技术。氨在新能源领域具有很大潜力,将来进一步提高氨的掺混比例、简化燃烧器结构、控制NOx生成,氨能将具有更广阔的发展前景。
2.1.2 氨与煤掺混燃烧
据统计,燃煤发电CO2排放量目前占我国CO2总排放量的34%左右,氨煤掺混燃烧可以有效实现节能降碳。然而,氨与煤粉共燃通常会有一些问题,如由于反应缓慢而导致火焰不稳定,由于氮含量较高而导致NOx排放更高,以及由于火焰温度较低而导致热辐射更低。日前,国家能源集团首次以35%掺烧比例在40 MW燃煤锅炉上实现了混氨燃烧工业应用。验证了燃煤锅炉混氨燃烧的可行性,为我国燃煤机组实现CO2减排提供了发展方向,氨煤掺混燃烧亟待进一步深入研究。
氨煤掺混后的着火与燃烧是锅炉稳定运行的基础。XIA等[92]和HADI等[93]对煤粉和氨燃料掺混燃烧过程中球形火焰在湍流流场中的传播特性进行了研究,通过对比煤粉/氨共燃和纯氨燃烧的火焰传播速度发现,煤粉/氨燃烧的火焰传播速度是否高于纯氨燃烧的火焰传播速度取决于氨氧化剂当量比。朱京冀等[94]发现氨煤掺混燃烧促进了煤挥发分释放,使贫燃和富燃条件下的着火时间提前。LEE等[95]按照燃气轮机燃烧室的模型设计了一套试验装置,结果表明,氨与煤颗粒混燃效果较好(图12),氨燃烧温度较低,氨-煤火焰形状比单独燃烧气态氨时更长。

图12 5 kWth容量下火焰观察结果[95]
Fig.12 Flame observation results at 5 kWth capacity[95]
由于氨燃料中富含N元素,因此掺氨燃烧中的NOx生成与排放特性备受关注。日本煤炭燃烧研究机构之一的电力工业中央研究院(CRIEPI)[96]在单燃烧器试验炉中进行了燃料型NOx生成的共燃试验,当氨喷入煤粉燃烧器燃烧,共燃率小于10%时,与常规煤燃烧产生的NOx量相当。NOx浓度随掺混燃烧速率的增加而增加。因此,可在燃烧器最佳距离喷射氨减少NOx产生。ISHII等[97]在10 MWth试验炉上,掺混燃烧率为20%时进行了氨与煤粉掺混燃烧试验,在额定负荷下的氨混烧中,通过适当控制氨流速和二级燃烧率,可将NOx浓度控制在与不掺氨时相同的水平。TAMURA等[98]在10 MWth试验锅炉中进行共燃试验,结果表明,通过控制燃烧空气旋流,可获得稳定火焰,同时测得20%掺混燃烧时NOx浓度等于或低于100%煤燃烧时的NOx浓度。此外,NOx生成量随喷氨位点的不同而不同,优化后,测得NO浓度低于燃煤时的NO浓度。
ITO等[99]通过向煤燃烧产生的强还原区注入氨来控制NO生成。氨在强还原区被分解为氮和氢。通过10 MW热输入测试设备解决了废气中NO浓度增加问题。通过数值分析,讨论了1 000 MW锅炉壁面热流密度问题,虽然氨煤掺混燃烧时的燃气温度略低于燃煤,但燃煤和氨掺混燃烧时的局部热流密度和总热流密度无太大差异。WANG等[100]在1 100 ℃下,在一维多进风口控制燃烧温度的降火炉中进行了氨煤掺混燃烧试验。在空气分级和不分级燃烧条件下,研究了氨掺混燃烧比对NO、CO2排放以及CO、H2S释放特性的影响,结果表明,氨煤掺混燃烧可有效降低CO2排放,且在氨煤掺混燃烧过程中空气分级燃烧能有效控制NO排放。采用20%~30%氨掺混燃烧比例经济性和NO排放控制效果更好,氨/煤掺混燃烧可极大促进煤气化反应,导致空气分级燃烧中还原区CO浓度高于煤燃烧。同时,氨掺混燃烧对煤中H2S的释放有明显抑制作用,会促进后续分解过程。ZHANG等[101]运用计算流体动力学(CFD)模拟方法,研究了单旋流式煤粉燃烧装置中NH3共燃过程,利用试验数据对仿真精度进行评价,结果表明模拟结果可较好再现煤与氨掺混燃烧的特性。CARDOSO[102]建立了二维欧拉-拉格朗日数值模型,描述了煤氨在流化床反应器中的掺混燃烧过程。结果表明,NH3掺混燃烧率在0~80%时,对燃烧过程放热、碳、NO和NH3排放影响较大。与纯煤燃烧相比,NH3掺混燃烧可减少CO2排放量。当NH3掺混燃烧率为10%时,NO排放水平与单纯燃煤相同,而在20%~80%时,NO排放逐渐下降,降幅高达40%。NH3注入位置对NO排放有显著影响,注入点位于床面下游,会导致NO浓度增加。空气分级对NO形成有主导影响,仅空气分级20%即可减少NO排放50%。
氨与煤颗粒的详细反应机理与影响机制亟需研究。CHEN等[103]采用试验和密度泛函理论对燃煤锅炉NH3掺混燃烧高温还原区NO非均相还原机理进行系统研究。结果表明,NH3掺混燃烧促进了还原区NO的还原,并与半焦协同促进了NO的非均相还原。在非均相反应中,理论计算阐明了焦炭和NH3对NO还原的协同促进机制。键序和电子定位函数(ELF)分析表明,B2结构(NH2以N-down形式吸附在炭上,NO以平行形式吸附在炭上形成的中间结构,图13)形成的NNH自由基提高了与C原子的结合能,抑制了NH2和NO的还原。

图13 B2结构上NH2-NO非均相反应的能量分布[103]
Fig.13 Energy distribution of the heterogeneous
reaction of NH2-NO on the B2 structure[103]
目前对氨煤掺混燃烧的研究主要集中在NOx排放、锅炉系统运行分析和模拟计算方面,缺乏系统的氨煤掺混燃烧试验数据分析。氨煤掺混燃烧中氨燃料会影响煤的着火行为以及煤燃烧中挥发分的形成、分布与转化,混燃时的湍流火焰传播速度则与煤的挥发分含量密切相关。氨与煤的掺混燃烧存在较大的NOx生成与排放风险,控制NOx生成具有较大挑战。现有研究初步揭示了中小掺混比下各因素的表观影响规律,而对深层次影响机制仍认识不足。大比例掺氨仍处于模拟阶段,具体还需考虑到氨煤掺烧的着火可能性,分级燃烧NOx生成情况仍须进一步探究。氨煤掺混燃烧的详细反应机理与影响机制须进一步研究。
2.2 纯氨燃烧
2.2.1 氨的催化燃烧
NH3与H2或碳氢燃料混合燃烧虽具有一系列优势,但由于NH3的低反应性、点火困难等特点,在燃料中大多以高比例H2或碳氢燃料掺混少部分NH3进行燃烧,关于混合燃料中高NH3比例甚至纯氨的燃烧研究仍比较缺乏。同时在燃烧过程中不可避免会产生大量NOx,因此有学者将NH3进行催化燃烧。催化燃烧操作温度低,可减少NOx排放从而实现高效率燃烧[104]。目前国内外学者以负载型催化剂为主要研究方向。HINOKUMA等[105]研究了O2浓度对不同负载催化剂NH3燃烧分解性能的影响,发现负载型催化剂抑制NH3燃烧分解过程中N2O/NO的生成与NH3分解催化活性的趋势不同,而负载型Cu和Pt催化剂表现出高N2(低N2O/NO)选择性和燃烧分解活性。ISUPOVA等[106]用纯氧化物和钙钛矿为蜂窝堇青石载体,制备了整体式蜂窝催化剂。通过催化剂测试表明,活性组分和载体之间存在强烈的化学相互作用,使NH3氧化成NO。PINAEVA等[107]以草酸铁作为催化剂前体制备了整体负载型FeОх/Al2O3催化剂。由于载体煅烧温度降低,并形成高度缺陷的Fe-Al-O固溶体,其表面层富含铁离子或稳定、超细的FeOx颗粒,因此催化剂活性很高。
HINOKUMA等[108]发现NH3燃烧活性与CuOx催化剂还原性与分散性密切相关,载体上高度分散的CuOx催化剂纳米颗粒被认为在NH3低温点燃中起关键作用,且其氧化态和吸附NH3的解离态是重要的催化燃烧性能,因此CuOx是NH3燃烧的潜在催化剂。HINOKUMA等[109]制备了以SiO2为载体负载的CuOx催化剂,进行催化燃烧时加强了NH3与燃烧过程中产生的NO还原反应,从而抑制了N2O/NOx产生率,最终实现高N2选择性。HINOKUMA[110]对比了基于氧化铜(CuOx)蜂窝/颗粒催化剂的NH3催化燃烧性能,发现蜂窝催化剂在高反应温度下的NO选择性高于颗粒催化剂。SHRESTHA[111]制备了双功能混合双层Cu-SSZ-13催化剂和Pt/Al2O3涂层整体式催化剂,发现将二者混合能实现更高的NH3转化率,同时保持较低的NOx选择性。HINOKUMA等[112]研究表明,氧化铜催化剂在高温下催化NH3氧化反应过程中,可有效降低NOx排放,但在高温燃烧过程中,部分CuO氧化成Cu2O,导致催化剂失效,影响催化NH3燃烧效果,因此需性能更好的催化剂进行NH3燃烧,从而推进NH3作为清洁能源的进程。WU等[113]采用试验和DFT(密度泛函理论)第一性原理计算相结合的方式研究了高温(>800 ℃)下不同催化剂对NH3氧化过程中NOx排放和N2选择性的影响。结果表明,以Fe2O3为催化剂时,NH3转化率为96.2%,N2选择性为97.7%,高于无催化剂时NH3的转化率。DFT模拟结果表明,NH3和O2可分别吸附在Fe2O3(001)的Fe(top)上。共同吸附在Fe2O3(001)的Fe(top)上时,NH3和O2的吸附增强,同时原子间键长增加形成氧空位,促进NH3氧化(图14)。

图14 镍改性的Fe2O3基催化剂催化氨氧化反应机理[113]
Fig.14 Mechanism of ammonia oxidation catalyzed by Ni modified Fe2O3 based catalyst[113]
最后,用浸渍法制备了一种Ni改性的Fe基催化剂(10% NiO/30% Fe2O3/60% Al2O3),经X射线光电子能谱(XPS)证实为充满氧空位。DFT模拟结果表明,吸附NH3和O2的能力进一步增强,NH3转化效率和N2选择性稳定提高至96.8%和100%,具备良好的催化活性,后续的NH3催化氧化试验也证实该催化剂具有很高的NH3转化率和N2选择性。
总体而言,氨的催化燃烧方面,Pt等贵金属催化剂在低温下活性较好,但温度升高会使其选择性降低,NO等副产物增多。而Cu、Fe等过渡金属催化剂反应温度较高,但N2选择性较好。目前研究还处于催化氧化阶段,后续还需进一步提高催化剂活性及N2选择性。
2.2.2 氨的化学链燃烧
化学链燃烧(CLC)是一种很有前途的CO2封存技术,不需高耗能。在化学链循环燃烧中,用于燃料氧化的氧气由固体氧气载体(通常是金属氧化物)提供,避免了燃料和空气直接接触。在没有N2存在的情况下氧化碳氢化合物和空气中痕量气体会产生含高浓度CO2的烟道气。系统一般由2个相互连接的沸腾床反应器组成一个环路。在燃料反应堆中,碳氢化合物CnH2m与金属氧化物MxOy的氧同时氧化,生成CO2和H2O(式(3))。还原的金属氧化物MxOy-1循环到空气反应器,被空气提供的氧气重新氧化(式(4))。这2个反应的总和高度放热,其中载氧体的类型和结构、还原气体和操作温度是决定反应活性的重要参数。
CnH2m (2n m)MxOy![]()
nCO2 mH2O (2n m)MxOy-1,
(3)
O2 2MxOy-1![]() 2MxOy。
2MxOy。
(4)
将化学链循环燃烧应用于NH3燃烧,能很好控制NOx。NOx和N2生成反应之间的选择性高度依赖燃烧条件[114],燃烧过程通常为减少NOx生成而设计。MAYRHUBER等[115]提出了化学链循环燃烧中NH3可能发生的几种反应:
2NH3![]() N2 3H2,
N2 3H2,
(5)
NH3 2.5MxOy![]() NO 1.5H2O 2.5MxOy-1,
NO 1.5H2O 2.5MxOy-1,
(6)
2NH3 3MxOy![]() N2 3H2O 3MxOy-1,
N2 3H2O 3MxOy-1,
(7)
6NO 4NH3![]() 5N2 6H2O,
5N2 6H2O,
(8)
2NO 2MxOy-1![]() N2 2MxOy。
N2 2MxOy。
(9)
NH3催化分解(式(5))的热力学最佳温度为400 ℃以上(由吉布斯自由能计算得出)。一些金属对NH3分解有催化作用,LEPP LAHTI等[116]研究发现亚铁白云石、烧结铁矿石和镍(Ni)颗粒对NH3分解有催化作用。以氧化镍为载氧体的化学发光试验表明,镍促进NH3分解。因此,NH3的催化分解在燃料反应堆中尤为重要。
LAHTI等[116]研究发现亚铁白云石、烧结铁矿石和镍(Ni)颗粒对NH3分解有催化作用。以氧化镍为载氧体的化学发光试验表明,镍促进NH3分解。因此,NH3的催化分解在燃料反应堆中尤为重要。
NH3被载氧体氧化(式(6))是燃料反应堆中NO生成的主要路径。GU等[117]列出了氧化铁和NH3可能反应的路径,在标准吉布斯自由能的基础上,计算几种反应的平衡常数K,只有从Fe2O3还原为Fe3O4,且热力学有利温度在700 ℃以上时,NH3才可能生成NO,在其他计算温度下,NH3不会被Fe3O4或FeO氧化成NO。
NH3与载氧体的反应(式(7))是最理想的反应式,该反应最终未生成NOx,也是氨化学链循环燃烧期望发生的反应。
NH3还原生成的NO(式(8))最佳热力学温度在25 ℃以上,NO可被NH3通过纯气相反应还原,也可被金属氧化物催化还原。
NO可被还原后的载氧体还原,生成N2(式(9))。HAYHURST等[118]研究表明铁可有效还原NO。然而,NO能否被部分还原的氧化铁(Fe3O4,FeO)还原尚不清楚。热力学计算结果表明,高于25 ℃时,Fe、FeO、Fe3O4都能还原NO。
载氧体在化学链循环燃烧中极为重要,学者开发和测试了一系列载氧体,包括合成载氧体(Ni-、Fe-、Cu-、Mn-)和天然材料(主要是CaSO4和铁矿石)[119-120]。在CLC过程中,由于磨损、颗粒烧结、反应性恶化等原因,载氧体不可避免会损失,此时需提供载氧体来维持运行,增加投资成本。CHENG等[121]在化学链循环燃烧条件下开展了钛铁矿氧化氨研究,分析了NH3在钛铁矿上的催化分解、NH3氧化以及还原钛铁矿和NH3还原NO的反应。研究表明,NH3分解是钛铁矿床CLC燃料反应器中生成N2的重要途径,存在还原气体时,钛铁矿上NH3氧化是NO生成的唯一可能途径。反应体系中主要含氮物种为N2和NO,反应器尾气中仅检出少量N2O和NO2。NORMANN等[122]在化学链循环燃烧条件下开展了Ni、Fe、Mn三种载氧体氧化氨的研究,分析了3种载氧体可能发生的反应路径,并对其进行热力学分析,NH3催化分解被认为是NH3氧化的主导。对于完全氧化的材料,锰载体的NO生成量最高,在6 000×10-6以上,而铁基材料在引入1% NH3气体时的峰值约为1 000×10-6(图15)。QIN等[123]经周期性DFT计算揭示了CLC过程中,NH3在普通和还原Fe2O3表面的吸附、脱氢和氧化的详细机制,认为第2步脱氢为NH3完全成为H2O和N2的速控步骤,解释了水的形成步骤以及2个被吸附的N*形成N2的过程。在氨气CLC过程中,氧化铁的产物分布有显著影响。该研究对后续NH3化学链循环燃烧有一定指导意义。

图15 在载氧体中加入1% NH3 10 s(铁基载氧体)
和60 s(锰基载氧体和镍基载氧体)时NO生成情况[122]
Fig.15 NO generation when 1% NH3 is added to the oxygen
carrier for 10 s(iron based oxygen carrier) and 60 s(manganese
basic oxygen carrier and nickel based oxygen carrier)[122]
关于NH3化学链燃烧研究较少,后续可从载氧体的晶格氧活性出发,探究其对于NH3转化和N2/NO选择性的影响。NH3直接燃烧机理研究较多,为进一步开展NH3化学链燃烧机理研究奠定基础。
3 氨利用
氨作为一种重要的基础化工原料,除用作氮肥和制冷剂外,还用于硝酸、铵盐、纯碱、塑料、合成纤维、尿素等材料生产。由于具有还原性、碱性及富含氢等特性,工业用途广泛,主要介绍氨在制氢、碳捕集以及脱硫脱硝方面研究进展。
3.1 氨制氢
3.1.1 贵金属催化剂催化氨制氢
贵金属主要指金、银和铂族金属等8种金属元素。早期研究氨分解主要是为了解氨合成。纯金属的催化活性遵循经典的火山型曲线。贵金属催化剂中的钌基(Ru)催化剂具有最高的催化产氢效率。
近年来,对于钌基催化剂催化氨分解产氢的研究较多,DI CARLO等[124]研究了温度(400~500 ℃)、压力(0.1~1.0 MPa)、GHSV(Gas Hourly Space Velocity,气体体积空速,300~2 400 h-1)对于Ru/Al2O3(Ru质量分数8.5%)催化活性的影响。结果表明,在0.1和0.5 MPa压力下,GHSV和温度均能达到接近化学平衡的转化率。特别是0.1 MPa时,NH3转化率始终高于99%,而0.5 MPa时,NH3转化率由400 ℃的96%到500 ℃时的99%不等。1 MPa时,只有在450和500 ℃时,所有GHSVs达到化学平衡,NH3转化率分别为95.5%和97.2%。400 ℃、GHSV为300 h-1时,才达到接近化学平衡转化率(92%),而其余GHSV的NH3转化率始终较低,GHSV为2 400 h-1时解离率为80.8%。
HUANG等[125]利用共沉淀法、热解法和尿素法制备了4种不同载体(La2O3、Al2O3、SiO2和Er2O3)负载的Ru基催化剂,比较其NH3转化效率(图16),结果表明,300~550 ℃,Ru/La2O3为催化效果最好的负载型催化剂,500 ℃时,Ru/La2O3催化的NH3转化率为80.7%。研究不同煅烧温度对催化分解效果的影响,对Ru/La2O3而言,最合适的煅烧温度为700 ℃。XRD和TEM分析显示,Ru/La2O3-700的高催化活性可能是因为纯La2O3相的形成。在Ru/La2O3-700-i样品中,平均Ru颗粒达4.7 nm,该催化剂在525 ℃下84 h内表现出优异的稳定性,这可能是由于La2O3高度分散和空间隔离了Ru颗粒。

图16 不同氨分解催化剂活性比较[125]
Fig.16 Comparison of activity of different catalysts[125]
CHIUTA等[126]研究了微通道反应器中商用Ru/Al2O3催化剂催化氨分解制氢的效率,确定温度区间为723~873 K,NH3流量控制在100~500 mL/min(标况下)。基于Temkin-Pyzhev动力学,通过参数细化和估计建立了准确预测整个试验操作过程的全局速率表达式。动力学模型为后续的CFD模拟提供反应源项,旨在了解微通道反应器内的反应耦合输运现象,利用速度、温度和物质浓度分布详细讨论了输送过程和反应器性能。结果发现500 mL/min和873 K时,NH3转化率达到最大,为99.8%。
贵金属催化剂活性较好,但在高温条件下催化反应时催化活性受到影响[127],且贵金属催化剂生产成本较高,限制其进一步大规模应用。过渡金属如镍(Ni)、铁(Fe)等凭借其低廉的价格和较好的催化活性,推动过渡金属催化剂研究。
3.1.2 非贵金属催化剂催化氨制氢
Ni基催化剂的价格相较Ru基催化剂低廉,MUROYAMA等[128]发现尽管Ni/La2O3型催化剂的比表面积(4.7 m2/g)比Ni/Al2O3型催化剂(200 m2/g)小得多,但二者催化活性相差无几。Ni/La2O3催化剂负载量在10%~70%时,Ni质量分数40%的样品在550 ℃时的NH3转化率在78.9%。进一步研究表明,Ni/La2O3催化剂在还原过程中,LaNiO3促进了La2O3表面细小镍颗粒的形成,使其具有较高的催化活性。CAO等[129-130]通过酸消化和碱再沉淀方法对赤泥改性,进一步采用均相沉淀方式制备了不同质量分数Ni负载的氨分解催化剂,研究发现Ni负载量低于9%时,催化活性提升并不明显;Ni负载量为15%时,催化剂催化活性最高;继续提高Ni负载量,催化活性迅速下降。Ni与催化剂载体之间的协同作用、高分散的Ni物种和催化剂的高表面积是提高催化活性和产氢量的关键,过高的Ni负载量会使催化剂颗粒团聚,破坏其孔隙结构进而影响催化活性。
与Ni基催化剂相比,铁基催化剂来源更广泛且价格低廉,催化效果良好。LI等[131]运用共沉淀法和湿性浸渍法得到了Ru/Fe-C样品。样品在328 K下干燥5 h,823 K下Ar气流下煅烧2 h,采用盐酸处理铁碳样品,去除铁氧化物纳米颗粒,得到近乎纯净的多孔碳材料(C#)。由于Fe的辅助作用,Ru/Fe-C催化剂相比Fe-C和Ru/C#催化剂,NH3分解性能明显提高。600 ℃、20 000 mL/(h·g)时,Ru/Fe-C催化剂上的NH3转化率最高,为97.5%。ZHANG等[132]研究了碳纳米管管状通道内Fe-Co合金纳米颗粒的合成、表征和催化性能,研究证实Fe和Co可在分离的纳米颗粒中均匀分布,Fe负载质量分数为20%时,催化剂的催化活性最好,通过与少量Co合金化可进一步提高Fe的催化活性,碳纳米管内部的限域作用可提高纳米颗粒的热稳定性。
铁基、镍基、钌基催化剂中,钌基催化剂催化氨分解活性最高,且贵金属基氨分解催化剂在500 ℃以下同样具有良好活性,480 ℃可达99.5%,400 ℃以下较受限。但贵金属催化剂成本较高,限制了广泛应用,目前较好的思路是将贵金属与过渡金属结合,降低价格同时提升催化活性。铁基催化剂价格低廉,来源广泛,但其催化活性相比钌基和镍基催化剂存在不足。镍基催化剂研究最成熟,商业化应用广泛。如中国石油化工集团有限公司与福大紫金氢能科技股份有限公司共同打造了全国首座氨现场制氢加氢一体站示范项目,采用的镍基催化剂由福州大学江莉龙团队研发,能将氨制氢温度由850 ℃降至500 ℃以下,氨分解率达99.5%。
3.2 氨法碳捕集
氨法碳捕集技术利用氨水对合成气进行脱碳处理,同时生产碳酸氢铵化肥,是目前应用较成熟的技术。2007年开始,阿尔斯通公司便在美国Mountaineer电厂、挪威Mongstad炼油厂等地建造10万t/a商业化示范装置。近年来,随着温室效应加剧,CO2减排问题引起关注。燃煤电厂烟气是CO2长期稳定排放源,利用氨法碳捕集将电厂烟气中CO2捕集回收是降低CO2排放最直接有效的手段之一[133]。AN等[134]对比了氨水吸收法与传统MEA吸收法的动力学和吸收能力,结果表明,氨水对CO2的吸收比MEA更快,特定条件下二者动力学几乎相同。而氨水价格低廉,产物碳酸氢铵可作为肥料提供植物生长所需氮元素和CO2,也可再次分解获得氨水从而循环利用,具有很好的经济价值;实际应用中,氨水还能吸收烟气中酸性气体,进一步降低污染物排放。
氨法碳捕集技术分为CO2吸收和解吸2个过程。将烟气通入一定浓度氨水中,CO2扩散至气液相界面,融入碱性氨水中,进入液相后CO2继续向液相主体扩散,并与液相中氨反应,研究显示该过程首先生成氨基甲酸铵,进一步生成碳酸铵,CO2过量时则生成碳酸氢铵[135]。氨水吸收CO2是常见的可逆化学反应,生成的碳酸氢铵可再次解吸放出CO2。具体反应如下:
CO2 NH3![]() NH2COOH,
NH2COOH,
(10)
NH2COOH NH3![]() NH2COONH4,
NH2COONH4,
(11)
NH2COONH4 H2O![]() NH4HCO3 NH3,
NH4HCO3 NH3,
(12)
NH4HCO3 NH3![]() (NH4)2CO3,
(NH4)2CO3,
(13)
NH2COONH4 CO2 2H2O![]() 2NH4HCO3。
2NH4HCO3。
(14)
以上反应中氨基甲氨酸的生成速率较快,属于不可逆的二级反应。除以上途径外,碳酸氢铵还可通过以下途径生成:
CO2 H2O![]() H2CO3,
H2CO3,
(15)
H2CO3 NH3![]() NH4HCO3。
NH4HCO3。
(16)
以上反应为典型的碳酸盐体系反应,因此在氨法碳捕集过程中,NH2COO-和![]() 物质的量浓度始终高于
物质的量浓度始终高于![]() 除碳后的产物随溶液浓度和碳化度的变化而变化,氨水浓度较高时,反应物碳化度降低,主要生成氨基甲酸盐;氨水浓度降低时,反应物碳化度较高,此时氨基甲酸盐将进一步水解为碳酸氢铵析出[136-137]。
除碳后的产物随溶液浓度和碳化度的变化而变化,氨水浓度较高时,反应物碳化度降低,主要生成氨基甲酸盐;氨水浓度降低时,反应物碳化度较高,此时氨基甲酸盐将进一步水解为碳酸氢铵析出[136-137]。
氨水吸收法中CO2解吸过程即碳酸氢铵溶液受热分解的过程,该过程36 ℃以上便可进行,且温度过高会导致氨逃逸,降低溶液的循环利用能力。解吸时首先碳酸氢铵被分解为碳酸氨、CO2和水,继续升高温度,碳酸氢铵将直接分解产生NH3溶于水中,最后碳酸铵分解,溶液恢复吸收能力,其反应方程式如下[138]:
2NH4HCO3(aq)![]() (NH4)2CO3(aq) CO2(g) H2O(l),ΔH=27.51 kJ/mol,
(NH4)2CO3(aq) CO2(g) H2O(l),ΔH=27.51 kJ/mol,
(17)
NH4HCO3(aq)![]() NH3(aq) CO2(g) H2O(l),
NH3(aq) CO2(g) H2O(l),
ΔH=64.87 kJ/mol,
(18)
(NH4)2CO3(aq)![]() 2NH3(aq) CO2(g) H2O(l),
2NH3(aq) CO2(g) H2O(l),
ΔH=102.23 kJ/mol。
(19)
氨法碳捕集技术早在20世纪90年代就已有理论研究。1983年,钦淑均等[139-140]研究了纯氨水以及低碳化度下氨水吸收CO2的速率,研究表明,CO2在氨水中的溶解度与温度及氨水浓度有关,温度升高,反应速率常数增大,但气体溶解度系数降低,最终导致CO2吸收速率不变。通过测得的二级反应速率常数与温度的关系,推算出NH3与CO2吸收反应的活化能,给出了二级反应速率常数与温度、离子强度的关系式以及CO2溶解度系数的修正式,为此后氨水吸收CO2机理研究提供参考。氨水吸收CO2是可逆吸收过程,因此,在适当条件下,CO2可按吸收的逆反应从碳化氨水中解吸出来。基于此,张成芳等[141]通过低于沸点的膜状解吸试验,论证了CO2的解吸机理,即解吸速率由NH4HCO3分解成NH2COONH4的反应控制,且CO2更易从碳化度较低的氨水中解吸。刁永发等[137]对氨水洗涤电厂模拟烟气中的CO2进行研究,发现在合适的条件下,氨水洗涤可脱除大部分CO2,平衡时脱碳率在95%以上,其动力学研究表明,在试验温度范围内,氨水与CO2的反应符合Arrhenius公式。
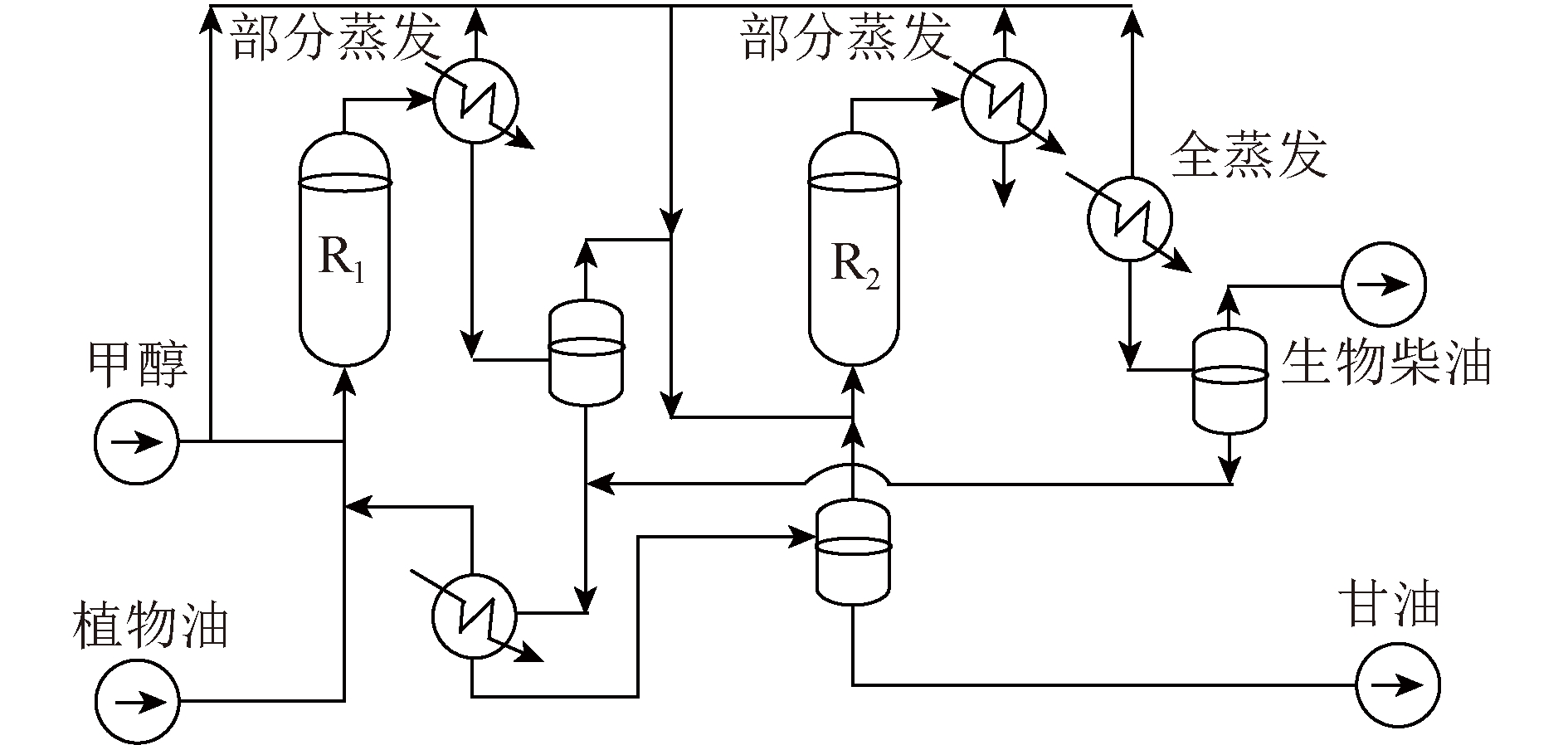
为论证氨法碳捕集技术的发展潜力,实现该化学吸收法在电厂尾气捕集中的应用与推广。BAI等[142]对氨水和MEA吸收CO2进行试验,发现氨水吸收容量为1.2 kg/kg,远高于MEA溶液,证明通过氨水洗涤脱除CO2的潜力巨大。马双忱等[143]对比了氨水与MEA的CO2捕集效果,结果表明氨水吸收法的CO2吸收质量为1.141 2 kg/kg,而MEA法的CO2吸收质量仅为0.326 1 kg/kg,且氨水吸收法能进行吸收剂再生或副产物利用,更具工业应用潜力。TORO-MOLINa等[144]运用Aspen Plus软件对电厂烟气氨法和MEA法脱除CO2过程进行了模拟,结果显示氨水吸收法是从烟气中分离CO2的有效解决方案,其能效损失为7.2%,且通过间接接触器可进一步将损失降至6.3%。
近几年,学者通过优化反应条件、改进反应容器等措施提高CO2吸收率及解吸率,同时降低再生过程的氨损失甚至抑制氨逃逸。张君等[145]采用超重场强化氨水常压吸收燃煤锅炉烟道气中低浓度CO2,相比传统鼓泡吸收方法CO2脱碳率更高,在超重场强化作用下,质量分数10%的氨水脱碳率甚至优于质量分数28%的传统鼓泡法。张茂等[146]以稀氨水为吸收剂,在喷淋塔内对温度、氨水浓度及CO2浓度等参数进行研究,过程中连续监测CO2浓度。结果表明,即使是稀氨水也可以实现85%的CO2脱除,增大氨水浓度有利于化学平衡正移,但过大的氨浓度也会增加氨逃逸造成的损失。22~50 ℃下CO2脱除率受反应温度影响显著,波动较明显,并在40 ℃附近达到最大值。马双忱等[147]采用鼓泡反应器系统研究了氨水质量分数、烟气中CO2浓度、入口气体流量、溶液pH及温度对CO2脱除率的影响,结果表明,CO2脱除率随氨水质量分数的增加而增加,但质量分数高于16%后增长不明显;在氨水吸收量恒定的情况下,增大烟气中CO2浓度与入口气体流量不利于CO2脱除;最终确定最佳反应工况为氨水质量分数16%、CO2体积分数12%以及反应温度45 ℃。BAK等[148]对冷冻氨法碳捕集技术进行研究,结果表明,改变氨水温度会显著改变氨逃逸率和CO2脱除率,而改变烟气温度对CO2脱除率和氨逃逸绿的影响很小。此外,氨水温度和烟气温度分别在7 ℃和10 ℃下运行时,CO2吸收效率超过85%,且氨泄漏最小。TORO等[149]采用一种内侧为PMP,外侧为PP的复合膜进行试验,结果表明采用膜接触器不仅可以减少氨逃逸,还可以改善吸收过程,进而扩大温度、压力和氨浓度的可调节范围,在较低气体速度下,CO2去除效率达99%以上。膜接触器虽然不能完全避免氨逃逸,但可将其降至1%以下,不仅减少二次污染,还保留了再生溶液的吸收性能,有助于氨水碳捕集技术的优化发展。
综上,氨法碳捕集技术效率较高,产物可以进一步加工产出化肥,并且氨水对于SO2和NOx等一并脱除,是一种经济环保的技术。但目前也存在氨逃逸、再生液效率降低等问题亟需解决。
3.3 氨法脱硫脱硝
氨法脱硫脱硝工艺对于降低烟气中SO2和NOx排放十分重要,是发展较成熟的一种技术,目前已有较多工程化示范项目。2016年,《高效节能氨法脱硫、脱硝、除尘深度净化技术》科技成果鉴定会在北京举行,宇清环保科技有限公司自主研发“高效节能氨法脱硫脱硝除尘深度净化技术”取得了较高的评价,该项目通过化肥厂燃煤锅炉烟气余热,实现塔外饱和结晶,对氨法脱硫技术进步具有明显示范作用。我国新疆地区,由西安航天源动力工程有限公司建设的热电厂氨法脱硫超低排放示范工程也取得令人满意的结果,仅2018年削减SO2 15 000 t、NOx 3 000 t、烟粉尘200 t,对于减少空气污染、减轻酸雨危害、改善环境质量、保护人类身体健康具有积极作用。
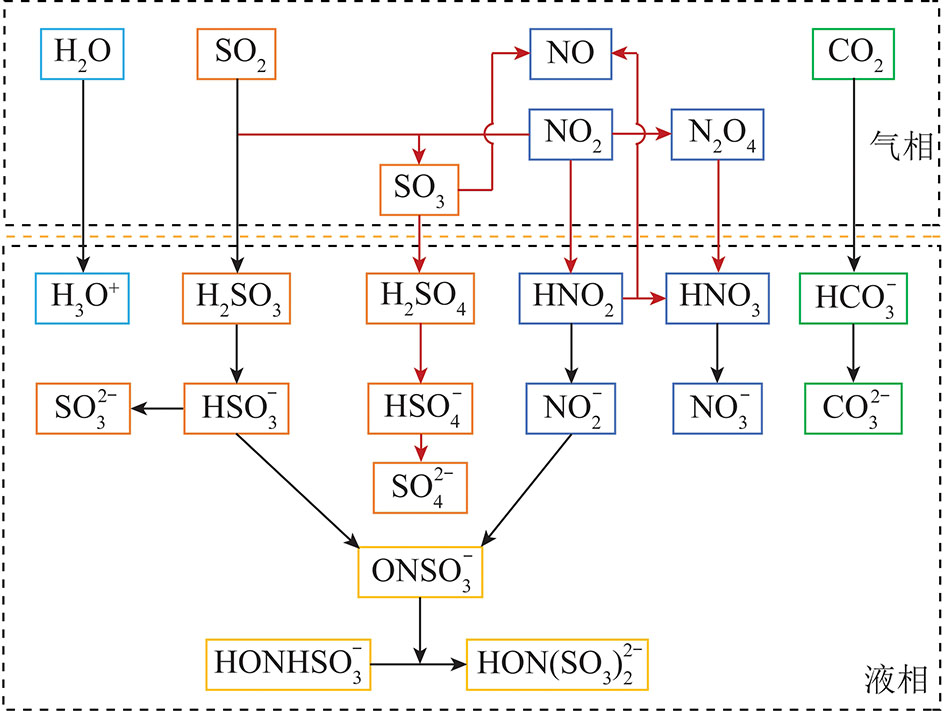
氨法脱硫脱硝工艺主要利用氨溶液吸收尾气中的SO2和NOx,将SO2转变为硫铵或亚硫胺,NOx转变为N2和水,进而降低污染物排放[150]。目前3种发展前景较好的脱硫脱硝工艺分别为氨/活性炭法、氨/电子束法及氨/脉冲电晕法。
3.3.1 氨/活性炭法
活性炭脱硫脱硝技术是一种先进的烟气进化技术,日本、德国等国家研究较多[151]。该工艺主要包括吸收、解吸和硫回收3部分:首先利用活性炭比表面积大、孔隙结构良好的特点将SO2和NOx吸附于微孔中,其中SO2在表面被氧化为SO3;随后向吸收塔中喷入氨,将NOx转变为N2同时形成硫铵;最后将活性炭加热至400 ℃进行解吸附。该方法由活性炭干法脱硫技术演化而来,通过选择一种性能较好的活性炭,将其与SCR脱硝法相结合,达到同时脱硫脱硝的目的。该过程副产物经济价值较好,在避免污染物排放的同时节约了硫资源,符合绿色可持续发展的生产理念[152]。具体化学反应式如下[151]:

(20)

(21)

(22)
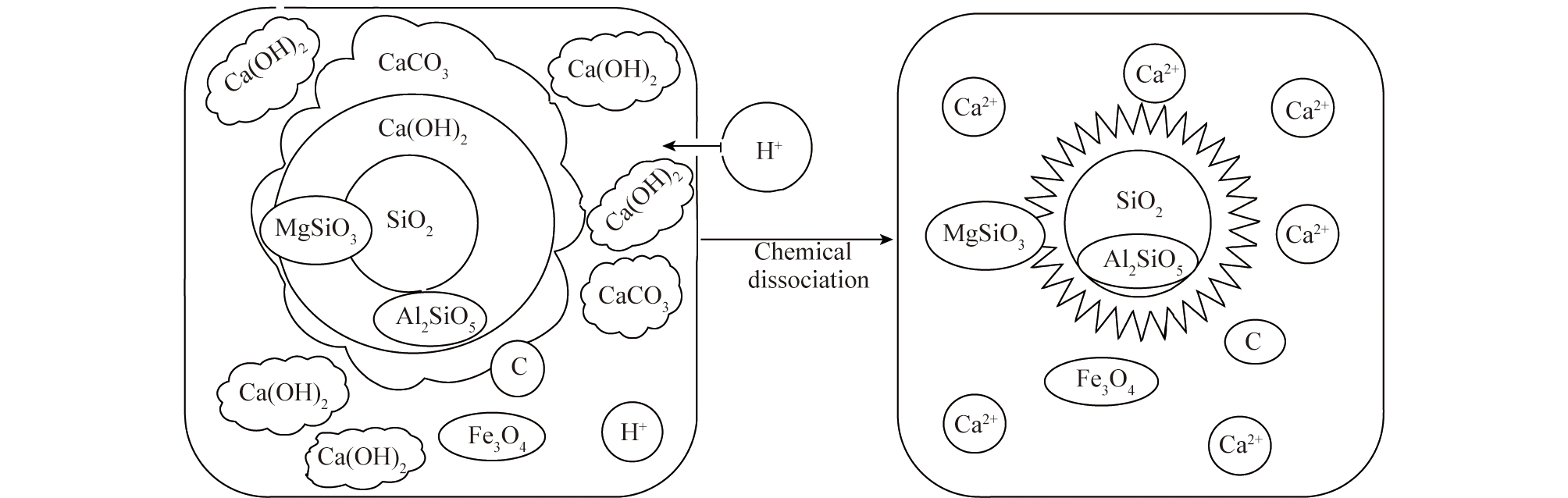
通常活性炭具有丰富的表面基团及较好的热稳定性,因此氨/活性炭法在长期、连续稳定运行时可达到98%的脱硫率和80%的脱硝率,且该过程对于SO3去除率也很高,同时活性炭还能吸附烟气中碳氢化合物及部分重金属[153],具有较好的商业应用价值。基于此,学者针对炭材料改性、烟气处理工艺及温度压力等多种因素对脱硫脱硝效果的影响规律和机理进行大量研究,以期进一步提高脱硝率。马双忱等[154]提出利用微波诱导活性炭催化还原脱硫脱硝技术,即利用活性炭自身吸附性能吸附饱和NO,再向活性炭载体中施加微波,将其还原成N2。杨丽敏等[155]采用光敏电阻研究了微波辐射功率、SO2浓度及杂质组分对活性炭吸附性能及脱硫效率的影响。结果表明经微波诱导放电脱硝后的活性炭表面化学含氧官能团增加,一定程度上改性了活性炭的化学吸附能力;随活性炭粒径增大,加热终温升高,微波诱导放电强度增大,促使脱硝效率回升,CO生成量随之增大。宋欣钰等[156]分析了比表面积、孔容和表面化学性质对脱硫脱硝性能的影响规律,活性炭的表面基团相比比表面积、孔容对其脱硫性能的影响更大。表面碱性基团对于酸性SO2的吸附有利,因此,可通过酸碱处理、金属氧化物负载及表面修饰等方式在活性炭表面引入合适的化学官能团或活性位点,提高活性炭对SO2、NOx的吸附能力,进而提高其脱硫脱硝性能。太原理工大学针对活性炭改性进行了一系列研究[157-158],如以添加新型非沥青黏结剂制成的非沥青基活性焦(NPAC)为研究对象,通过试验和仪器表征对其表面孔结构和酸碱官能团变迁以及脱硝活性进行研究。发现NPAC是实现低浓度SO2和NOx同时脱除的良好催化剂。以NPAC为载体,采用等体积浸渍法制备了一系列脱硝催化剂,研究了不同氧化物负载及不同煅烧温度、时间等对改性活性焦低温脱硝性能的影响,如图17所示。可知500 ℃焙烧1 h制备的NPAC-CoCeNi-7具有最佳低温脱硝活性;三聚氰胺浸渍5 h、500 ℃焙烧1.5 h制备的NPAC-N-Co(0.7)CeNi-8具有最佳的低温脱硝活性。

图17 改性活性焦低温脱硝性能比较[157]
Fig.17 Comparison of denitration performance of modified
activated coke at low temperature[157]
3.3.2 氨/电子束法
氨/电子束法(EBA法)研究最早可追溯到20世纪70年代初,该法由日本荏原公司和日本原子力研究所提出,此后40多年中,中国、美国、德国等均对其展开深入研究,规模也从小试、中试和工业示范逐步走向工业化。该方法主要通过高能电场产生高能电子束,采用电子束轰击降温增湿后的烟气,使烟气中各种组分解离产生OH、O3、O和OH2等强氧化性的自由基,进而氧化烟气中的SO2和NOx,最后用静电除尘器回收反应后的产物。
氨/电子束法因其SO2和NOx去除率较高,且无二次污染、脱硫剂利用率高、副产物可资源化利用等优点得到广泛关注。清华大学核能技术设计研究院徐光教授课题组在深入研究传统电子束烟气净化技术原理的基础上,提出了全新的电子束半干法烟气净化工艺[159],如图18所示,并建立了烟气处理量为10 000 m3/h的中试装置,验证得出:经过2 000 h运行,该装置脱硫率达95%,脱硝率达20%,副产品成分符合国家标准。在半干法工艺的基础上,针对烟气中SO2脱除,进一步提出了电子束深度氧化烟气净化技术。李亚冰等[160]在中试装置上进行SO2吸收和电子束辐照氧化试验,验证了电子束深度氧化烟气净化技术的可行性,发现其比半干法净化装置更简单,能耗更低,是一种具有广阔应用前景的烟气脱硫新技术。

图18 氨/电子束法工艺流程对比[159]
Fig.18 Comparison of ammonia/electron beam process flow[159]
为进一步提高脱硝率, 等[161]研究添加剂对NOx脱除效率的影响,发现加入NH3能显著提高NOx脱除效率,且NOx的脱除效率随吸收剂量的增加而增加。但氨/电子束法技术由于存在高价购买的进口核心部件电子加速器导致造价高、产生的辐射对人体及环境有危害、脱硫后烟气排放以及氨逃逸等问题[162-163],制约了其在国内的推广应用。
等[161]研究添加剂对NOx脱除效率的影响,发现加入NH3能显著提高NOx脱除效率,且NOx的脱除效率随吸收剂量的增加而增加。但氨/电子束法技术由于存在高价购买的进口核心部件电子加速器导致造价高、产生的辐射对人体及环境有危害、脱硫后烟气排放以及氨逃逸等问题[162-163],制约了其在国内的推广应用。
3.3.3 氨/脉冲电晕法
1986年,Masuda和Mizuno在氨/电子束法的基础上开发研制了脉冲电晕法[164]。2种技术的机理基本相同,区别在于高能电子产生的方式。脉冲电晕法是利用前沿陡峭、纳米级的窄脉冲电场加速得到高能电子,能在常温下将气体电离产生OH、O等大量活性粒子,从而将工业废气中的气体分子进行氧化降解,转化无害物。该工艺占地少且常温常压下有较好脱除率。
以往研究主要集中在排放参数、停留时间、气体种类和温度等运行参数对脱除效果的影响。同济大学机械与能源工程学院洪鎏团队则对脉冲电晕法脱硫脱硝的反应机理和动力学进行深入研究。HONG等[165]以水合联氨为添加剂,研究脉冲电晕法的NO脱除效率,并分析其反应机理。研究发现,联氨与脉冲电晕放电等离子体反应器生成的自由基发生反应,形成大量以氨基为主要成分的强还原性物质,可直接将NO还原为N2,有效防止N2O产生,从而实现NO减排。该团队通过模拟计算和试验研究对脉冲电晕法脱除SO2和NO的机理和动力学模型再次进行验证,揭示了脉冲电晕放电等离子体反应器中脱硫反应和脱硝反应的相互作用机制[166],为提高脉冲电晕法同时脱硫脱硝的性能提供了理论依据。
总体来说,氨法脱硫脱硝具有效率高、副产物便于利用等优点。但目前,氨/活性炭法脱硫脱碳技术仍存在活性炭消耗大、设备投资规模大、喷射氨造成管道阻塞等缺陷,氨/电子束法以及氨/脉冲电晕法则需进一步开发低能耗、高稳定性、低成本的技术。
4 结语与展望
自Haber-Bosch法合成氨问世后,一个多世纪的氨合成不仅解决了人类粮食问题,还推动了许多氨化工产业的生产与发展。然而其苛刻的反应条件及需要大量化石能源作为基础使Haber-Bosch法逐渐受限,化学链、光催化、电催化及等离子体等技术在Haber-Bosch法的基础上,避免了高温高压的反应条件,实现了温和条件下的氨合成,化学链合成氨技术能有效避免传统方法热力学与动力学之间的矛盾,碳基化学链技术虽然反应条件相对更严苛,但以H2O作为氢源大幅降低了生产成本,且副产物CO也能回收利用。这些技术有望实现合成氨工艺的节能环保、绿色高效,但总体而言,这些新技术目前仍停留在实验室研究阶段,离工业应用还有距离,加之Haber-Bosch法合成氨工艺建设完备,新的合成氨技术必须具有绝对优势才能推进合成氨工艺改革。
氨的能源化利用是当前研究热点。氨的掺混燃烧,H2燃烧速度快、放热量大,可有效促进氨燃烧,但会增加危险性;CH4由于其密度、黏度与NH3相似也被大量用于氨的掺混燃烧试验,但势必增加CO、CO2排放;氨与煤共燃无论是燃烧还是污染物排放均具有较大挑战。氨催化燃烧备受关注,各种催化剂相继被提出,而化学链燃烧有望为氨燃烧提供新方向,在促进燃烧的同时还能控制污染物排放,具有很好的研究价值。
除作为清洁能源,氨的其他化工潜力也得到广泛发展。氨制氢方面,多种贵金属催化剂以及非贵金属催化剂研究很多,非贵金属催化剂以其价格低廉,催化活性较稳定而更受青睐。氨法碳捕集技术发展较成熟,氨法脱硫脱硝技术由于其均相反应原理能有效降低烟气中的SOx与NOx,并由于氨的选择性反应,在一定条件下不会影响烟气中其他物质。这些技术的发展使氨化工应用更广泛,但氨大量使用也会带来氨逃逸等问题,目前多通过吸收剂吸收,也有学者研究了不同温区下氨的分解特性,将来有望通过合适的催化剂解决此类问题。总体来说,从氨合成到氨燃烧再到氨利用,氨化工正朝着绿色高效稳步发展。
[1] ERISMAN Jan Willem, SUTTON Mark A, GALLOWAY James, et al. How a century of ammonia synthesis changed the world[J]. Nature Geoscience, 2008, 1(10): 636-639.
[2] ZAMFIRESCU C, DINCER I. Ammonia as a green fuel and hydrogen source for vehicular applications[J]. Fuel Processing Technology, 2009, 90(5): 729-737.
[3] VALERA-MEDINA A, AMER-HATEM F, AZAD A K, et al. Review on ammonia as a potential fuel: From synthesis to economics[J]. Energy &Fuels, 2021, 35(9): 6964-7029.
[4] 林伟忠, 刘化章. 钌基氨合成催化剂研究进展[J]. 现代化工, 1994,14(7): 12-17.
LIN Weizhong, LIU Huazhang. Advances in research on ruthenium catalysts for ammonia synthesis[J]. Modern Chemical Industry,1994,14(7):12-17.
[5] 刘化章, 胡樟能, 李小年, 等. FeO基氨合成催化剂[J]. 化工学报, 1994,45(4): 385-392.
LIU Huazhang,HU Zhangneng,LI Xiaonian,et al. FeO based catalyst for ammonia synthesis[J]. CIESC Journal, 1994,45(4): 385-392.
[6] WANG Qianru, GUO Jianping, CHEN Ping. Recent progress towards mild-condition ammonia synthesis[J]. Journal of Energy Chemistry, 2019, 36(9): 25-36.
[7] VOJVODIC Aleksandra, MEDFORD Andrew James, STUDT Fe-lix, et al. Exploring the limits: A low-pressure, low-temperature haber-bosch process[J]. Chemical Physics Letters, 2014, 45(25): 108-112.
[8] HAGEN Stefan, BARFOD Rasmus, FEHRMANN Rasmus, et al.
Ammonia synthesis with barium-promoted iron-cobalt alloys supported on carbon[J]. Journal of Catalysis, 2003, 214(2): 327-335.
[9] TANG Ya, KOBAYASHI Yoji, MASUDA Naoya, et al. Metal-dependent support effects of oxyhydride-supported Ru, Fe, Co catalysts for ammonia synthesis[J]. Advanced Energy Materials, 2018, 8(36): 1801772.
[10] HATTORI Masashi, IIJIMA Shinya, NAKAO Takuya, et al. Sol-id solution for catalytic ammonia synthesis from nitrogen and hydrogen gases at 50 ℃[J]. Chemicals &Chemistry, 2020, 11(1): 2001.
[11] WANG Qianru, PAN Jaysree, GUO Jianping, et al. Ternary ruthenium complex hydrides for ammonia synthesis via the associative mechanism[J]. Nature Catalysis, 2021, 4(11): 959-967.
[12] LI Lingling, FEI Jiangya, ZHANG Tianhua, et al. Size sensit-ivity of supported Ru catalysts for ammonia synthesis: From nanoparticles to subnanometric clusters and atomic clusters[J]. Chem, 2021, 8(3): 749-768.
[13] REN Ke, ZHANG Tianzuo, TAN Xianfeng, et al. Life cycle assessment of ammonia synthesis based on pulverized coal entrained flow gasification technology in china[J]. Journal of Cleaner Production, 2021, 328: 129658.
[14] HABGOOD David C C, Hoadley Andrew F A, ZHANG Lian. Techno-economic analysis of gasification routes for ammonia production from victorian brown coal[J]. Chemical Engineering Research and Design, 2015, 102: 57-68.
[15] 刘化章. 传统合成氨工业转型升级的几点思考[J]. 化工进展, 2015, 34(10): 3509-3520.
LIU Huazhang. Transformation-upgrading and energy-saving of ammonia synthesis industry[J]. Chemical Industry and Engineering Progress, 2015, 34(10): 3509-3520.
[16] ZHANG Yueling, LIU Huan, LI Junjie. et al. Life cycle assessment of ammonia synthesis in China[J]. The International Journal of Life Cycle Assessment, 2022, 27(1): 50-61.
[17] 全国煤化工信息总站.2021年我国合成氨、尿素产能、产量、进出口量统计[J]. 煤化工, 2022, 50(3): 78.
[18] 王国祥. 煤气化技术在合成氨生产中的应用情况[J]. 氮肥技术, 2016, 37(2): 12-19.
WANG Guoxiang. Application of coal gasification technology in synthetic ammonia production[J]. Nitrogen Fertilizer Technology, 2016, 37(2): 12-19.
[19] 顾宗勤. 固定床间歇煤气化技术不应一刀切[J]. 中国石油和化工产业观察, 2021(S1): 46-48.
[20] 顾宗勤. 关于应重新认识固定床间歇煤气化技术的建议[J]. 化学工业, 2021, 39(1): 1-4.
GU Zhongqin. Recommendations for a new understanding of fixed-bed batch gasification technology[J]. Chemical Industry, 2021, 39(1): 1-4.
[21] 王翔. 新型煤气化与常压固定床煤气化工艺探讨:生产合成氨的能耗与污染物对比分析[J]. 氮肥技术, 2019, 40(6): 7-11.
WANG Xiang. Discussion on new coal gasification and atmospheric fixed bed gasification:Comparison and analysis of energy consumption and pollutants during synthetic ammonia production[J]. Nitrogen Fertilizer Technology, 2019, 40(6): 7-11.
[22] 周鹏,郎中敏. Ge水煤浆加压气化中粗煤气洗涤工艺的优化和设计[J]. 现代化工, 2018, 38(7): 194-198.
ZHOU Peng, LANG Zhongmin. Optimization and design of purification process for crude gas in pressurized gasification of Ge coal-water slurry[J]. Modern Chemical Industry, 2018, 38(7): 194-198.
[23] 曹军锋. 煤气化技术在合成氨生产中的应用情况[J]. 化工管理, 2019(14): 100-101.
[24] 李琼玖,杜世权,廖宗富,等.我国天然气制氨、尿素生产工艺发展前景[J].化肥设计, 2011, 49(3): 3-9,12.
LI Qiongjiu, DU Shiquan, LIAO Zongfu,et al. Discussion on developing prospect for making ammonia by natural gas and urea production in China[J]. Chemical Fertilizer Design, 2011, 49(3): 3-9,12.
[25] 李亮荣, 李秋平, 艾盛, 等. 传统化石与新型生物质能源重整制氢研究现状[J].化学与生物工程, 2021, 38(11): 1-6.
LI Liangrong, LI Qiuping, AI Sheng, et al. Research status of hydrogen production from reforming of fossil energy and new biomass energy[J]. Chemistry &Bioengineering, 2021, 38(11): 1-6.
[26] 侯建国, 单彤文, 张超, 等. 小型橇装天然气制氢技术现状与发展趋势分析[J].天然气化工(C1化学与化工), 2021, 46(3): 1-6.
HOU Jianguo, SHAN Tongwen, ZHANG Chao, et al. Current situation and development trend analysis of small skid mounted natural gas hydrogen production technology[J]. Natural Gas Chemical Industry, 2021, 46(3): 1-6.
[27] SMITH C, HILL A K, TORRENTE-MURCIANO L. Current and future role of Haber-Bosch ammonia in a carbon-free energy landscape[J]. Energy &Environmental Science, 2020, 13(2): 331-344.
[28] 高阳, 郭凯凯, 李琪, 等. 浙江沿海地区可再生能源制氢的成本研究[J]. 能源工程, 2022, 42(3): 45-49.
GAO Yang, GUO Kaikai, LI Qi, et al. Research on the cost of hydrogen production from renewable energy in coastal areas of Zhejiang[J]. Energy Engineering, 2022, 42(3): 45-49.
[29] 李志军, 刘京京, 陈爱琴, 等.可再生能源转化为氨氢能源体系技术和经济性分析[J]. 上海节能, 2022(9): 1125-1131.
LI Zhijun, LIU Jingjing, CHEN Aiqin, et al. Technical and economic analysis on renewable energy conversion to ammonia hydrogen energy system[J]. Shanghai energy conservation, 2022(9): 1125-1131.
[30] 徐也茗, 郑传明, 张韫宏. 氨能源作为清洁能源的应用前景[J]. 化学通报, 2019, 82(3): 214-220.
XU Yeming, ZHENG Chuanming, ZHANG Yunhong. Applicat-ion prospect of ammonia energy as clean energy[J]. Chemistry Bulletin, 2019, 82(3): 214-220.
[31] 王月姑. 以氨为燃料和载氢介质的生命周期能效和环境效益分析[D]. 厦门:厦门大学, 2019.
[32] XIONG Chuhao, WU Ye, FENG Mingqian, et al. High thermal stability Si-Al based N-carrier for efficient and stable chemical looping ammonia generation[J]. Applied Energy, 2022, 323: 119519.
[33] LIU Huazhang. Ammonia synthesis catalyst 100 years: Practice, enlightenment and challenge[J]. Chinese Journal of Catalysis, 2014, 35(10): 1619-1640.
[34] MICHALSKY R, AVRAM A M, PETERSON B A, et al. Che-
mical looping of metal nitride catalysts: Low-pressure ammonia synthesis for energy storage[J]. Chemical Science, 2015, 6(7): 3965-3974.
[35] WANG Baoyi, GUO Huixin, YIN Xianglei, et al. N-sorption capability of Al2O3-supported Mn-/Fe-based nitrogen carriers during chemical looping ammonia synthesis technology[J]. Energy &Fuels, 2020, 34(8): 10247-10255.
[36] AFRAMEHR Wrya Mohammadi, PFROMM Peter H. Activating dinitrogen for chemical looping ammonia synthesis: Nitridation of manganese[J]. Journal of Materials Science, 2021, 56(22): 12584-12595.
[37] GAO Wenbo, GUO Jianping, WANG Peikun, et al. Production of ammonia via a chemical looping process based on metal imides as nitrogen carriers[J]. Nature Energy, 2018, 3(12): 1067-1075.
[38] YAN Hanxue, GAO Wenbo, WANG Qianru, et al. Lithium palladium hydride promotes chemical looping ammonia synthesis mediated by lithium imide and hydride[J]. The Journal of Physical Chemistry C, 2021, 125(12): 6716-6722.
[39] LAASSIRI Said, ZEINALIPOUR-YAZDI Constantinos D,CATL-OW C Richard A. The potential of manganese nitride based materials as nitrogen transfer reagents for nitrogen chemical looping[J]. Applied Catalysis B: Environmental, 2018, 223: 60-66.
[40] FENG Sheng, GAO Wenbo, WANG Qianru, et al. A multi-functional composite nitrogen carrier for ammonia production via a chemical looping route[J]. Journal of Materials Chemistry A, 2021, 9(2): 1039-1047.
[41] G LVEZ M E, HALMANN M, STEINFELD A. Ammonia production via a two-step Al2O3/AlN thermochemical cycle. 1. Thermodynamic, environmental, and economic analyses[J]. Industrial &Engineering Chemistry Research, 2007, 46(7): 2042-2046.
LVEZ M E, HALMANN M, STEINFELD A. Ammonia production via a two-step Al2O3/AlN thermochemical cycle. 1. Thermodynamic, environmental, and economic analyses[J]. Industrial &Engineering Chemistry Research, 2007, 46(7): 2042-2046.
[42] TSUGE A, INOUE H, KASORI Mituo, et al. Raw material ef-fect on ain powder synthesis from Al2O3 carbothermal reduction[J]. Journal of Materials Science, 1990,25(5): 2359-2361.
[43] FORSLUND B, ZHENG J. Carbothermal synthesis of aluminium nitride at elevated nitrogen pressures. I. Effect of process parameters on conversion rate[J]. Journal of Materials Science, 1993,28(12): 3125-3131.
[44] WANG Qi, CUI Wei, GE Yiyao, et al. Carbothermal synthesis of spherical aln granules: Effects of synthesis parameters and Y2O3 additive[J]. Ceramics International, 2015, 41(5): 6715-6721.
[45] ZHANG Quan, WU Ye, GAO Yuan, et al. High-performa-nce mesoporous (AlN/Al2O3) for enhanced NH3 yield during chemical looping ammonia generation technology[J]. International Journal of Hydrogen Energy, 2020, 45(16): 9903-9913.
[46] BARTEL Christopher J, MUHICH Christopher L, WEIMER Alan W, et al. Aluminum nitride hydrolysis enabled by hydroxyl-mediated surface proton hopping[J]. ACS Applied Materials &Interfaces, 2016, 8(28): 18550-18559.
[47] GAO Yuan, WU Ye, ZHANG Quan, et al. N-desorption or NH3 generation of TiO2-loaded Al-based nitrogen carrier during chemical looping ammonia generation technology[J]. International Journal of Hydrogen Energy, 2018, 43(34): 16589-16597.
[48] WU Ye, GAO Yuan, ZHANG Quan, et al. Promising zirconia-
mixed Al-based nitrogen carriers for chemical looping of NH3: Reduced NH3 decomposition and improved NH3 yield[J]. Fuel, 2020, 264: 116821.
[49] 吴烨, 冯鸣谦, 方婧,等. 化学链合成氨技术研究进展及展望[J]. 洁净煤技术, 2021, 27(2): 92-106.
WU Ye,FENG Mingqian,FANG Jing, et al. Research progress and prospect of ammonia synthesis technology[J]. Clean Coal Technology, 2021, 27(2): 92-106.
[50] 范天熙. MOFs催化剂制备及其低温电催化合成氨性能[D]. 北京:北京化工大学, 2016: 17-21.
[51] KYRIAKOU V, GARAGOUNIS I, VASILEIOU E, et al. Prog-
ress in the electrochemical synthesis of ammonia[J]. Catalysis Today, 2016, 286: 2-13.
[52] STUART Licht, CUI Baochen, WANG Baohui, et al. Ammonia synthesis by N2 and steam electrolysis in molten hydroxide suspensions of nanoscale Fe2O3[J]. Science, 2014, 345: 637-640.
[53] QIU Weibin, XIE Xiaoying, QIU Jianding, et al. High-performance artificial nitrogen fixation at ambient conditions using a metal-free electrocatalyst[J]. Nature Communications, 2018, 9(1): 3485.
[54] LI Xia, WU Xiufeng, WANG Yuan, et al. S-doped carbon na-nospheres: An efficient electrocatalyst toward artificial N2 fixation to NH3[J]. Small Methods, 2019, 3(6): 1800251.
[55] ZHAO Jingxiang, CHEN Zhongfang. Single Mo atom supported on defective boron nitride monolayer as an efficient electrocatalyst for nitrogen fixation: A computational study[J]. Journal of the American Chemical Society, 2017, 139(36): 12480-12487.
[56] LIU Sisi, WANG Mengfan, QIAN Tao, et al. Facilitating nit-rogen accessibility to boron-rich covalent organic frameworks via electrochemical excitation for efficient nitrogen fixation[J]. Nature Communications, 2019, 10(1): 3898.
[57] SURYANTO Bryan H R, DU Hoang Long, WANG Dabin, et al. Challenges and prospects in the catalysis of electroreduction of nitrogen to ammonia[J]. Nature Catalysis, 2019, 2(4): 290-296.
[58] SURYANTO Bryan H R, MATUSZEK Karolina, CHOI Jaecheol, et al. Nitrogen reduction to ammonia at high efficiency and rates based on a phosphonium proton shuttle[J]. Science, 2021, 372: 1187-1191.
[59] REN Yongwen, YU Chang, TAN Xinyi, et al. Strategies to suppress hydrogen evolution for highly selective electrocatalytic nitrogen reduction: Challenges and perspectives[J]. Energy &Environmental Science, 2021, 14(3): 1176-1193.
[60] SCHRAUZER G N,GUTH T D. Photolysis of water and photoreduction of nitrogen on titanium dioxide[J]. Journal of the American Chemical Society, 1977, 99(22): 7189-7193.
[61] ZHU Di, ZHANG Linghong, RUTHER Rose E,et al. Photo-illuminated diamond as a solid-state source of solvated electrons in water for nitrogen reduction[J]. Nature Materials, 2013, 12(9): 836-841.
[62] LI Hao, SHANG Jian, AI Zhihui, et al. Efficient visible light nitrogen fixation with biobr nanosheets of oxygen vacancies on the exposed {001} facets[J]. Journal of the American Chemical Society, 2015, 137(19): 6393-6399.
[63] HIRAKAWA Hiroaki, HASHIMOTO Masaki, SHIRAISHI Yasuhiro, et al. Photocatalytic conversion of nitrogen to ammonia with water on surface oxygen vacancies of titanium dioxide[J]. Journal of the American Chemical Society, 2017, 139(31): 10929-10936.
[64] ZHAO Yufei, ZHAO Yunxuan, WATERHOUSE Geoffrey I N, et al. Layered-double-hydroxide nanosheets as efficient visible-light-driven photocatalysts for dinitrogen fixation[J]. Advanced Materials, 2017, 29(42): 1703828.
[65] ZHANG Ning, JALIL Abdul, WU Daoxiong, et al. Refining de-fect states in W18O49 by Mo doping: A strategy for tuning N2 activation towards solar-driven nitrogen fixation[J]. Journal of the American Chemical Society, 2018, 140(30): 9434-9443.
[66] HAN Qing, WU Chongbei, JIAO Haimiao, et al. Rational design of high-concentration Ti3 in porous carbon-doped TiO2 nanosheets for efficient photocatalytic ammonia synthesis[J]. Advanced Materials, 2021, 33(9): 2008180.
[67] HU Canyu, CHEN Xing, JIN Jianbo, et al. Surface plasmon enabling nitrogen fixation in pure water through a dissociative mechanism under mild conditions[J]. Journal of the American Chemical Society, 2019, 141(19): 7807-7814.
[68] WINTER Lea R, ASHFORD Bryony, HONG Jungmi, et al. Identifying surface reaction intermediates in plasma catalytic ammonia synthesis[J]. ACS Catalysis, 2020, 10(24): 14763-14774.
[69] LI Laiquan, TANG Cheng, CUI Xiaoyang, et al. Efficient nitro-gen fixation to ammonia through integration of plasma oxidation with electrocatalytic reduction[J]. Angewandte Chemie, 2021, 60(25): 14131-14137.
[70] WANG Yaolin, CRAVEN Michael, YU Xiaotong, et al. Plasma-enhanced catalytic synthesis of ammonia over a Ni/Al2O3 catalyst at near-room temperature: Insights into the importance of the catalyst surface on the reaction mechanism[J]. ACS Catalysis, 2019, 9(12): 10780-10793.
[71] WANG Yaolin, YANG Wenjie, XU Shanshan, et al. Shielding protection by mesoporous catalysts for improving plasma-catalytic ambient ammonia synthesis[J]. Journal of the American Chemical Society, 2022, 144(27):12020-12031.
[72] BIOCHE Kévin, BRICTEUX Laurent, BERTOLINO Andrea, et al. Large eddy simulation of rich ammonia/hydrogen/air combustion in a gas turbine burner[J]. International Journal of Hydrogen Energy, 2021, 46(79): 39548-39562.
[73] HAN Xinlu, WANG Zhihua, COSTA Mário, et al. Experimental and kinetic modeling study of laminar burning velocities of NH3/air, NH3/H2/air, NH3/CO/air and NH3/CH4/air premixed flames[J]. Combustion and Flame, 2019, 206: 214-226.
[74] LEE J H, LEE S I, KWON O C. Effects of ammonia substitution on hydrogen/air flame propagation and emissions[J]. International Journal of Hydrogen Energy, 2010, 35(20): 11332-11341.
[75] KUMAR Praveen, MEYER Terrence R . Experimental and modeling study of chemical-kinetics mechanisms for H2-NH3-air mixtures in laminar premixed jet flames[J]. Fuel, 2013, 108: 166-176.
[76] DUYNSLAEGHER C, JEANMART H, VANDOOREN J. Flame structure studies of premixed ammonia/hydrogen/oxygen/argon flames: Experimental and numerical investigation[J]. Proceedings of the Combustion Institute, 2009, 32(1): 1277-1284.
[77] DAI Liming, GERSEN Sander, GLARBORG Peter, et al. Autoignition studies of NH3/CH4 mixtures at high pressure[J]. Combustion and Flame, 2020, 218: 19-26.
[78] SHU Tao, XUE Yuan, ZHOU Zijun, et al. An experimental stu-dy of laminar ammonia/methane/air premixed flames using expanding spherical flames[J]. Fuel, 2021, 290: 120003.
[79] OKAFOR Ekenechukwu C, NAITO Yuji, COLSON Sophie, et al. Experimental and numerical study of the laminar burning velocity of CH4-NH3-air premixed flames[J]. Combustion and Flame, 2018, 187: 185-198.
[80] XIAO Hua, VALERA-MEDINA Agustin, BOWEN Philip J.
Study on premixed combustion characteristics of co-firing ammonia/methane fuels[J]. Energy, 2017, 140: 125-135.
[81] LI Rui, KONNOV Alexander A, HE Guoqiang, et al. Chemical mechanism development and reduction for combustion of NH3/H2/CH4 mixtures[J]. Fuel, 2019, 257: 116059.
[82] OKAFOR Ekenechukwu Chijioke, NAITO Yuji, COLSON So-phie,et al. Measurement and modelling of the laminar burning velocity of methane-ammonia-air flames at high pressures using a reduced reaction mechanism[J]. Combustion and Flame, 2019, 204: 162-175.
[83] XIAO Hua, LAI Shini, VALERA-MEDINA Agustin, et al. St-udy on counterflow premixed flames using high concentration ammonia mixed with methane[J]. Fuel, 2020, 275: 117902.
[84] RAMOS C Filipe, ROCHA Rodolfo C, OLIVEIRA Pedro M R, et al. Experimental and kinetic modelling investigation on NO, CO and NH3 emissions from NH3/CH4/air premixed flames[J]. Fuel, 2019, 254: 115693.
[85] TIAN Zhenyu, LI Yuyang, ZHANG Lidong, et al. An experimental and kinetic modeling study of premixed NH3/CH4/O2/Ar flames at low pressure[J]. Combustion and Flame, 2009, 156(7): 1413-1426.
[86] CHAI Wai Siong, BAO Yulei, JIN Pengfei, et al. A review on ammonia, ammonia-hydrogen and ammonia-methane fuels[J]. Renewable and Sustainable Energy Reviews, 2021, 147: 111254.
[87] TAKIZAWA Kenji, TAKAHASHI Akifumi, TOKUHASHI Kazuaki, et al. Burning velocity measurements of nitrogen-containing compounds[J]. Journal of Hazardous Materials, 2008, 155(1/2): 144-152.
[88] ROCHA Rodolfo C, ZHONG Shenghui, XU Leilei, et al. Structure and laminar flame speed of an ammonia/methane/air premixed flame under varying pressure and equivalence ratio[J]. Energy &Fuels, 2021, 35(9): 7179-7192.
[89] SOMARATHNE Kapuruge Don Kunkuma Amila, OKAFOR Ekenechukwu C, SUGAWARA Daiki, et al. Effects of OH concentration and temperature on no emission characteristics of turbulent non-premixed CH4/NH3/air flames in a two-stage gas turbine like combustor at high pressure[J]. Proceedings of the Combustion Institute, 2021, 38(4): 5163-5170.
[90] SUN Yuze, CAI Tao, ZHAO Dan. Thermal performance and NOx emission characteristics studies on a premixed methane-ammonia-fueled micro-planar combustor[J]. Fuel, 2021, 291: 120190.
[91] OKAFOR Ekenechukwu C, YAMASHITA Hirofumi, HAYAK-AWA Akihiro, et al. Flame stability and emissions characteristics of liquid ammonia spray co-fired with methane in a single stage swirl combustor[J]. Fuel, 2021, 287: 119433.
[92] XIA Yu, HADI Khalid, HASHIMOTO Genya, et al. Effect of ammonia/oxygen/nitrogen equivalence ratio on spherical turbulent flame propagation of pulverized coal/ammonia co-combustion[J]. Proceedings of the Combustion Institute, 2020, 38(3): 4043-4052.
[93] HADI Khalid, ICHIMURA Ryo, HASHIMOTO Genya, et al. Effect of fuel ratio of coal on the turbulent flame speed of ammonia/coal particle cloud co-combustion at atmospheric pressure[J]. Proceedings of the Combustion Institute, 2020, 38(3): 4131-4139.
[94] 朱京冀, 徐义书, 徐静颖, 等. 掺烧氨燃料对煤挥发分火焰特性及颗粒物生成的影响[J]. 发电技术, 2022, 43(6): 1-10.
ZHU Jingji, XU Yishu, XU Jingying, et al. Effect of co-firing ammonia on coal volatile matter flame characteristics and particulate matter formation behaviours[J]. Power Generation Technology, 2022, 43(6): 1-10.
[95] LEE Hookyung, LEE MinJung. Recent advances in ammonia
combustion technology in thermal power generation system for carbon emission reduction[J]. Energies, 2021, 14(18): 5604-5604.
[96] YAMAMOTO A, KIMOTO M, OZAWA Y, et al. Basic co-firing characteristics of ammonia with pulverized coal in a single burner test furnace[C]//2018 AIChE Annual Meeting. Pittsburgh: AIChE, 2018.
[97] ISHII Hiroki, OHNO Emi, KOZAKI Takahiro, et al. Developm-ent of co-firing technology of pulverized coal and ammonia for suppressing the NOx generation[J]. Transactions of the JSME, 2020, 883(86): 19-00363.
[98] TAMURA Masato, GOTOU Takahiro, ISHII Hiroki, et al. Experimental investigation of ammonia combustion in a bench scale 1.2 MW-thermal pulverised coal firing furnace[J]. Applied Energy, 2020, 277: 115580.
[99] ITO Takamasa, ZHANG Juwei, ISHIHARA Sakiko, et al. Development of the coal co-firing technology with ammonia and numerical evaluation of the boiler performance[J]. Journal of the Combustion Society of Japan, 2019, 61(198): 304-308.
[100] WANG Xin, FAN Weidong, CHEN Jun, et al. Experimental study and kinetic analysis of the impact of ammonia co-firing ratio on products formation characteristics in ammonia/coal co-firing process[J]. Fuel, 2022, 329: 125496.
[101] ZHANG Juwei, ITO Takamasa, ISHII Hiroki, et al. Numerical investigation on ammonia co-firing in a pulverized coal combustion facility: Effect of ammonia co-firing ratio[J]. Fuel, 2020, 267: 117166.
[102] CARDOSO João Sousa, SILVA Valter, EUSÉBIO Daniela, et al. Numerical modelling of ammonia-coal co-firing in a pilot-scale fluidized bed reactor: Influence of ammonia addition for emissions control[J]. Energy Conversion and Management, 2022, 254: 115226.
[103] CHEN Ping, FANG Yao, WANG Peipei, et al. The effect of ammonia co-firing on no heterogeneous reduction in the high-temperature reduction zone of coal air-staging combustion: Experimental and quantum chemistry study[J]. Combustion and Flame, 2022, 237: 111857.
[104] AKBARI Ehsan, ALAVI Seyed Mehdi, REZAEI Mehran, et al. CeO2-promoted bao-mnox catalyst for lean methane catalytic combustion at low temperatures: Improved catalytic efficiency and light-off temperature[J]. International Journal of Hydrogen Energy, 2022, 47(26): 13004-13021.
[105] HINOKUMA Satoshi, ARAKI Kento, IWASA Takeshi. et al. Ammonia-rich combustion and ammonia combustive decomposition properties of various supported catalysts[J]. Catalysis Communications, 2019, 123: 64-68.
[106] ISUPOVA L A, SUTORMINA E F, KULIKOVSKAYA N A, et al. Honeycomb supported perovskite catalysts for ammonia oxidation processes[J]. Catalysis Today, 2005, 105(3/4): 429-435.
[107] PINAEVA L G, DOVLITOVA L S, ISUPOVA L A. Monolithic FeOx/Al2O3 catalysts for ammonia oxidation and nitrous oxide decomposition[J]. Chemicals &Chemistry, 2017, 2(58): 183-195.
[108] HINOKUMA Satoshi, MATSUKI Shun, KAWABATA Yusuke, et al. Copper oxides supported on aluminum oxide borates for catalytic ammonia combustion[J]. Journal of Physical Chemistry C, 2016, 43: 24734-24742.
[109] HINOKUMA Satoshi, KIRITOSHI Saaya, KAWABATA Yus-uke, et al. Catalytic ammonia combustion properties and operando characterization of copper oxides supported on aluminum silicates and silicon oxides[J]. Journal of Catalysis, 2018, 361: 267-277.
[110] HINOKUMA Satoshi , IWASA Takeshi, ARAKI Kento, et al. Ammonia combustion properties of copper oxides-based honeycomb and granular catalysts[J]. Journal of the Japan Petroleum Institute, 2020, 63(5): 274-281.
[111] SHRESTHA S, HAROLD M P, KAMASAMUDRAM K, et al.
Selective oxidation of ammonia to nitrogen on Bi-functional Cu-SSZ-13 and Pt/Al2O3 monolith catalyst[J]. Catalysis Today, 2016, 267:130-144.
[112] HINOKUMA Satoshi, SATO Kazuhiko. Ammonia combustion catalysts[J]. Chemistry Letters, 2021, 50(4): 752-759.
[113] WU Ye, MEI Jian, CAI Tianyi. et al. Reducing the NOx emissions during NH3 oxidation with nickel modified Fe2O3:A promising cost-effective and environmentally friendly catalyst for NH3 combustion[J]. Combustion and Flame, 2022, 237: 111845.
[114] GLARBORG P, JENSEN A D, JOHNSSON J E. Fuel nitrogen conversion in solid fuel fired systems[J]. Progress in Energy and Combustion Science, 2003, 29(2): 89-113.
[115] MAYRHUBER S, NORMANN F, YILMAZ D, et al. Effect of the oxygen carrier ilmenite on NOx formation in chemical-looping combustion[J]. Fuel Processing Technology, 2021, 222(10): 106962.
[116] LEPP LAHTI J, SIMELL P, KURKELA E. Catalytic conver-sion of nitrogen compounds in gasification gas[J]. Fuel Processing Technology, 1991, 29(1/2): 43-56.
LAHTI J, SIMELL P, KURKELA E. Catalytic conver-sion of nitrogen compounds in gasification gas[J]. Fuel Processing Technology, 1991, 29(1/2): 43-56.
[117] GU Haiming, SHEN Laihong, ZHONG Zhaoping, et al. NO release during chemical looping combustion with iron ore as an oxygen carrier[J]. Chemical Engineering Journal, 2015, 264: 211-220.
[118] HAYHURST N A, LAWRENCE A D , et al. The reduction of the nitrogen oxides NO and N2O to molecular nitrogen in the presence of iron, its oxides, and carbon monoxide in a hot fluidized bed[J]. Combustion and Flame, 1997, 110(3): 351-365.
[119] ADANEZ J, ABAD A, GARCIA-LABIANO F, et al. Progress in chemical-looping combustion and reforming technologies[J]. Progress in Energy &Combustion Science, 2012, 38(2): 215-282.
[120] LYNGFELT A. Oxygen carriers for chemical looping combustion: 4 000 h of operational experience[J]. Oil &Gas Science and Technology - Revue d IFP Energies nouvelles, 2011, 66(2): 161-172.
[121] CHENG Mao, NORMANN Fredrik, ZHAO Dongmei, et al. Oxidation of ammonia by ilmenite under conditions relevant to chemical-looping combustion[J]. Energy &Fuels, 2015, 29(12): 8126-8134.
[122] NORMANN Fredrik, WISMER A O, MÜLLER C R, et al. Oxidation of ammonia by iron, manganese and nickel oxides - implications on NOx formation in chemical-looping combustion[J]. Fuel, 2019, 240: 57-63.
[123] QIN Wu, LUO Laixing, FENG Anwen, et al. Ammonia deep chemical looping combustion on perfect and reduced Fe2O3: A theoretical account[J]. International Journal of Energy Research, 2021, 45(7): 10562-10571.
[124] DI CARLO Andrea, VECCHIONE Luigi, DEL PRETE Zaccaria. Ammonia decomposition over commercial Ru/Al2O3 catalyst: An experimental evaluation at different operative pressures and temperatures[J]. International Journal of Hydrogen Energy, 2014, 39(2): 808-814.
[125] HUANG Chuanqing, YU Yingzhi, YANG Jinmei, et al. Ru/La2O3 catalyst for ammonia decomposition to hydrogen[J]. Applied Surface Science, 2019, 476: 928-936.
[126] CHIUTA Steven, EVERSON Raymond C, NEOMAGUS Hein W J P, et al. Hydrogen production from ammonia decomposition over a commercial Ru/Al2O3 catalyst in a microchannel reactor: Experimental validation and CFD simulation[J]. International Journal of Hydrogen Energy, 2016, 41(6): 3774-3785.
[127] 琳石, 铁于, 王欣全, 等. NH3-SCR反应过程中NH3和NOx在Cu/SAPO-34分子筛催化剂上的吸附特性和作用[J]. 物理化学学报, 2013, 29 (7): 1550-1557.
LIN Shi, TIE Yu, WANG Xinquan, et al. Properties and roles of adsorbed NH3 and NOx over Cu/SAPO-34 zeolite catalyst in NH3-SCR process[J]. Acta Physico-Chimica Sinica, 2013, 29 (7): 1550-1557.
[128] MUROYAMA Hiroki, SABURI Chikara, MATSUI Toshiaki, et al. Ammonia decomposition over Ni/La2O3 catalyst for on-site generation of hydrogen[J]. Applied Catalysis A: General, 2012, 443/444: 119-124.
[129] CAO Jianliang, YAN Zhaoli, DENG Qingfang, et al. Homogeneous precipitation method preparation of modified red mud supported ni mesoporous catalysts for ammonia decomposition[J]. Catalysis Science &Technology, 2014, 4(2): 361-368.
[130] CAO Jianliang, YAN Zhaoli, DENG Qingfang, et al. Mesoporous modified-red-mud supported ni catalysts for ammonia decomposition to hydrogen[J]. International Journal of Hydrogen Energy, 2014, 39(11): 5747-5755.
[131] LI L, CHEN F, DAI Y, et al. Fe-assisted Ru clusters su-pported on porous and graphitic carbon for ammonia decomposition to COx free hydrogen[J]. RSC Advances, 2016,104: 102336-102342.
[132] ZHANG Jian, MÜLLER Jens Oliver, ZHENG Weiqing, et al. Individual Fe-Co alloy nanoparticles on carbon nanotubes: Structural and catalytic properties[J]. Nano Letters, 2008, 8(9): 2738-2743.
[133] 黄斌, 许世森, 郜时旺, 等. 华能北京热电厂CO2捕集工业试验研究[J]. 中国电机工程学报, 2009, 29(17): 14-20.
HUANG Bin, XU Shisen, GAO Shiwang, et al. Industrial test of CO2 capture in huaneng beijing coal-fired power station[J]. Proceedings of the CSEE, 2009, 29(17): 14-20.
[134] AN Chin Yeh, BAI Hsunling. Comparison of ammonia and monoethanolamine solvents to reduce CO2 greenhouse gas emissions[J]. The Science of the Total Environment, 1999, 228 (2/3): 121-133.
[135] 胡璐. 氨法碳捕集技术再生过程研究[D]. 武汉:江汉大学, 2017.
[136] ZHANG Yun, LI Zhen, LI Chengjun, et al. Experimental study on sequestrating of CO2 in the true flue gas by ammonia spray and producing NH4HCO3[J]. Hot Working Technology, 2003, 562-566.
[137] 刁永发, 郑显玉, 陈昌和. 氨水洗涤脱除CO2温室气体的机理研究[J]. 环境科学学报, 2003, 23(6): 753-757.
DIAO Yongfa, ZHENG Xianyu, CHEN Changhe. Study on removal mechanism of CO2 greenhouse gas by ammonia scrubbing[J]. Acta Scientiae Circumstantiae, 2003, 23(6):753-757.
[138] YEH James T, RESNIK Kevin P, RYGLE Kathy, et al. Semi-batch absorption and regeneration studies for CO2 capture by aqueous ammonia[J]. Fuel Processing Technology, 2005, 86(14/15): 1533-1546.
[139] 钦淑均, 郑志胜, 张成芳, 等. 纯氨水吸收二氧化碳的速率研究[J]. 华东化工学院学报, 1983(2): 155-167.
QIN Shujun, ZHENG Zhisheng, ZHANG Chenfang, et al. A study on absorption rate of CO2 into pure ammonia aqueous solutions[J]. Journal of East China Institute of Chemical Technology, 1983(2): 155-167.
[140] 郑志胜, 钦淑均, 沈小耀, 等. 低碳化度氨水吸收二氧化碳速率的研究[J]. 华东化工学院学报, 1984(2): 137-146.
ZHENG Zhisheng, QIN Shujun, SHEN Xiaoyao, et al. A study on absorption rates of CO2 into low degree carbonated ammonia-water solutions[J]. Journal of East China Institute of Chemical Technology, 1984(2): 137-146.
[141] 张成芳, 郑志胜, 钦淑均, 等. 碳化氨水解吸二氧化碳的研究[J]. 华东化工学院学报, 1987,13(2): 175-182.
ZHANG Chengfang, ZHENG Zhisheng, QIN Shujun, et al. A study on desorption of CO2 from carbonated ammonia-water solution[J]. Journal of East China Institute of Chemical Technology, 1987, 13(2): 175-182.
[142] BAI Hsunling,YEH An Chin. Removal of CO2 greenhouse gas by ammonia scrubbing[J]. Industrial &Engineering Chemistry Research, 1997, 36(6): 2490-2493.
[143] 马双忱, 王梦璇, 孙云雪, 等. 氨水与MEA的CO2捕集对比研究[J]. 动力工程学报, 2012, 32(1): 52-58.
MA Shuangchen, WANG Mengxuan, SUN Yunxue, et al. Efficiency comparison of CO2 removal respectively with ammonia solution and MEA[J]. Chinese Journal of Power Engineering, 2012, 32(1): 52-58.
[144] TORO-MOLINA Carol, BOUALLOU Chakib. Comparison of post-combustion CO2 capture by solutions of ammonia and organic amines: Assessment using direct and indirect contactors[J]. Energy Procedia, 2014, 63: 550-558.
[145] 张君, 公茂利, 荚江霞, 等. 超重场强化氨水吸收烟道气中CO2的研究[J]. 安徽理工大学学报(自然科学版), 2006, 26(1): 48-51.
ZHANG Jun, GONG Maoli, GU Jiangxia, et al. Study on removal of low concentration CO2 from flue gas by aqueous ammonia under higee at normal atmosphere[J]. Journal of Anhui University of Science and Technology, 2006, 26(1): 48-51.
[146] 张茂, 赛俊聪, 吴少华, 等. 氨法脱除燃煤烟气中CO2的实验研究[J]. 热能动力工程, 2008, 23(2): 191-194.
ZHANG Mao, SAI Juncong, WU Shaohua, et al. Experimental study of the removal of CO2 from coal fired flue gas by using ammonia[J]. Journal of Engineering for Thermal Energy and Power, 2008, 23(2): 191-194.
[147] 马双忱, 孙云雪, 赵毅, 等. 氨水捕集模拟烟气中二氧化碳的实验与理论研究[J]. 化学学报, 2011, 69(12): 1469-1474.
MA Shuangchen, SUN Yunxue, ZHAO Yi, et al. Experimental and mechanism research on CO2 capture from simulating flue gas using ammonia solution[J]. Acta Chimica Sinica, 2011, 69(12): 1469-1474.
[148] BAK C U, ASIF M, KIM W S. Experimental study on CO2 capture by chilled ammonia process[J]. Chemical Engineering Journal, 2015, 265: 1-8.
[149] TORO Molina Carol, BOUALLOU Chakib. Assessment of different methods of CO2 capture in post-combustion using ammonia as solvent[J]. Journal of Cleaner Production, 2015, 103: 463-468.
[150] 陈颖, 李慧, 李金莲, 等. 氨法烟气脱硫脱硝一体化工艺的研究进展[J]. 化工科技, 2010, 18(2): 65-69.
CHEN Ying, LI Hui, LI Jinlian, et al. Research progress on ammonia process for desulfurization and denitration from flue gas[J]. Science &Technology in Chemical Industry, 2010, 18(2): 65-69.
[151] 罗永刚, 李大骥, 杨亚平. 活性炭联合脱硫脱硝工艺[J]. 热能动力工程, 2001, 16(4): 444-446.
LUO Yonggang, LI Daji, YANG Yaping. Activated carbon-based combined desulfuration and denitration technology[J]. Journal of Engineering for Thermal Energy and Power, 2001, 16(4): 444-446.
[152] 邱广明, 宁占武, 兰学军, 等. 烟气脱硫脱硝技术的回顾与综合利用[J]. 内蒙古电力技术, 2000, 18(5): 8-9.
QIU Guangming, NING Zhanwu, LAN Xuejun, et al. The retrospect and the comprehensive utilization of the flue gas desulphurization and denitrification technology[J]. Inner Mongolia Electric Power, 2000, 18(5): 8-9.
[153] 杜黎明, 刘金荣. 燃煤锅炉同时脱硫脱硝技术工艺性分析[J]. 中国电力, 2007, 40(2): 71-74.
DU Liming, LIU Jinrong.Process characteristic analysis on simultaneous desulfurization and denitrification for coal-fired boilers[J]. China Electric Power, 2007, 40(2): 71-74.
[154] 马双忱, 姚娟娟, 马宵颖, 等. 活性炭吸附/微波解吸脱除烟气中SO2的实验研究[J]. 中国电机工程学报, 2012, 32(26): 50-56.
MA Shuangchen, YAO Juanjuan, MA Xiaoying, et al. Experimental study on removal of SO2 using adsorption of activated carbon/microwave desorption[J]. Proceedings of the CSEE, 2012, 32(26): 50-56.
[155] 杨丽敏, 刘海玉, 谢创举, 等. 微波放电对活性炭脱硝的影响[J]. 中国电机工程学报, 2018, 38(21): 6375-6382.
YANG Limin, LIU Haiyu, XIE Chuangju, et al. Effect of microwave discharge on activated carbon for denitration[J]. Proceedings of the CSEE, 2018, 38(21): 6375-6382.
[156] 宋欣钰, 宁国庆. 烟气脱硫脱硝活性炭的研究进展[J]. 山东化工, 2017, 46(7): 71-75.
SONG Xinyu, NING Guoqing.Review of the active carbon used for desulfurization and denitrification of flue gas [J].Shandong Chemical Industry, 2017, 46(7): 71-75.
[157] 李源. 改性非沥青基煤质活性焦低温脱硝性能研究[D].太原:太原理工大学, 2018.
[158] 付亚利. 非沥青基煤质活性炭/焦的特性及其低温脱除NOx的研究[D].太原:太原理工大学, 2016.
[159] 汤宗慧, 徐光. 电子束半干法烟气净化技术[J]. 华东电力, 2003, 31(8): 9-10.
TANG Zonghui, XU Guang. Semidry electron beam technique for flue gas purification[J]. East China Electric Power, 2003, 31(8): 9-10.
[160] 李亚冰, 徐光, 徐晓画, 等. 电子束深度氧化烟气净化技术[J]. 热力发电, 2005, 34(11): 37-40.
LI Yabing, XU Guang, XU Xiaohua, et al. Gas purification technology with deep oxidation by using electron beam[J]. Thermal Power Generation, 2005, 34(11): 37-40.
[161]  Ewa, SUN Yongxia, CHMIELEWSKI A G, et al. Modelling study of NOx removal in oil-fired waste off-gases under electron beam irradiation[J]. Radiation Physics and Chemistry, 2015, 113: 20-23.
Ewa, SUN Yongxia, CHMIELEWSKI A G, et al. Modelling study of NOx removal in oil-fired waste off-gases under electron beam irradiation[J]. Radiation Physics and Chemistry, 2015, 113: 20-23.
[162] 巩梦丹, 尹华强. 燃煤电厂锅炉烟气脱硫脱硝技术及展望[C]//2016燃煤电厂超低排放形势下SCR(SNCR)脱硝系统运行管理及氨逃逸与空预器堵塞技术交流研讨会论文集. 杭州:中国节能协会热电产业联盟,2016: 388-394.
[163] 李盼宋, 李建军, 贺尧祖, 等. 电子束氨法协同脱硫脱硝技术的研究进展[J]. 四川化工, 2016, 19(1): 7-9.
LI Pansong, LI Jianjun, HE Yaozu, et al. The research progress of combined removal of NOx/SO2 by electron beam method used NH3[J]. Sichuan Chemical Industry, 2016, 19(1): 7-9.
[164] 任先文, 赵君科, 王保健. 脉冲电晕等离子体烟气脱硫脱硝工业化应用技术研究现状与展望[C]//第四届环境与发展中国(国际)论坛论文集.北京:现代教育出版社,2008: 369-374.
[165] HONG Liu, CHEN Dezhen, YIN Lijie, et al. Hydrazine-enhanced NO conversion in a pulsed corona discharge plasma (PCDP) reactor: Behaviors and mechanism[J]. AIP Advances, 2016, 6(9): 095108.
[166] HONG Liu, CHEN Dezhen, YANG Min, et al. Interaction between NO and SO2 removal processes in a pulsed corona discharge plasma (PCDP) reactor and the mechanism[J]. Chemical Engineering Journal, 2018, 359: 1130-1138.
Future and challenge of coal based ammonia synthesis and clean utilization under the double carbon target

吴 烨 副教授
南京理工大学