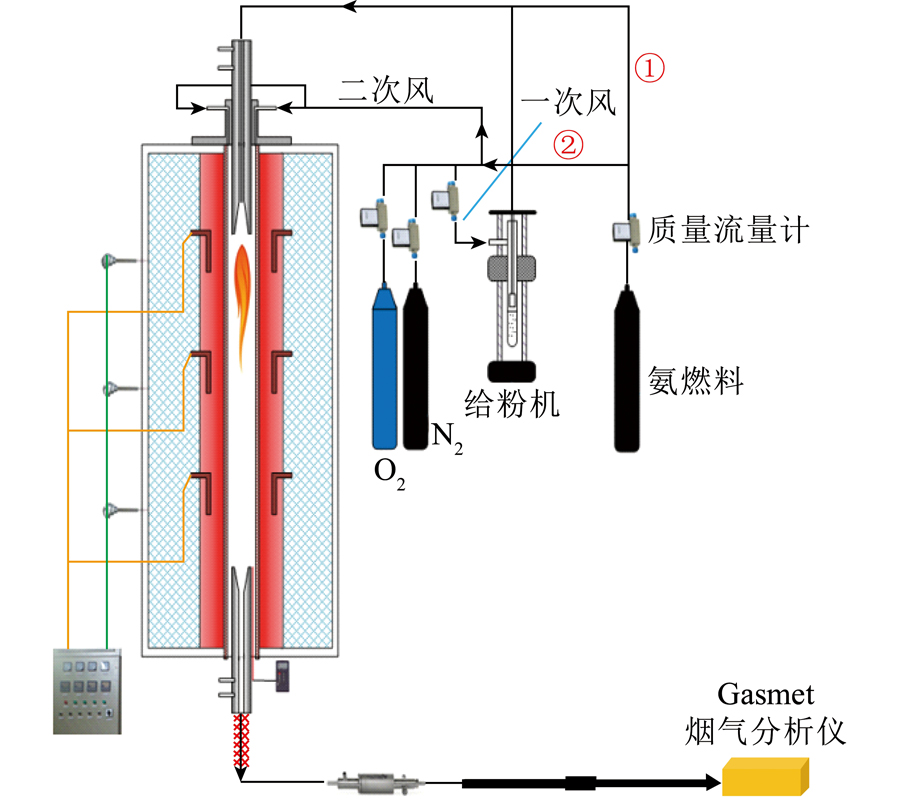
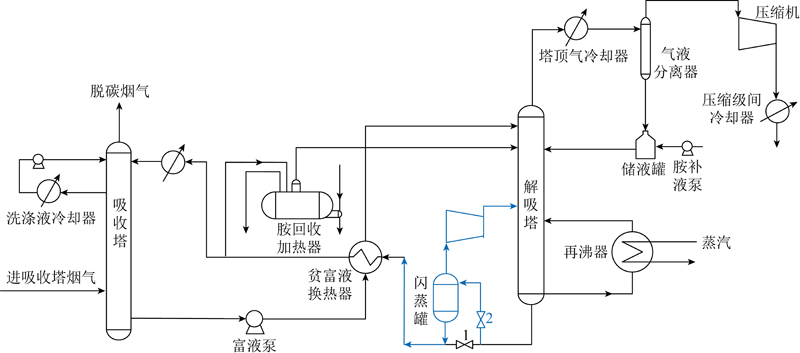
高硫无烟煤制备柱状活性炭对Cu2 的吸附规律及影响机制
0 引 言
高硫煤燃烧时硫分挥发产生大量硫氧化物,并产生碳氧化物等温室气体,严重污染环境。我国作为工业大国,金属、电镀、皮革等产业迅速崛起,产生大量含重金属的污水[1]。随着环保政策不断收紧,如何高效、快速处理重金属污水成为焦点[2-4]。煤基活性炭是由煤炭加工得到的人工炭材料制品,是性质优良的吸附剂,广泛应用于环保、航天、化工、医药等方面[5-6]。将煤炭加工制备活性炭是其高值化清洁利用的有效途径。
水处理是国内活性炭最大应用领域[1],活性炭主流应用指标包括吸附性能如碘值、亚甲蓝值,理化性质如漂浮率、装填密度、颗粒分布、强度以及水溶物指标[7],但无法体现活性炭对水中某特定类型污染物的吸附能力。活性炭孔结构分布、表面化学性质对活性炭净水能力影响及对污染物作用机制不清晰[5],造成活性炭制备阶段目标模糊,影响精准量化调控制备技术开发,应用效果不理想。
为提高活性炭水处理能力,需对活性炭改性,丰富其表面活性官能团。常用的改性手段有氧化改性[8-12]、氨化改性[13]、硫化改性[14-15]以及配位配体功能改性[15-16]。AGGARWAL等[17]以Cr3 为吸附质,使用硝酸、过硫酸铵、过氧化氢对活性炭进行氧化改性,提高了Cr3 的吸附量。MACIAS-GARCIA团队于900 ℃使用SO2硫化处理活性炭,使其对Cd2 去除率达70.3%[18]。CHENG等[19]使用氨气高温处理活性炭,显著提高了有机物的吸收率。然而通过改性、负载等手段进一步加工耗时耗力,成本高,且可能造成比表面积下降[7],亟需了解对某特定污染物的去除机理及影响因素,并以此设计满足去除该种污染物的活性炭制备路线。
现有研究大多围绕表面活性官能团对污染物的去除机制。对于重金属而言,主要机理有Π-Π堆积相互作用、形成络合物、离子交换等[20-22]。鲜见孔结构等物理性质对吸附性能的影响。笔者以晋城望云15号高硫无烟煤为原料,采用水蒸气活化法制备柱状活性炭,提出了该高硫煤清洁高值化利用的有效途径。对自制活性炭进行处理改变其孔径分布,比较2种活性炭对铜离子吸附性能的差异。从孔径分布出发,探索影响吸附水平的因素,剖析活性炭对水溶液中铜离子的吸附机理,为重金属水处理领域的活性炭定向制备提供思路。
1 试 验
1.1 试验样品
试验样品为晋城所用高硫无烟煤,其工业分析和元素分析见表1。
表1 高硫无烟煤工业分析和元素分析
Table 1 Proximate and ultimate analysis of high-sulfur anthracite

1.2 柱状活性炭制备方法
研磨高硫无烟煤至粒度<0.074 mm备用。采用沥青、煤焦油和聚乙烯醇做黏结剂,制备柱状高硫煤基活性炭工艺流程如图1所示。

图1 柱状活性炭制备方法
Fig.1 Preparation method of columnar activated carbon
采用马弗炉炭化,每份制样取高硫无烟煤100 g,加入15 g煤焦油、20 g沥青、27 g水,经搅拌混匀、挤条成型后,置于烘箱中100 ℃恒温干燥12 h;干燥后将其截断为长度10~15 mm的柱状干燥料条,移入炭化杯,将炭化杯置于马弗炉恒温区,保持N2气氛以12 ℃/min升温至550 ℃,保温30 min,冷却得到炭化料。采用管式炉活化,将炭化料置于钢管中部,管式炉升温至550 ℃时将钢管插入管式炉,继续升温,温度升至700 ℃启动蠕动泵向钢管注水,流量为0.3 L/min;温度升至920 ℃时,流量改为0.5 L/min,活化4 h,冷却得到活性炭成品,记为AC-1。
将AC-1磨至粒度<0.074 mm,置于200 mL烧杯中,置于磁力搅拌器上;量取100 mL磷酸倒入烧杯中,保持30 ℃恒温,转速300 r/min处理5 h。将烧杯中浊液过滤、洗涤直至洗液pH不变,于105 ℃烘箱烘干24 h得到成品,记为AC-2。
1.3 柱状活性炭表征方法
采用傅里叶变换红外光谱仪(美国Thermo Scientific Nicolet iS20)表征2种活性炭的表面官能团种类,扫描波数为4 000~400 cm-1,分辨率为0.06 cm-1。
采用X射线光电子能谱仪(美国Thermo Scientific K-Alpha)分析活性炭表面各元素相对含量,使用Al靶Kα为X射线源,束斑尺寸900 μm。全扫描透过能力50 eV,步长1.00 eV;窄扫描透过能力为20 eV,步长0. 050 eV。以C 1s(284.8 eV)为定标标准进行荷电校正,拟合后得到表面元素各官能团相对含量。
以场发射扫描电子显微镜(SEM)观察活性炭表面形貌,直观反映孔隙结构变化。采用全自动比表面及孔隙度分析仪(美国Quantachrome Autosorb IQ3)进行吸附等温线测量绘制。采用氮气作为吸附质,吸附温度77.3 K,试验前样品于150 ℃真空脱气6 h。样品比表面积采用BET方程拟合计算,样品孔体积由相对压力p/p0=0.99时的氮气吸附量计算得到。
1.4 Cu2 吸附性能检测
称取0.20 g铜试剂(二乙基氨基二硫代甲酸钠),用去离子水溶解后定容至100 mL,所得溶液可保存5 d备用。称取1.963 9 g CuSO4·5H2O,去离子水溶解后定容至500 mL,得1 000 mg/L铜离子溶液,稀释得50 mg/L标准铜离子溶液。使用移液枪取1.000 mL标准铜离子溶液,加入1 mL铜试剂溶液,使用乙醇溶剂定容至25 mL得到2 mg/L铜离子溶液。采用紫外-可见分光光度计进行全波长扫描,发现最大吸收波长位于436 nm,因此采用436 nm处吸光度。依次配制0.1、0.3、0.5、0.7、1.0、1.2、1.4、1.6、2.0 mg/L铜离子溶液,检测吸光度,铜离子标准吸光度曲线如图2所示。线性拟合后得到Cu2 标准吸光度曲线(式(1)),可由吸光度求得平衡时铜离子浓度。

图2 铜离子标准吸光度曲线
Fig.2 Standard absorbance curve of copper ion
y=3.491 4x-0.082 8。
(1)
量取40 mL质量浓度50 mg/L铜离子溶液置于100 mL烧杯中。称取活性炭粉末0.20 g置于溶液中,以300 r/min速率搅拌。待反应结束后,离心取上清液,使用紫外-可见分光光度计检测吸光度,由式(1)计算吸附平衡时铜离子质量浓度C1,计算吸附量qe(mg)与吸附率η(%):
qe=(C0-C1)V,
(2)

(3)
式中,C0为铜离子溶液初始质量浓度,mg/L;V为加入铜离子溶液的体积,均为40 mL。
1.5 吸附过程分析
设计吸附温度、吸附时间、Cu2 溶液pH值、吸附质投入量及Cu2 初始浓度5个不同单因素。通过对比2种活性炭表面化学性质、孔隙结构差异分析导致吸附性能不同的内在原因,并对吸附过程进行动力学、热力学模型拟合,研究吸附过程内在机理。采用Lagergren动力学模型拟合得到吸附速率的控制步骤,通过Langmuir等温模型拟合得到吸附内在情形,通过Freundlich吸附经验式拟合得到初始浓度与单位体积吸附量的函数关系[23-24]。
2 结果与讨论
2.1 活性炭物理性质
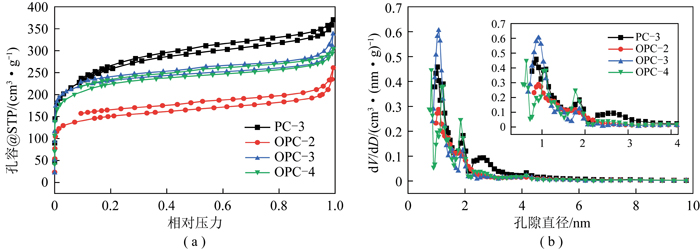
使用BJH方法处理吸附等温线,所得全孔分布如图3(a)所示。可知AC-1与AC-2孔隙主要分布在微孔(<2 nm)、介孔(2~50 nm),大孔(>50 nm)数量很少。使用DFT方法进行微介孔精确计算,由DFT方法计算得到的孔径分布如图3(b)所示。可知孔径较小时(<4 nm),AC-2的微孔结构比AC-1发达。但随孔径增大,AC-2单位体积孔容急速减少,AC-1下降较平缓,AC-2介孔更发达,这一点在图3(a)得到印证。为观察二者在微孔上的差异,使用HK方法处理数据,得到的微孔分布如图3(c)所示。可知AC-2在整个微孔范围内具有比AC-1更大的孔容和更丰富的孔隙结构。结合图3(b)中AC-2孔径在4 nm左右断崖式下降,推测磷酸造成介孔坍缩,使其转变为微孔,从而形成发达的微小结构。

图3 2种活性炭的孔径分布
Fig.3 Pore size distribution of two activated carbons
AC-1、AC-2的比表面积、总孔、微孔容、最几可孔径及中位孔径对比见表2。由表2可以看出,AC-2比表面积上升。这是由于磷酸处理使活性炭颗粒变小,在一定体积内表现出更大表面积,SEM扫描照片可以印证这一点。相较AC-1,AC-2微孔孔容和总孔容大幅提升,结合电镜扫描照片可以看出,这是由于酸刻蚀活性炭表面,使其产生更多孔洞。在微孔介孔范围内,AC-2最几可孔径为0.718 nm,小于AC-1的1.688 nm,说明AC-2大部分孔分布在<1 nm的极小范围内,而AC-1孔分布在较大较宽范围。而AC-1的全孔中位孔径小于AC-2,AC-2具有更丰富的较大孔分布,图3(b)中AC-2横坐标延伸更长可以证明这一点,说明磷酸具有造孔作用。
表2 2种活性炭孔隙
Table 2 Pores of two activated carbons

总体来看,AC-2相比AC-1具有更发达的微孔结构,AC-1相比AC-2有更发达的介孔结构。此外AC-2具有更多大孔,造成全孔中位数升高。
对比同等倍数下电镜放大照片,可以观察活性炭表面形貌,并与吸附等温线进行对比分析,如图4所示。由图4(b)可知,AC-2表面颗粒更小,颗粒与颗粒间孔隙更多,形成更多微孔,与HK方法获得的微孔分布结果相吻合。此外,由图AC-1-B、AC-2-B可知AC-2孔隙更深邃,表明经过磷酸处理使微孔得以延伸。同时AC-2表面具有沟壑,主要是由于酸刻蚀表面,使原本平整、光滑的地方出现凹陷。图3(b)中AC-2在较大孔径下延伸更远,这些孔可能来自于沟壑的形成。

图4 2种活性炭SEM对比
Fig.4 SEM comparison of two activated carbons
2.2 活性炭表面化学性质
AC-1与AC-2的红外光谱图如图5所示。3 436 cm-1处的谱带可归属为活性炭表面的缔合羟基,一般包括化学吸附水及形成氢键的酚羟基、羧基等。值得注意的是,磷酸处理后此处峰吸收强度相较处理前大幅降低,可知处理后活性炭表面羟基含量减少。2 921及2 853 cm-1处的谱带可归属为饱和—CH—,—CH2—和—CH3烷基中C—H的对称、反对称振动。2 516 cm-1处有微弱的特征明显的吸收峰,为S—H的伸缩振动,与原料为高硫煤有关。上述谱峰为2样品所共有。1 400~1 700 cm-1多组峰信号可归属为芳环骨架振动[25]。且1 427 cm-1处较弱的吸收峰与COO-的对称伸缩振动有关,AC-1较AC-2吸收峰明显,表明磷酸作用后活性炭表面羧基含量降低。AC-2在1 091 cm-1处有一强烈的吸收峰,可能是由于酸性磷酸酯中的P —O-键和多磷酸盐链P—O—P对称振动的组合[26]。且该峰附近波数对应含P化合物(如P![]() O双键伸缩振动)的吸收,该峰较宽,说明处理后活性炭表面有多种含P化合物,如1 000~990 cm-1处峰值可能是由于脂肪族P—O—C拉伸、芳香族P—O—C不对称拉伸,O—P
O双键伸缩振动)的吸收,该峰较宽,说明处理后活性炭表面有多种含P化合物,如1 000~990 cm-1处峰值可能是由于脂肪族P—O—C拉伸、芳香族P—O—C不对称拉伸,O—P![]() O中的P—O拉伸、P—OH弯曲,多磷酸盐中的P—O—P不对称拉伸及磷酸盐-碳络合物中存在的P—O对称拉伸[27-30]。而AC-1在1 033 cm-1附近有较弱吸收峰,归属于某些脂肪酸酯和内酯的C—O伸缩振动[25]。这在AC-2中体现不明显,是多种官能团吸收带所在波数重叠且被含P化合物覆盖所致。
O中的P—O拉伸、P—OH弯曲,多磷酸盐中的P—O—P不对称拉伸及磷酸盐-碳络合物中存在的P—O对称拉伸[27-30]。而AC-1在1 033 cm-1附近有较弱吸收峰,归属于某些脂肪酸酯和内酯的C—O伸缩振动[25]。这在AC-2中体现不明显,是多种官能团吸收带所在波数重叠且被含P化合物覆盖所致。

图5 2种活性炭的FTIR对比
Fig.5 FTIR comparison of two activated carbons
2种活性炭的全元素谱如图6所示。可知2种活性炭主要元素均为C、O、S、Si与Al。说明磷酸处理并未将磷元素大量引入活性炭,但FTIR显示其具有P元素吸收峰,可能由于AC-2中无法检测到磷元素,其相对于C、O、Si等太少,说明吸附性能的差异并非磷元素有关物质造成。

图6 2种活性炭的全电子能谱
Fig.6 Full electron spectra of two activated carbons
2.3 Cu2 吸附规律与影响机制
2.3.1 吸附时间
保持其他试验条件(初始pH,35 ℃,投入0.2 g,初始质量浓度50 mg/L)不变,分别于5、10、15、20、25、30、60、120、180、240 min检测铜离子浓度,计算去除率,得到去除率-时间图如图7所示。

图7 不同时间下去除率对比
Fig.7 Comparison of removal rates at different times
活性炭对金属离子的吸附包含物理吸附、化学吸附2方面[21]。其中物理吸附速率较快且可逆,化学吸附一般较慢且不可逆。吸附过程开始阶段,2种活性炭吸附效果相当,但AC-1整体呈上升趋势,AC-2明显波动。可能由于早期改性炭以物理吸附为主,由于搅拌作用在吸附脱附中呈现动态。吸附初期物理吸附占主导,化学吸附缓慢进行,单位时间去除率不稳定是由于物理吸附脱附,抵消部分化学吸附量。对于AC-1,随化学吸附不断进行,总吸附量呈上升趋势,并最终多于AC-2。根据孔隙分布可知,AC-1介孔结构比AC-2发达,因此AC-2最终去除率低可能由于其介孔吸附量低。由XPS分析可知,AC-2的羧基含量低于AC-1,表面化学吸附位点少,饱和化学吸附量低,在初期物理吸附的脱附甚至在某些时间段内占优,二者原因综合导致初期去除率波动且最终去除率低。2 h后去除率基本稳定,结合去除率与生产实际,选择2 h作为最佳吸附时间。
吸附动力学主要用于分析吸附速率与吸附时间的关系。吸附速率影响吸附达到平衡的时间,反映吸附过程快慢,是描述吸附行为的重要手段。在吸附动力学研究中,通常采用Lagergren准一级动力学方程和Lagergren准二级动力学方程模型描述质量浓度随时间的变化。准一级吸附动力学模型假定吸附受扩散步骤控制,准二级动力学模型假定吸附速率由化学吸附过程控制[1]。准一级、准二级动力学模型的线性形式为
ln(q′e-qt)=lnqe-k1t′,
(4)

(5)
式中,qt为t时刻的吸附量,mg/g;q′e为平衡时的吸附量,mg/g;k1为准一级速率常数,h-1;k2为准二级速率常,g/(mg·h);t′为吸附时间,min。
AC-1、AC-2的准一级、准二级动力学方程拟合如图8所示,详细参数见表3。

图8 2种活性炭的动力学拟合结果
Fig.8 Kinetic fitting results of two types of activated carbons
表3 动力学拟合相关参数
Table 3 Related parameters of kinetic fitting

注:K1为准一级动力学常数;K2为准二级动力学常数。
由表3可知,准二级动力学方程对AC-1和AC-2拟合效果更好。对于AC-1拟合所得qe为7.87 mg,与试验值7.82 mg接近。说明AC-1吸附Cu2 的过程由化学吸附步骤而非颗粒内扩散控制,AC-2同理。
2.3.2 吸附温度
保持其他试验条件(初始pH,吸附时间2 h,投入0.2 g,初始质量浓度50 mg/L)不变,改变吸附过程温度,温度与去除率的关系如图9所示。可知温度对反应影响较小。由于吸附一般是放热过程,脱附一般是吸热过程[21],在试验温度范围内,随温度小幅升高,温度引起的吸附、脱附作用互相抵消,故去除率相对稳定。

图9 温度对去除率的影响
Fig.9 Effect of temperature on removal rate
2.3.3 Cu2 溶液pH
保持其他试验条件(35 ℃,吸附时间2 h,投入0.2 g,初始质量浓度50 mg/L)不变,改变铜离子溶液pH,pH与去除率的关系如图10所示。

图10 pH对去除率的影响
Fig.10 Effect of pH on removal rate
由图10可知,随着pH升高,2种活性炭对铜离子的去除率均上升。pH主要影响化学吸附,而化学吸附机理一般以形成配合物、离子交换为主[21],一般是羧基、酚羟基的质子与铜离子交换并最终形成络合物(图11)。

图11 羧基、酚羟基对铜离子吸附机理
Fig.11 Adsorption mechanism of carboxyl and phenolic hydroxyl groups on copper ions
由图10可知,pH较小时,氢离子浓度高,在表面络合物形成过程中其与铜离子竞争吸附位点,这一趋势在很多炭质吸附剂中观察到[30-32]。此外,pH很低时AC-1去除率低于AC-2,pH>2时,AC-1去除率高于AC-2,AC-1去除率随pH变化较AC-2明显。这可能是由于:① 从化学吸附机理角度考虑,羧基作为影响吸附作用的主要官能团[27],在pH很小时质子强烈抑制羧基吸附时发挥的作用,随pH上升,羧基解离,与铜离子进行离子交换,去除率上升。通过表面化学分析可知AC-1表面羧基含量较高,单位pH下AC-1中恢复吸附能力的羧基多于AC-2,因此其去除率随pH增大升高更快。② 从孔隙分布考虑,由于吸附在水溶液中进行,若铜离子被官能团捕获需与活性炭表面接触。活性炭孔隙结构主要按如下方式排列:大孔直接通向颗粒外表面,中孔(即过渡孔)是大孔的分支,微孔又是中孔的分支[5]。而溶液中铜离子正是随溶液逐步进入孔隙而被捕获。但由于介质是水,表面张力很高,难以浸润微孔,使微孔表面官能团无法与铜离子接触,导致其在吸附过程中难以发挥作用。而只有活性炭孔径与吸附质几何尺寸相匹配时才能发生最佳吸附效果[5],铜离子半径仅127.8 pm,远小于大孔孔径。因此在本研究中仅介孔发挥作用。AC-2介孔体积很小,其表面化学吸附位点较少,因此吸附性能随pH增加提升不明显。pH很小时其吸附量主要来源于物理吸附,物理吸附来源于分子间作用力,受pH影响不大。综上原因导致2种活性炭吸附行为的差异。
2.3.4 吸附质投入量
保持其他试验条件(初始pH,35 ℃,吸附时间2 h,初始质量浓度50 mg/L)不变,改变活性炭投入量,投入量与去除率的关系如图12所示。可知铜离子浓度一定时,随投入活性炭质量增多,AC-1去除率提高,但接近最大值时基本停滞;AC-2去除率与活性炭投入量无明显关系。对于AC-1,随活性炭投入量增多,总吸附量提高,故去除率随投入量增多而提高。投入量增至一定程度时,去除率接近100%,此时溶液中铜离子含量极低,去除率不再提高。对于AC-2,由于其以微孔为主,介孔含量低,表面官能团难以发挥作用,即以可逆的物理吸附为主导;同时吸附过程一直处于搅拌状态,难以预测其吸脱附状态,因此总吸附量与投入量无明确关系。综合考虑经济效益与去除率,AC-1最佳投入量为0.30 g。

图12 投入量对去除率的影响
Fig.12 Effect of input on removal rate
2.3.5 Cu2 溶液浓度
保持其他试验条件(初始pH,35 ℃,吸附时间2 h,投入量0.2 g)不变,改变铜离子溶液浓度,初始浓度与去除率的关系如图13所示。

图13 初始浓度对去除率的影响
Fig.13 Effect of initial concentration on removal rate
由图13可知,单位质量活性炭吸附平衡时的吸附量随初始质量浓度的增大而提高。去除率与浓度无明确函数关系。随初始质量浓度增大,虽然单位质量活性炭吸附量提高,吸附的铜离子总量增多,但水溶液中铜离子含量升高,去除率反而下降。
通过吸附等温模型拟合可知在某一温度下单位质量吸附剂对吸附质的最大吸附量[1],常采用Langmuir和Freundlich等温吸附模型对吸附数据进行线性拟合。由于本文温度对吸附性能影响不大,考虑实际应用情况选用35 ℃下数据。2种等温模型[1]为

(6)

(7)
式中,Ce为吸附平衡时溶液中Cr(Ⅵ)质量浓度,mg/L;qmax为单分子层饱和吸附量,mg/g;KL为Langmuir吸附平衡常数,L/mg;KF为吸附剂吸附能力有关常数,mg/g;n为吸附剂与金属离子亲和力的有关常数。
AC-1、AC-2两种等温线模型拟合结果如图14所示,2种活性炭拟合结果相关参数见表4。

图14 吸附等温线拟合对比
Fig.14 Comparison of adsorption isotherm fitting
表4 吸附等温线相关参数
Table 4 Adsorption isotherm related parameters

由表4可知,对于AC-1,其Langmuir等温模型拟合相关系数为0.975 7,拟合程度良好,表明AC-1对铜离子的吸附符合Langmuir理论假设,属于单分子层吸附。AC-1的Freundlich拟合相关系数为0.983 0,说明该模型同样可较准确描述其吸附行为。对于AC-2,Langmuir模型拟合程度较差,饱和吸附量及KL表明该模型不适用。从表面化学及孔隙分布看,AC-2化学吸附位和中孔更少,微孔、大孔更多,活性位点分布不均匀,违背Langmuir理论基本假设。而Freundlich模型拟合相关系数为0.974 0,能更准确描述AC-2的吸附行为。
2.4 活性炭吸附性能评价
AC-1对Cu2 的吸附性能显著优于AC-2,影响因素有孔隙结构与表面官能团。对于孔隙结构,中孔主导吸附效果,原因在于水相中水溶液难以浸润微孔,Cu2 难以接触微孔表面官能团,无法被捕获;大孔孔径过大,与Cu2 半径不匹配,不符合最佳吸附效果的假设,在吸附中难以发挥作用[5]。由于AC-2介孔容非常微小,微孔容占总孔容的绝大部分,表面官能团基本分布在微孔,难以发挥作用,导致其化学吸附量低,以物理吸附为主。吸附初始阶段去除率明显波动及吸附量随pH变化不大可以印证这点。对于表面官能团,羧基含量主导吸附效果,原因在于羧基质子可与Cu2 发生离子交换,形成配合物。此外,物理吸附量一般较少,获得高性能活性炭产品需在化学吸附性能上调控,因此定向制备时要从孔隙结构和官能团优化2方面考虑。
3 结 论
1)AC-1具有更发达的中孔结构,AC-2具有更发达的微孔结构。
2)AC-1以化学吸附为主,AC-2以物理吸附为主,前者具有更优越的吸附性能。在水溶液吸附过程中,由于水表面张力很大,难以浸润微孔,微孔表面官能团难以发挥作用,而大孔与吸附质几何尺寸不匹配,中孔才是影响吸附的主要因素。AC-1具有发达的中孔结构,其表面官能团可发挥作用。而AC-2中孔体积微小,微孔体积较大,表面官能团很难与吸附质Cu2 接触,难以发生化学吸附。
3)活性炭的吸附性能由孔隙分布和表面官能团协同发挥作用。
4)准二级动力学模型更好贴合试验数据,证明主导铜离子吸附过程的因素是化学吸附而不是颗粒内扩散。Langmuir吸附等温模型不适用于AC-2的吸附行为,证明AC-2不是单分子层吸附且吸附质之间具有相互作用力,这与AC-2以物理吸附为主有关。
[1] 刘立华,邢丹,贾静娴,等.玉米秸秆对废水中Cr(Ⅵ)吸附的热力学和动力学研究[J].南开大学学报(自然科学版),2018,51(4):5-11.
LIU Lihua,XING Dan,JIA Jingxian,et al. Study on thermodynamics and kinetics of adsorption of Cr(Ⅵ)in wastewater by corn straw[J]. Journal of Nankai University(Natural Science Edition),2018,51(4):5-11.
[2] 姚元勇,何来斌,张萌,等.新型生物质果胶吸附材料的制备及水溶液中铜离子(Ⅱ)吸附性能研究[J].化学试剂,2022,44(3):393-400.
YAO Yuanyong,HE Laibing,ZHANG Meng,et al .Preparation of novel biomass pectin adsorbing material and its adsorption performance for copper(Ⅱ)ion in aqueous solution[J].Chemical Reagents,2022,44(3):393-400.
[3] 邓文博,冯拥军.水体中重金属污染物产生原因及其去除方法[J].黄冈师范学院学报,2020,40(6):25-32.
DENG Wenbo,FENG Yongjun.Research on causes and removal methods of heavy metal pollutants in water[J].Journal of Huanggang Normal University,2020,40(6):25-32.
[4] 罗进,彭陈亮,王观石,等.多孔氧化物块体材料的制备及其对重金属离子吸附研究进展[J].化学通报,2022,85(12):1425-1434.
LUO Jin,PENG Chenliang,WANG Guanshi,et al.Advances in preparation of porous oxide monoliths and their applications in adsorption of heavy metal ions[J].Chemistry Bulletin,2022,85(12):1425-1434.
[5] 解强,张香兰,梁鼎成,等.煤基活性炭定向制备:原理·方法·应用[J].煤炭科学技术,2021,49(1):100-127.
XIE Qiang,ZHANG Xianglan,LIANG Dingcheng,et al. Directional preparation of coal-based activated carbon:Principles,approaches and applications[J]. Coal Science and Technology,2021,49(1):100-127.
[6] 解炜.我国煤基活性炭的应用现状及发展趋势[J].煤炭科学技术,2017,45(10):16-23.
XIE Wei. Application status and development trend of coal-based activated carbon in China[J]. Coal Science and Technology,2017,45(10):16-23.
[7] 邱国兴,沈正华,金杰.活性炭的改性及其水处理研究进展[J].唐山师范学院学报,2022,44(3):24-28.
QIU Guoxing, SHEN Zhenghua, JIN Jie. Research progress on modified activated carbon and its water treatment[J].Journal of Tangshan Normal University,2022,44(3):24-28.
[8] XUE Yuye,LU Guanzhong,GUO Yun,et al.Effect of pretreatment method of activated carbon on the catalytic reduction of NO by carbon over CuO[J]. Applied Catalysis B: Environmental,2008,79:262-269.
[9] HAYDAR S,FERRO-GARC A M A,RIVERA-UTRILLA J,et al.Adsorption of pnitrophenol on an AC with different oxidations[J]. Carbon,2003,41:387-395.
A M A,RIVERA-UTRILLA J,et al.Adsorption of pnitrophenol on an AC with different oxidations[J]. Carbon,2003,41:387-395.
[10] ZHAO N, WEI N,LI J, Z,et al.Surface properties of chemically modified ACs for adsorption rate of Cr (VI)[J].Chemical Engineering Journal,2005,115:133-138.
[11] 范明霞, 李玉堂, 李柱,等.硝酸改性活性炭对镉离子的吸附和再生[J]. 应用化工, 2019, 48 (7): 1625-1628,1634.
FAN Mingxia, LI Yutang, LI Zhu,et al. Adsorption and regeneration of cadmium ions by nitric acid-modified activated carbon[J]. Applied Chemical Industry, 2019, 48 (7): 1625-1628,1634.
[12] 田龙,王林风,屈凌波,等.磷酸改性秸秆基活性炭的吸附性能研究[J].河南化工,2020,37(4):15-19.
TIAN long,WANG Linfeng,QV Lingbo,etal. Study on adsorption properties of phosphoric acid modified straw-based activated carbon[J]. Henan Chemical Industry,2020,37(4):15-19.
[13] 张文彬,左宋林,王宜望.氨气改性活性炭表面含氮官能团的形成与演变[J].林产化学与工业,2017,37(2):35-41.
ZHANG Wenbin,ZUO Songlin,WANG Yiwang.Formation and evolution of surface nitrogen functionalities on activated carbons by ammonia modification[J]. Chemistry and Industry of Forest Products,2017,37(2):35-41.
[14] DAN Mugisidi, ARIA Ranaldo, JOHNY W Soedarsono,et al. Modification of activated carbon using sodium acetate and its regeneration using sodium hydroxide for the adsorption of copper from aqueous solution[J].Carbon, 2007, 23(6):1081-1084.
[15] AMIT Bhatnagar, WILLIAM Hogland, MARCIA Marques,et al.An overview of the modification methods of activated carbon for its water treatment applications[J]. Chemical Engineering Journal,2013,219(1):499-511.
[16] MORENOCASTILLA C,FERROGARCIA M A,JOLY J P,et al.Activated carbon surface modifications by nitric acid, hydrogen peroxide, and ammonium peroxydisulfate treatments[J]. Langmuir,1995,11: 4386-4392.
[17] AGGARWAL D, GOYAL M,BANSAL R C.Adsorption of chromium by activated carbon from aqueous solution [J].Carbon, 1999,37:1989-1997.
[18] MACIAS-GARCIA A,GOMEZ-SERRANO V, ALEXANDRE-Franco M F, et al.Adsorption of cadmium by sulphur dioxide treated activated carbon[J].Journal of Hazardous Materials,2003,103(1/2):141-152.
[19] CHENG W, DASTGHEI S A, KARANFIL T.Adsorption of dissolved natural organic matter by modified activated carbons [J]. Water Research,2005,39:2281-2290.
[20] 杨颖,李磊,孙振亚,等.活性炭表面官能团的氧化改性及其吸附机理的研究[J].科学技术与工程,2012,12(24):6132-6138,6147.
YANG Ying, LI Lei, SUN Zhenya, et al. Study on the oxidative modification of functional groups on the surface of activated carbon and their adsorption mechanism [J]. Science and Technology and Engineering, 2012,12(24): 6132-6138,6147.
[21] 张淑琴,童仕唐.活性炭对重金属离子铅镉铜的吸附研究[J].环境科学与管理,2008(4):91-94.
ZHANG Shuqin, TONG Shitang. Study on the adsorption of heavy metal ions lead, cadmium, and copper on activated carbon [J]. Environmental Science and Management, 2008(4): 91-94.
[22] GAO Xinyuan,WU Long,XV Qing,et al.Edsorption kinetics and mechanisms of copper ions on activated carbons derived from pinewood sawdust by fast H3PO4 activation[J].Environmental Science and Pollution Research International,2018,25(8):7907-7915.
[23] 朱晓蕾,杨建平,李海龙,等.燃煤飞灰合成磁性沸石对脱硫废水中Hg2 吸附性能[J].洁净煤技术,2022,28(10):103-109.
ZHU Xiaolei, YANG Jianping, LI Hailong, et al. The adsorption performance of magnetic zeolite synthesized from coal-fired fly ash on Hg2 in desulfurization wastewater [J]. Clean Coal Technology, 2022,28(10): 103-109.
[24] 俞泽涛,曾光华,周雅彬,等.中药固废制备多孔碳及其CO2吸附性能[J].洁净煤技术,2022,28(10):203-211.
YU Zetao, ZENG Guanghua, ZHOU Yabin, et al. Preparation of porous carbon from solid waste of traditional Chinese medicine and its CO2 adsorption performance [J]. Clean Coal Technology, 2022,28 (10): 203-211.
[25] MYGLOUETS M, PODDUBNAYA O I, SEVASTYANOUA O. Preparation of carbon adsorbents from lignosulfonate by phosphoric acid activation for the adsorption of metal ions[J]. Carbon,2014,15(7)80771-80783.
[26] 翁诗甫,徐怡庄.傅里叶变换红外光谱分析[M].3版.北京:化学工业出版社,2016:495-496.
[27] XIN Yuangao, LONG Wu, QING Xu, et al. Adsorption kinetics and mechanisms of copper ions on activated carbons derived from pinewood sawdust by fast H3PO4 activation[J]. Environmental Science and Pollution Research,2018,25(8):7907-7915.
[28] SOCRATES G.Infrared characteristic group frequencies[M].2nd ed.New York:John Wiley &Sons,1994:432-433.
[29] BELLAMY L J.The infra-red spectra of complex molecules[M].New York:Wiley,1980:124-127.
[30] BOURBIGOT S, BRAS M L,RENÉ Delobel,et al.Carbonization mechanisms resulting from intumescence-part II. Association with an ethylene terpolymer and the ammonium polyphosphate-pentaerythritol fire retardant system[J]. Carbon, 1995, 33(3):283-294.
[31] PUZIY A M,PODDUBNAYA O I, ZAITSEV V N,et al. Model-ing of heavy metal ion binding by phosphoric acid activated carbon [J]. Applied Surface Science, 2004, 221(1): 421-429.
[32] PUZIY A M, PODDUBNAYA O I, GAWDZIK B,et al. Functionalization of carbon and silica gel by phosphoric acid[J]. Adsorption Science &Technology,2007,25(8):531-542.
Adsorption law and influencing mechanism of Cu2 by columnar activated carbon prepared from high-sulfur anthracite
ZHAO Jinke,GUO Ziyi,DUAN Chenlong,et al.Adsorption law and influencing mechanism of Cu2 by columnar activated carbon prepared from high-sulfur anthracite[J].Clean Coal Technology,2024,30(1):124-133.

移动阅读