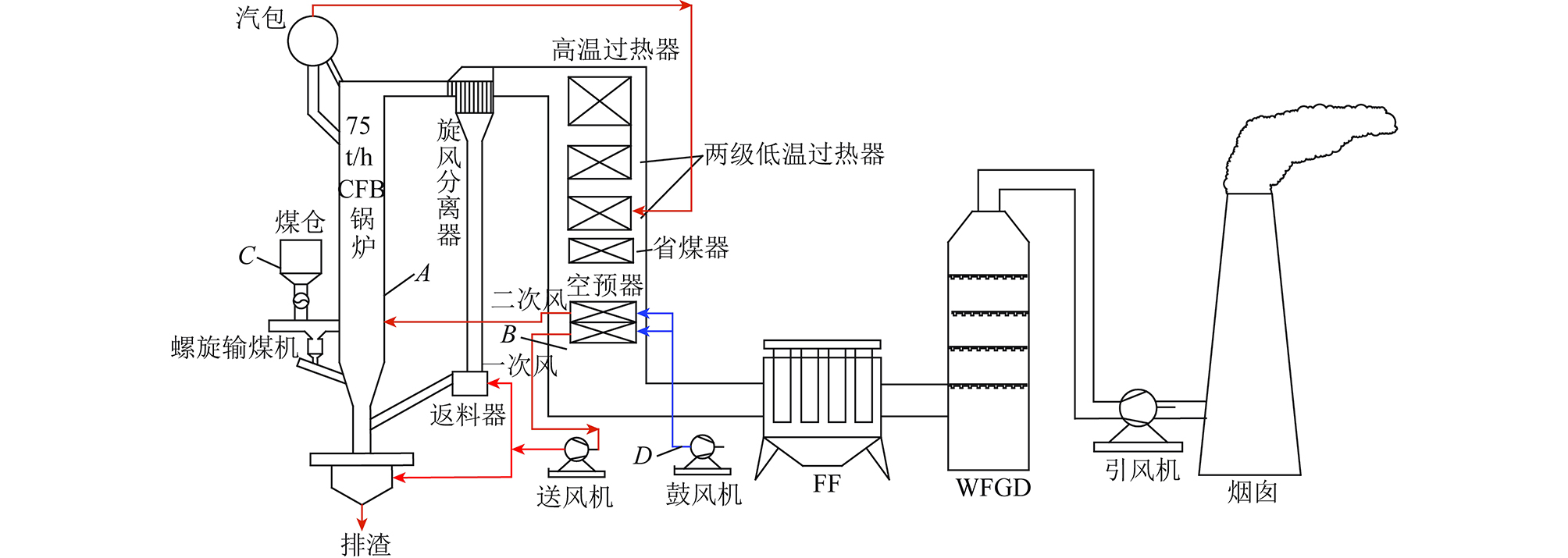
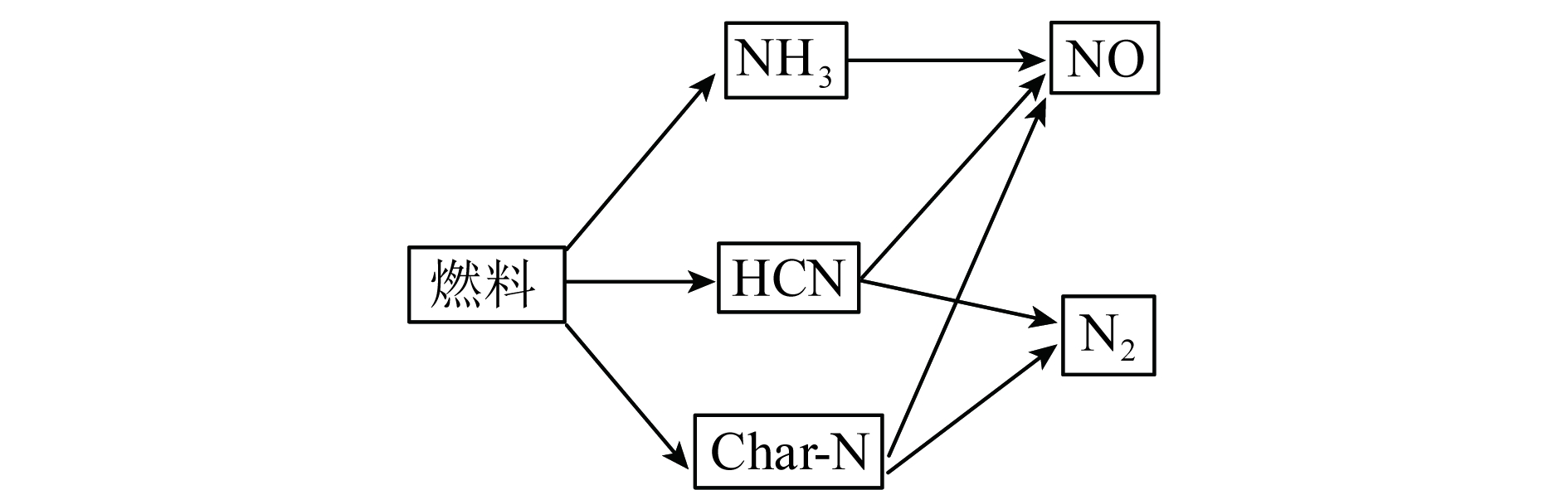
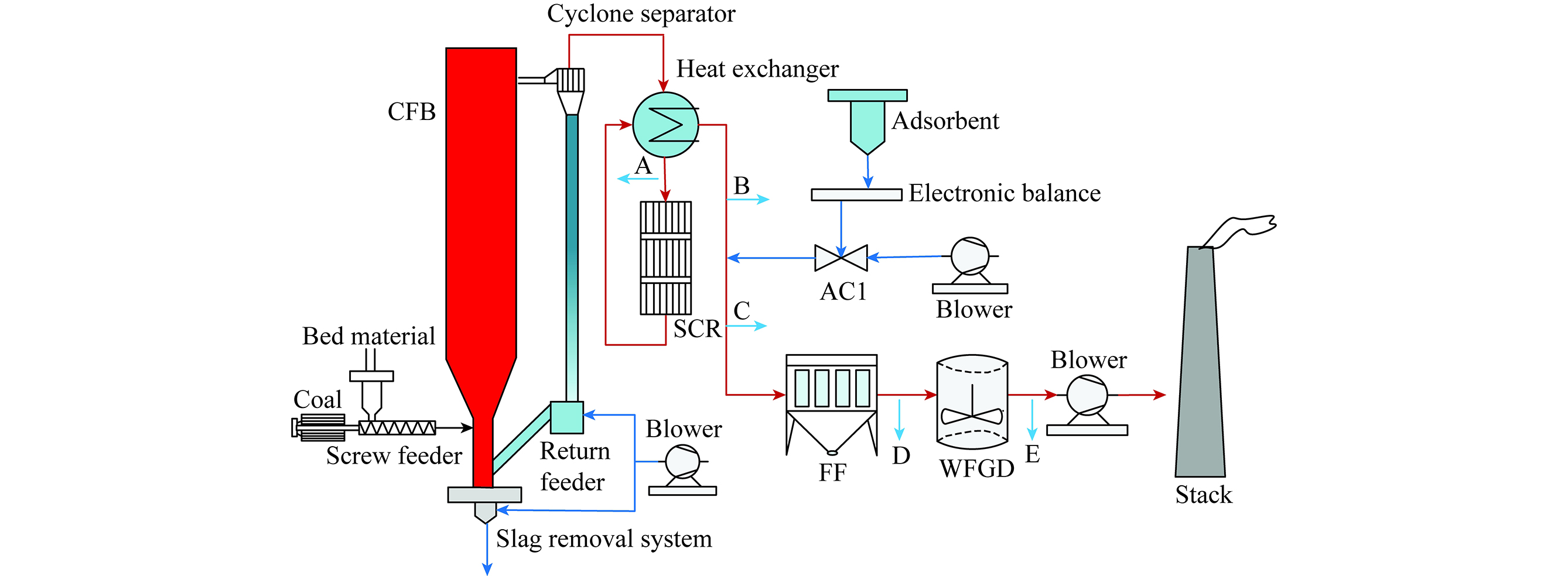
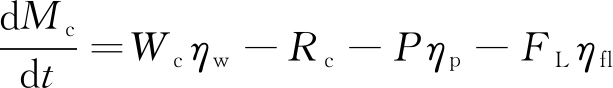铜基载氧体的焦炉煤气化学链燃烧特性
0 引 言
焦炉煤气(COG)是炼焦副产品,包括60% H2、28% CH4、9% CO和3% CO2及少量N2、C2烃类和硫化物,其中可燃气体体积分数高达96%[1-2]。COG广泛用于制合成气、发电、制化工原料、直接还原铁、燃料、制氢等领域[3-6]。COG作为燃料时,由于气体成分不稳定且存在少量杂质,导致燃烧不充分和热值较低等问题。化学链燃烧技术(CLC)通过避免燃料和空气直接接触降低碳捕集成本,无需额外能源产生高纯CO2[7],可直接用做下游化工合成原料。
CLC反应器一般由燃料反应器(FR)和空气反应器(AR)组成。载氧体(OC)在2个反应器之间通过氧的释放与吸收,实现氧化还原循环。在FR中,OC与H2、CH4、CO等燃料气体反应生成CO2和H2O,CO2可通过冷凝分离,OC被还原,在AR中,被还原的OC通过氧化性气体进行补氧使载氧体再生。目前,CLC工艺研究较多的载氧体(OCs)包括铁[8-9]、钴[10-11]、镍[12-13]、铜[13-14]、锰[15-16]等金属氧化物。载氧体除要求具有较高的燃烧性能以外,良好的循环稳定性也很关键。铜基载氧体具有较高的反应速率和氧转移能力[17],但在高温反应条件下热稳定性不强,ZEDAN等[18]发现在CeO2固溶体中掺杂6% CuO明显提高了CeO2催化CH4的活性,CeO2在585 ℃仅转化25% CH4,掺杂铜后T50=502 ℃,T90=556 ℃,显著降低CH4转化温度。SAHA等[19]以褐煤作为燃料,发现CuO载氧体1 223 K烧结而失活,但降低反应温度后在1 073 K时仍保持96%的活性,表明CuO热稳定性较差。LUIS等[20]通过热重分析法发现CuO作为载氧体时,纯CuO的氧化还原速率随循环次数增加而迅速下降。而在TiO2和SiO2载体上负载Cu后,制得的Cu基载氧体反应性较高;CuO/Al2O3载氧体在1 073 K下进行200 h化学链燃烧试验[21],在整个反应中表现出良好的反应性能。结果表明,负载于惰性载体可在一定程度解决Cu基载氧体热稳定性较差的问题。WANG等[22]研究了Zr掺杂对CuO载氧体释氧性能的影响机理。研究表明,掺杂Zr的CuO比纯CuO氧释放容量增大,具有更低的氧空位能垒,从而具有更高的反应活性。CAI等[23]通过微波辅助共沉淀法制备了Cu-Ce0.8Zr0.2O2,发现其中活性Cu均匀分散且与Cu-Ce0.8Zr0.2O2有强烈的相互作用,从而起到稳定铜物种的作用。综上所述铜基载氧体用于化学链燃烧性能优异,而铈锆复合氧化物具有高储存释放氧的能力与热稳定性[24],还具有稳定铜物种、促进晶格氧迁移率、提高活性的作用,因此CuO/CexZr1-xO2用于COG化学链燃烧潜力较好,有助于拓宽COG化学链燃烧铜基载氧体体系。
笔者通过添加Ce-Zr-O固溶体有效增强CuO载氧体在COG化学链燃烧的反应性能,运用XRD、SEM、Raman、XPS对铜基载氧体结构进行表征,探究COG化学链燃烧反应性能及循环稳定性。
1 试 验
1.1 载氧体制备
采用溶胶凝胶法制备了一系列x(%)CuO/Ce-Zr-O(x=0、30、50、70、90、100)载氧体。具体制备步骤如下:① 将一定量金属前驱盐(Cu(NO3)2·3H2O、Ce(NO3)3·6H2O、Zr(NO3)2·5H2O)按比例加入去离子水中在80 ℃水浴温度下搅拌;② 搅拌20 min后向混合盐溶液加入柠檬酸,快速搅拌直至成凝胶状,其中柠檬酸与金属离子物质的量比为1.1∶1.0;③ 将胶状物在120 ℃干燥12 h,取出烘干的样品研磨均匀;④ 研磨后前驱体放入马弗炉,以2 ℃/min升温至350 ℃煅烧2 h后,以相同升温速率升温至800 ℃焙烧 2 h;⑤ 载氧体制备成粒度0.5~0.8 mm颗粒。得到一系列Ce∶Zr物质的量比为2∶1时,(Ce∶Zr)∶Cu物质的量比为1∶9(90CuO/CZ)、3∶7(70CuO/CZ)、5∶5(50CuO/CZ)、7∶3(30CuO/CZ)及(Ce∶Cu)物质的量比为1∶9(90CuO/CeO2),(Zr∶Cu)物质的量比为1∶9(90CuO/ZrO2),CuO和Ce0.67Zr0.33O2(CZ)等载氧体。
1.2 载氧体物理化学表征
载氧体物相成分测定采用日本理学Mini Flex600型X射线粉末衍射仪(XRD),Cu靶(λ=0.154 06 nm),工作电压为40 kV,电流为15 mA,扫描范围为2θ=10°~90°,扫描速度为5 (°)/min,步长为0.02°,驻留时间为0.3 s。
拉曼光谱采用Thermo Fisher DXRxi型显微拉曼光谱仪测定。激光器波长为532 nm。激光功率为4.0 mW,频率为200~1 000 cm-1。
X射线光电子能谱(XPS)试验在Thermo Scientific K-Alpha仪器上进行,加速电压为15 kV,样品表面电荷被校正为C 1s=284.8 eV作为内部标准。
1.3 微观形貌分析
采用扫描电子显微镜(SEM)NOVA NANOSEM450 仪器观察载氧体反应前后的形态,使用能量色散X射线光谱法(EDS)获得元素的分布图像。加速电压为3 kV。
1.4 程序升温还原
氢气程序升温还原(H2-TPR)在ChemiMaster 8320 化学吸附仪(北京华璞恒创仪器有限公司)进行。将0.3 g载氧体放入U型反应器,Ar气氛吹扫,在10% H2/Ar气氛中由室温加热至900 ℃,升温速率10 ℃/min,气体流量30 mL/min。
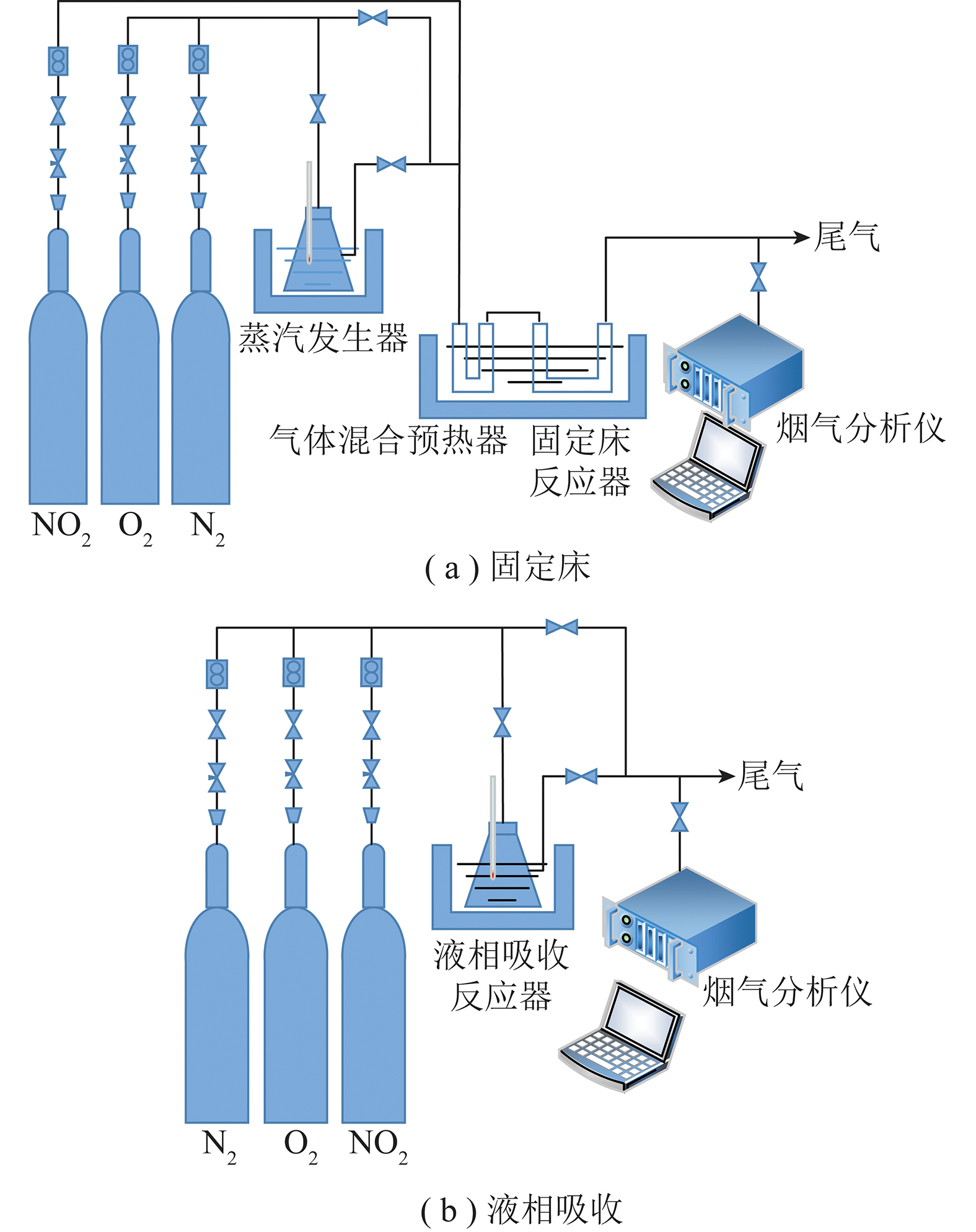
甲烷程序升温还原(CH4-TPR)是在实验室搭建固定床设备上进行,装置如图1所示。将1 g载氧体放入反应管,在N2气氛(99.9%,100 mL/min)下吹扫10 min后,通入5% CH4/N2(100 mL/min),温度由100 ℃升温至900 ℃,升温速率为10 ℃/min。

图1 载氧体活性评价装置
Fig.1 Schematic diagram of the performance evaluation device for the oxygen carrier
CO程序升温还原(CO-TPR)在实验室搭建固定床设备进行,装置如图1所示。将1 g载氧体放入反应管中,在N2气氛(99.9%,100 mL/min)下吹扫10 min后,通入10% CO/N2(100 mL/min),温度由100 ℃升温至900 ℃,升温速率为10 ℃/min。
焦炉煤气升温还原(COG-TPR)基于实际COG主要组分[1],配制得到实验室用COG(0.9% CO、0.3% CO2、2.8% CH4、6% H2、N2为平衡气)。载氧体和焦炉煤气程序升温还原试验在固定床反应系统进行,气体流量为200 mL/min,载氧体用量1 g,以10 ℃/min速率由室温升温至 900 ℃。
1.5 载氧体恒温反应活性评价
1.5.1 固定床试验
载氧体活性评价在固定床反应系统中进行。装置如图1所示,整体由配气系统、反应系统、检测系统3部分组成。反应系统由石英管和控温电弧炉组成,使用烟气分析仪实时检测尾气CH4、H2、O2、CO和CO2变化。
1.5.2 恒温氧化还原反应和循环试验
载氧体用量为2 g,恒温时间10 min,所有样品均在800 ℃进行COG恒温测试。步骤如下:① 程序设置由室温升温至800 ℃,升温速率10 ℃/min,升温过程通入N2为保护气,清除管路杂质;② 升温至800 ℃,COG以200 mL/min流速进入反应管,与载氧体反应;③ 吹入N2吹扫;④ 反应管中通入10% O2/N2,流速200 mL/min。
1.5.3 载氧体的性能评价指标
CH4转化率X(CH4):

(1)
式中,Cin(CH4)、Cout(CH4)分别为CH4进气和出气时体积分数,%;Fin为进管时气体流量,mL/min;Fout为出管时气体流量,mL/min。
CO2产率Y(CO2):

(2)
式中,Cout(CO2)为CO2出气时体积分数,%;R为理想状态下气体摩尔体积,22.4 L/moL;moxygen carrier为每次反应所需载氧体质量,g。
CO2捕集率η(CO2):

(3)
式中,Cout(CO)为CO出气时的体积分数,%。
2 结果与讨论
2.1 载氧体物理化学表征
为确定载氧体的晶体结构,通过XRD分别对x(%)CuO/Ce-Zr-O (x=0、30、50、70、90、100)、90 CuO/CeO2和90CuO/ZrO2载氧体样品进行物相分析,结果如图2所示。x(%)CuO/Ce-Zr-O (x=30、50、70、90)及90CuO/CeO2、90CuO/ZrO2载氧体均具有明显CuO特征衍射峰,分别存在单独的Ce0.67Zr0.33O2、CeO2和ZrO2特征峰。相比纯CeO2,样品中CZ特征衍射峰向高角度方向迁移(区域放大图)。这是由于Zr4 半径(0.084 nm)小于Ce4 半径(0.097 nm)[25],Zr4 可进入CeO2占据Ce4 的立方晶格,形成铈锆固溶体。ROOBERTA等[26]研究CeO2-ZrO2结构性质,发现Zr4 完全固溶到CeO2晶格中形成更多缺陷和晶格应力,提高耐温性,增加氧空位,提高体相氧迁移和扩散速率,进而提高燃料氧化能力。

图2 不同新鲜载氧体XRD图与Ce0.67Zr0.33O2主特征峰区域放大图
Fig.2 XRD pattern of different fresh oxygen carriers and enlarged image of Ce0.67Zr0.33O2 main characteristic peak region
随CuO含量增多,峰宽变窄,峰强增加,其他特征峰位置无明显变化,说明载氧体上CuO并未与Ce0.67Zr0.33O2形成Cu-Ce-Zr固溶体[27]。文献[28]报道煅烧温度500 ℃时,制备的Cu-Ce-Zr氧化物中Cu2 进入Ce-Zr晶格,铜氧化物以Cu-Ce-Zr固溶体和CuO两种形式存在,活性试验表明形成的Cu-Ce-Zr固溶体的载氧体H2还原峰温度较高,说明Cu-Ce-Zr固溶体释放氧能力较差,不宜作为载氧体。浸渍法制备的催化剂,Cu-Ce-Zr-4样品H2-TPR中主还原峰与CuO还原峰温度相近,发现CuO分散度低,形成大块CuO(1~3 μm),难以还原,不利于CO氧化[29]。
为进一步研究晶体结构,对不同样品进行拉曼光谱测试,如图3所示。268 cm-1处振动峰对应CuO结构,321 cm-1处对应ZrO2结构[30],453 cm-1处对应CeO2面心立方结构F2g振动峰,由于Zr4 固溶到CeO2中发生晶格畸变,使CZ振动的吸收峰发生蓝移,与XRD分析一致[31]。

图3 不同载氧体的拉曼图谱
Fig.3 Raman spectra of different oxygen carriers
CeO2、ZrO2、Ce0.67Zr0.33O2的加入对Cu结构无明显影响。添加CuO后,由于铜与铈锆之间的强相互作用[32],x(%)CuO/Ce-Zr-O (x=30、50、70、90)和90 CuO/CeO2中CeO2的F2g峰相较CZ样品发生蓝移,且在617 cm-1处出现新的振动峰,这归因于CeO2中部分Ce4 转变为Ce3 形成氧空位[28]。氧气吸附在氧空位上可降低表面释氧的吉布斯自由能,平衡化学价态,形成表面活性氧物种[33]。Zr4 加入CeO2晶格也可产生电荷平衡的氧缺陷[28],氧空位对提高载氧体活性至关重要。
XPS谱图如图4所示。由图4(a)可知,O 1s XPS图谱均由2个峰组成,其中529 eV的OⅠ归因于晶格氧(O2-),而532 eV的OⅡ则归因于表面吸附氧[28]。文献[34-35]报道表面吸附氧易与CH4反应生成CO2和H2O。OⅡ/OⅠ比值与氧缺陷浓度成正比。随CuO负载量增加,载氧体OⅡ/OⅠ比例增加,吸附氧在90CuO/CZ催化剂中最大,促进燃烧反应进行。由图4(b)可知,Cu 2p中结合能分别为930~936、950~958 eV处Cu 2p3/2和Cu 2p1/2的2个主峰,并在938~945 eV处出现卫星弱特征峰。高结合能Cu 2p3/2和卫星峰出现表明Cu在CuO中以Cu2 形式存在[36]。由图4(c)可知,Ce的XPS曲线显示4对3d5/2-3d3/2的自旋轨道分裂峰,用v和u表示,其中v(882.48 eV)、v″(889.5 eV)、v‴(898.4 eV)归属于Ce4 的3d5/2轨道,u(901.6 eV)、u″(908.1 eV)、u‴(916.7 eV)归属于Ce4 的3d3/2轨道,u′和v′是Ce 3d5/2和Ce 3d3/2中Ce3 离子特征峰[35]。表明样品中铈以Ce4 和Ce3 两种氧化态共存。Ce3 离子存在会形成氧缺陷,Ce3 /Ce4 比值越高表明可能具有最丰富的氧空位。Ce物种主要以CeO2形式存在,CeO2中Ce3 占比15%[33]。根据XPS结果计算载氧体表面元素组成见表1,Ce3 占比增至19%,由于Zr4 取代Ce4 ,Ce4 (0.097 nm)离子自发转变为较大Ce3 (0.110 nm)补偿晶格收缩[37]。90CuO/CZ中Ce3 /Ce4 比例最大,产生较多氧空位以增加吸附氧量。由图4(d)可知,Zr 3d图谱中Zr 3d5/2和Zr 3d3/2的结合能分别为181.9和184.6 eV,分别为ZrO2中的Zr4 与亲电子羟基基团结合的Zr4 物种[38],说明以Zr4 形式存在[39]。Zr 3d3/2和Zr 3d3/2峰的结合能不随CuO负载量的增加而变化。
表1 根据XPS结果计算载氧体表面元素组成
Table 1 Surface atomic ratio estimated by XPS for oxygen carriers

注:50th-90CuO/CZ为90CuO/CZ经过50次循环反应后得到的载氧体;50th-70CuO/CZ为70CuO/CZ经过50次循环反应后得到的载氧体。

图4 XPS谱图
Fig.4 XPS spectra
2.2 程序升温还原
焦炉煤气成分复杂,通过H2-TPR、CO-TPR、CH4-TPR研究不同还原组分在焦炉煤气转化中的竞争效应。H2-TPR用于探究载氧体的释氧特性,载氧体H2-TPR图谱如图5所示。CuO还原峰集中在200~400 ℃。相较CuO样品,加入Ce0.67Zr0.33O2、CeO2和ZrO2降低载氧体还原温度,表明铈锆与铜之间相互作用增强其低温释氧性能[40-41]。单独添加CeO2、ZrO2时,分别显示低温还原峰、高温还原峰。从还原峰面积分析,添加CZ后,载氧体还原性更强。随CuO负载量增加,所有载氧体整体还原峰向较高温度移动。x(%)CuO/CZ(x=30、50、70、90)在200~300 ℃出现α和β两个峰。Cu/Ce[42]和Cu/Zr/Ce[28]氧化物体系H2-TPR谱通常由2个重叠还原峰组成。低温还原峰归属于铈锆产生相互作用的高分散态铜物种,而高温还原峰则归属于体相铜物种及分散不均匀大颗粒[43]。这2个强还原峰是不同类型铜物种与CZ表面氧的共同还原[27]。

图5 不同载氧体H2-TPR图谱
Fig.5 H2-TPR profiles of different oxygen carriers
CO-TPR过程中CO和CO2随温度变化如图6所示。CuO、CZ转化初始温度300 ℃。相较纯CuO,添加Ce0.67Zr0.33O2、CeO2和ZrO2,CO初始还原温度分别为200、150、150 ℃,铈锆提高CuO对CO氧化能力[36,44]。单独CeO2、ZrO2做载体时CO无法完全转化。负载CZ的载氧体与CO反应温度远低于与H2反应温度,说明CuO/CZ更易被CO还原。

图6 不同载氧体CO-TPR曲线
Fig.6 CO-TPR profiles of different oxygen carriers
CH4与不同载氧体之间的程序升温反应(CH4-TPR)如图7所示。x(%)CuO/CZ(x=30、50、70、90、100)、90CuO/CeO2和90CuO/ZrO2载氧体在400 ℃开始转化,与CH4反应前期主要是主要产生CO2和H2O。CH4氧化产生的CO2和H2O的强度随温度升高急剧增加。温度增至800 ℃,表面吸附氧耗尽,不再产生CO2,CO、H2继续升高。CuO未负载时,CZ在600 ℃开始转化,表明铜的加入能在较低温度下实现低浓度CH4转化[45]。与CO-TPR和H2-TPR相比,CH4反应温度明显更高。这表明CuO/CZ与COG的反应条件应与CH4氧化反应条件一致,保证所有组分(CO、H2和CH4)相对较高的转化率。


图7 不同载氧体CH4-TPR曲线
Fig.7 CH4-TPR profiles of different oxygen carriers
载氧体与焦炉煤气程序升温还原(COG-TPR)曲线如图8所示。整个还原过程可分为2个阶段,200~700 ℃产物可归因于还原性气体和样品中活性较高的氧物种发生反应。200 ℃时H2和CO浓度降低、CO2浓度增加,这是由于CuO在200 ℃附近优先被H2和CO还原生成H2O和CO2。而H2、CO浓度降低和CO2浓度升高的反应窗口区间随x(%)CuO/CZ(x=30、50、70、90)中CuO降低而收窄。CuO载氧体反应窗口区间比x(%)CuO/CZ载氧体明显宽化,温度升高,CuO氧化CO能力减弱,CO2浓度降低。


图8 不同载氧体的焦炉煤气程序升温还原曲线
Fig.8 COG-TPR profiles of different oxygen carriers
第2阶段在700~900 ℃,CH4与样品可能发生部分氧化反应和裂解反应。700 ℃附近时,x(%)CuO/CZ(x=30、50、70、90)、90CuO/CeO2、90CuO/ZrO2载氧体CH4浓度开始降低,H2和CO浓度开始升高,CH4开始发生部分氧化反应,生成CO和H2使各组分浓度变化。CuO和CZ各组分含量未变化。CuO载氧体在500~600 ℃内CH4浓度明显降低,90CuO/CZ样品在升温过程中趋势相同。
800 ℃时,对比CO-TPR、H2-TPR,2种还原性气体完全转化。在CH4-TPR和COG-TPR中生成大量H2,说明CH4发生部分氧化反应。800 ℃时,COG转化到最大值。由COG-TPR可知,H2在150 ℃左右开始转化,相比H2-TPR,还原温度降低。CO开始转化温度和CO-TPR基本一致,对CO转化没有太大影响。2种还原性气体被载氧体氧化后产生大量CO2,且CO2产量随CuO增多面积增大,与上述试验结果一致。
2.3 载氧体恒温反应活性评价
通过载氧体和COG的恒温反应可判断载氧体的反应活性,不同载氧体与COG恒温反应在800 ℃下进行,气体组分浓度变化如图9所示。

图9 3次氧化还原反应循环主要产物与反应物的典型曲线
Fig.9 Typical curves of the main products and reactant during 3 cycles of redox reaction
添加CeO2、ZrO2后,CH4转化率分别为82%、86%,但添加Ce0.67Zr0.33O2后CH4转化率达100%。x(%)CuO/CZ(x=30、50、70、90)随CuO含量增多,CH4消耗量逐渐增加,CO2产率随CuO含量增多随之增加,在3次循环中保持稳定。CuO负载量较低时,产生的活性位点较少,增加负载量可显著提高活性位点数量,进而提升燃烧性能。随循环次数增加,纯CuO活性减弱。结合CuO样品循环前后SEM图,循环后CuO样品烧结严重,影响反应活性。CZ转化CH4能力较弱,5 min后其他组分恢复初始浓度,失去活性。
在800 ℃下进行50次还原氧化循环,考察载氧体对COG化学链燃烧的稳定性。CH4转化率和CO2产率、捕集率如图10所示。x(%)CuO/CZ(x=50、70)活性明显高于CuO,CH4转化率由第1次84.7%降至第3次22%,70CuO/CZ、90CuO/CZ的CH4转化率由第1次至第50次循环分别由94.6%、99.8%降至77%、93.6%。从CO2捕集率角度对比,70CuO/CZ、90CuO/CZ由第1次92.4%、100%降至第50次76%、97%。CuO样品则由第1次86%降至第3次34%。随着CuO含量增加,90CuO/CZ整体性能好于70CuO/CZ。CuO和70CuO/CZ活性下降明显,90CuO/CZ循环稳定性高。

图10 载氧体和焦炉煤气反应循环试验
Fig.10 Oxygen carrier and coke oven gas reaction cycle experiment
2.4 微观形貌分析
采用SEM及EDS考察90CuO/CZ样品循环前后的整体结构和元素分布情况。90CuO/CZ样品循环前后EDS图如图11所示。90CuO/CZ样品循环前后的EDS图中,Cu、Ce、Zr和O元素分布区域重叠,表明表面Cu元素均匀分布。90CuO/CZ样品的XRD物相组成为Ce0.67Zr0.33O2和CuO两种物相,不存在Ce、Zr和Cu三种元素固溶,说明Ce0.67Zr0.33O2和CuO分布位置一致,且循环前后无明显变化。

图11 SEM-EDS
Fig.11 SEM-EDS
70CuO/CZ、90CuO/CZ和CuO样品循环前后的显微结构如图12所示。由图12(a)可知,CuO循环3次后颗粒尺寸显著增大,说明CuO样品存在严重烧结问题。由图12(a)、12(c)、12(e)可知,随Ce0.67Zr0.33O2含量增加,颗粒尺寸逐渐减小,其中D50由CuO的2.25 μm分别降至90CuO/CZ的399.66 nm和70CuO/CZ的223.88 nm,说明第二相颗粒Ce0.67Zr0.33O2的添加对CuO颗粒长大起抑制作用。通过对比图12(c)、12(d)及12(e)、12(f)发现,70CuO/CZ和90CuO/CZ样品循环50次后CuO颗粒尺寸接近,但70CuO/CZ和90CuO/CZ样品循环50次后活性评价存在差异,说明烧结情况对70CuO/CZ和90CuO/CZ样品活性评价影响不大。

图12 载氧体的SEM图谱
Fig.12 SEM images of oxygen carriers
2.5 载氧体循环前后的物性结构变化
50次循环后载氧体的XRD和拉曼图谱如图13所示,可知长时间COG/O2还原氧化循环未明显影响载氧体物相结构,无其他晶相特征峰出现,且载氧体的拉曼主峰基本恢复到之前状态。进一步证明载氧体具有良好循环稳定性。

图13 50次循环后的载氧体XRD和拉曼图谱
Fig.13 XRD and Raman pattern of oxygen carrier after 50 cycles
3 结 论
1)通过溶胶凝胶法制备一系列x(%)CuO/Ce-Zr-O(x=30、50、70、90)、CZ和CuO载氧体,用于焦炉煤气化学链燃烧。载氧体物相以CuO和Ce0.67Zr0.33O2共存。相对纯CeO2,Ce0.67Zr0.33O2在617 cm-1处出现了明显拉曼特征峰,说明Ce0.67Zr0.33O2固溶体的形成产生了氧空位。
2)H2-TPR、CO-TPR、CH4-TPR和COG-TPR结果表明,CuO与Ce-Zr-O之间相互作用促进铜物种低温的释氧能力。
3)CuO载氧体在3次循环后CH4转化率由84.7%降至22.0%,CO2捕集率由86%降至34%。而90CuO/CZ载氧体50次redox循环后CH4转化率和CO2捕集率分别保持在95%和77%以上,CO2捕集量为1.61 mmol/g。
[1] 任冰朗. 高温转炉煤气与焦炉煤气混合重整研究[D]. 北京:北京科技大学,2022.
[2] 颜丙才,薛垂峰,巴合义,等.浅论焦炉煤气的综合利用途径[J].山东化工,2020,49(9):87-88,90.
YAN Bingcai,XUE Chuifeng,BA Heyi,et al.Reviews on the comprehensive utilization of coke oven gas[J].Shandong Chemical Industry,2020,49(9):87-88,90.
[3] 佟帅,艾立群,洪陆阔,等.中国氢冶金的发展及关键技术研究进展[J/OL].钢铁研究学报:1-14[2024-01-11].https://doi.org/10.13228/j.boyuan.issn1001-0963.20230092.
TONG Shuai,AI Liqun,HONG Lukuo,et al.The development of hydrogen metallurgy in China and the research progress of key technologies[J/OL]. Journal of Iron and Steel Research:1-14[2024-01-11].https://doi.org/10.13228/j.boyuan.issn1001-0963.20230092.
[4] 刘华锋. 焦炉煤气高效多联产利用技术研究[J]. 当代化工研究,2022(3):147-149.
LIU Huafeng. Study onefficient multi-production utilization technology of coke oven gas[J]. Mordern Chemical Reearch, 2022(3):147-149.
[5] 肖学文,王刚,李牧明,等.基于富氢/含碳煤气用于冶炼还原剂的减碳策略分析[J].中国冶金,2023,33(5):121-127.
XIAO Xuewen,WANG Gang,LI Muming,et al.Analysis of carbon reduction strategy based on hydrogen-rich/carbon-containing gas used for smelting reducing[J]. China Metal-lurgy,2023,33(5):121-127.
[6] 李志强,王华,李孔斋.焦炉煤气制氢技术研究进展[J].洁净煤技术,2023,29(4):31-48.
LI Zhiqiang,WANG Hua,LI Kongzhai.Research progress on hydrogen technology from coke oven gas[J].Clean Coal Technology,2023,29(4):31-48.
[7] 武永健,罗春欢,魏琳,等. 基于化学链燃烧的转炉放散煤气利用研究[J]. 化工学报, 2019, 70(5):1923-1931.
WU Yongjian, LUO Chunhuan, WEI lin, et al. Utilization of converter off-gas based on chemical-looping combustion[J]. CIESC Journal, 2019, 70(5):1923-1931.
[8] ZHANG S, WANG X, MAO Z, et al. Effect of calcinatio-ncondition on the performance of iron ore in chemical-looping combustion[J]. Fuel Processing Technology, 2020, 203(12):106395.
[9] BARROS D N R A, PIMENTA D M H, MELO D M A, et al. Structure and reactivity of Brazilian iron ores as low-cost oxygen carriers forchemical looping combustion[J]. Industrial &Engineering Chemistry Research, 2022, 61(6):2469-2482.
[10] ALALWAN H A, CWIERTNY D M, GRASSIAN V H. Co3O4 nanoparticles as oxygen carriers for chemical looping combustion: A materials characterization approach to understanding oxygen carrier performance[J]. Chemical Engineering Journal, 2017,319(13):279-287.
[11] GÜLEÇ F, MEREDITH W, SUN C G, et al. A novel approach to CO2 capture in fluid catalytic cracking:Chemical looping combustion[J]. Fuel, 2019, 244(10):140-150.
[12] NANDY A, LOHA C, GU S, et al. Present status and overview of Chemical Looping Combustion technology[J]. Renewable and Sustainable Energy Reviews, 2016,59(6):597-619.
[13] TILLAND A, PRIETO J, PETITJEAN D, et al. Study and analyses of a CLC oxygen carrier degradation mechanism in a fixed bed reactor[J]. Chemical Engineering Journal, 2016, 302(20):619-632.
[14] PACHLER R F, PENTHOR S, MAYER K, et al. Investigation of the fate of nitrogen in chemical looping combustion of gaseous fuels using two different oxygen carriers[J]. Energy, 2020, 195(6):116926.
[15] SUNDQVIST S, KHALILIAN N, LEION H, et al. Manganese ores as oxygen carriers for chemical-looping combustion (CLC) and chemical-looping with oxygen uncoupling (CLOU)[J]. Journal of Environmental Chemical Engineering, 2017, 5(3):2552-2563.
[16] WU Y, LUO C, WU W, et al. Denitration of the gas-fired boiler flue gas based on chemical-looping combustion[J]. Chemical Engneeing Journal, 2019, 361(7):41-49.
[17] 文圆圆,李振山,蔡宁生. 铜基载氧体循环吸氧/释氧稳定性实验研究[J]. 工程热物理学报,2012,33(10):1798-1802.
WEN Yuanyuan, LI Zhenshan, CAI Ningshen. Experiment research on cyclic stability of oxygen capacity for copper-based oxygencarrier[J]. Journal of Engineering Thermophysics, 2012, 33(10):1798-1802.
[18] ZEDAN A, ALJABER A. Combustion synthesis of non-precious CuO-CeO2 nanocrystalline catalysts with enhanced catalytic activity for methane oxidation[J]. Materials, 2019, 12(6):878.
[19] SAHA C, BHATTACHARYA S. Comparison of CuO and NiO as oxygen carrier in chemical looping combustion of a Victorian brown coal[J]. International Journal of Hydrogen Energy, 2011, 36(18):12048-12057.
[20] LUIS F de Diegoa, FRANCISCO García-Labianoa , JUAN Adá-neza,et al. Development of Cu-based oxygen carriers for chemical-looping combustion[J]. Fuel, 2004, 83(13):1749-1757.
[21] LUIS F de Diego,FRANCISCO Garcl a-Labiano. Operation of a 10 kWth chemical-looping combustor during 200 h with a CuO-Al2O3 oxygen carrier[J]. Fuel, 2007, 86(7):1036-1045.
[22] WANG M, LIU J, HU J, et al. O2-CO2 mixed gas production using a Zr-doped Cu-based oxygen carrier[J]. Industrial &Engineering Chemistry Research, 2015, 54(40):9805-9812.
[23] CAI W J, DONG J L, CHEN Q, et al. One-pot microwave-assisted synthesis of Cu-Ce0.8Zr0.2O2 with flower-like morphology: Enhanced stability for ethanol dry reforming[J]. Advanced Powder Technology, 2020, 31(9):3874-3881.
[24] 熊靖. 高性能多级孔铈锆复合氧化物担载纳米活性位炭烟燃烧催化剂研究[D]. 北京:中国石油大学(北京),2021.
[25] TENG M, LUO L, YANG X. Synthesis of mesoporous Ce1-xZrxO2(x=0.2-0.5) and catalytic properties of CuO based catalysts[J]. Microporous and Mesoporous Materials, 2009, 119(1/3):158-164.
[26] ROOBERTA Di Monte,JAN Kašpar. Heterogeneous environmental catalysis-a gentle art: CeO2-ZrO2 mixed oxides as a case history[J]. Catalysis Today, 2005, 100(1/2):27-35.
[27] 邓莲. 掺杂Cu的Ce-Zr-O2催化剂在富氢气中CO选择性氧化的研究[D]. 昆明:昆明理工大学,2014.
[28] WANG Y J, ZHENG Y, WANG Y, et al. Syngas production mod-ified by oxygen vacancies over CeO2-ZrO2-CuO oxygen carrier via chemical looping reforming of methane[J]. Applied Surface Science, 2019, 481(13):151-160.
[29] DONG X F, ZOU H B, LIN W M. Effect of preparation con-ditions of CuO-CeO2-ZrO2 catalyst on CO removal from hydrogen-rich gas[J]. International Journal of Hydrogen Energy, 2006, 31(15):2337-2344.
[30] MARCOS Davi L Goncalves, PIERRE B N Assis,ANTONIO N da silva,et al. Laser-power dependence effects on the structural stability of nanocomposite catalysts studied by Raman spectroscopy: On the structure-activity. correlations in glycerol acetylation[J].
Spectrochimica Acta Part A:Molecular and Biomolecular Spectroscopy,2022,280:121526.
[31] 费兆阳,李磊,成超,等. 铈锆复合氧化物催化HCl氧化中相互作用机制[J]. 化工学报,2018,69(12):5081-5089.
FEI Zhaoyang, LI Lei, CHENG Chao, et al. Interaction between CeO2 and ZrO2 in HCl catalytic oxidation[J]. CIESC Journal, 2018, 69(12): 5081-5089.
[32] 曹原. 铈基催化剂在NO、CO催化消除中的基础研究[D]. 南京:南京大学,2017.
[33] 郑燕娥. 三维有序大孔铈基储氧材料的制备及其化学链重整与催化CO氧化性能研究[D]. 昆明:昆明理工大学,2016.
[34] CHENG X, LI K, ZHU X, et al. Enhanced performance of ch-emical looping combustion of methane by combining oxygen carriers via optimizing the stacking sequences[J]. Applied Energy, 2018, 230(22):696-711.
[35] XU Zonghao, CHEN Yu, ZHAO Depeng, et al. Synthesis of high-performance Pd/Ce0.4Zr0.5La0.05Y0.05O1.95 catalysts for low-temperature methane combustion with the ultrasound-assisted field[J]. Fuel, 2024, 357:129746.
[36] 王威威. 铜铈锆催化剂在二氧化碳加氢合成甲醇反应中的催化性能与反应机理的研究[D].大连:大连理工大学,2020.
[37] LIU L J, YAO Z J, LIU B, et al. Correlation of structural characteristics with catalytic performance of CuO/CexZr1-xO2 catalysts for NO reduction by CO[J]. Journal of Catalysis, 2010, 275(1):45-60.
[38] INDOVINA V, OCCHIUZZI M, PIETROGIACOMI D, et al. The surface composition of CuOx/ZrO2 catalysts as determined by FTIR, XPS, ESR spectroscopies and volumetric CO adsorption[J].Journal of Physical Chemistry B, 1999, 103(45):9967-9977.
[39] LI Xuehua ,DOU Xiaomin, LI Junqing, et al.Antimony(V) removal from water by iron-zirconium bimetal oxide: Performance and mechanism[J].Journal of Environmental Sciences, 2012, 24(7):1197-1203.
[40] CAO J L, WANG Y, ZHANG T Y, et al. Preparation, characteriza-tion and catalytic behavior of nanostructured mesoporous CuO/Ce0.8Zr0.2O2 catalysts for low-temperature CO oxidation[J]. Applied Catalysis B:Environmental, 2008, 78(1/2): 120-128.
[41] ZHANG Shan,JIANG Binbo,TONG Mingliang,et al.Efficient Cu/CeO2 for ketonization of carboxylic acids with synergistic interactions[J].Industrial Engineering Chenistry Research, 2023, 62(48):20667-20676.
[42]  GUILA G, GRACIA F, ARAYA P. CuO and CeO2 catalysts supported on Al2O3, ZrO2, and SiO2 in the oxidation of CO at low temperature[J]. Applied Catalysis A: General, 2008, 343(1/2):16-24.
GUILA G, GRACIA F, ARAYA P. CuO and CeO2 catalysts supported on Al2O3, ZrO2, and SiO2 in the oxidation of CO at low temperature[J]. Applied Catalysis A: General, 2008, 343(1/2):16-24.
[43] DENG Q F, REN T Z, AGULA B, et al. Mesoporous CexZr1-xO2 solid solutions supported CuO nanocatalysts for toluene total oxidation[J]. Journal of Industrial and Engineering Chemistry, 2014, 20(5):3303-3312.
[44] CHEN Y, LIAW B, CHEN H. Selective oxidation of CO in exc-ess hydrogen over CuO/CexZr1-xO2 catalysts[J]. International Jo
urnal of Hydrogen Energy, 2006, 31(3):427-435.
[45] GENG H J, YANG Z Q, ZHANG L ,et al. Effects of O2/CH4 ratio on methane catalytic combustion over Cu/γ-Al2O3 particles[J].International Journal of Hydrogen Energy, 2016,41(40):18282-18290.
Combustion characteristics of coke oven gas chemical looping of copper-based oxygen carrier

移动阅读