煤制合成气中温变压吸附H2/CO2分离研究与示范
0 引 言
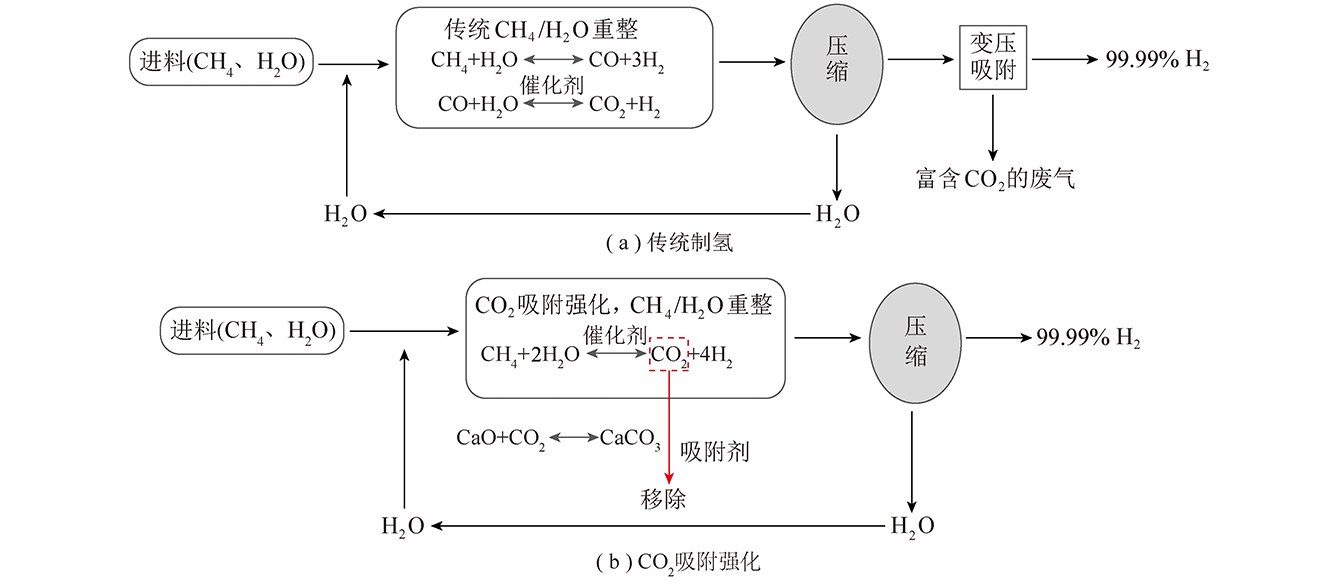
氢能是双碳背景下一种重要的能源载体,目前自然界中几乎没有单质H2,化石气体燃料转化和煤气化是目前最具成本效益和实用性的制氢方法[1]。我国目前H2最主要来源为煤制氢,即煤气化后通过净化工段获得目标H2。为避免后续催化剂中毒,满足燃料电池级别H2使用要求,需深度脱除合成气中CO2、CO、H2S等杂质[2]。以煤为原料的能源化工、发电、多联产技术行业中,水气变换后H2/CO2分离纯化及提取的作用不可替代。目前已有多种H2/CO2分离传统工艺路线,主要是常温或低温湿法(如溶液吸收[3]、低温甲醇洗技术[4])和变压吸附技术(Pressure Swing Adsorption,PSA)。然而净化工段能耗占整个煤制氢的约20%,是节能降耗重要环节之一。目前,溶液吸收和低温甲醇洗工艺共性问题是吸收温度低、溶剂昂贵、脱硫和脱碳需设置独立的吸收和再生系统[5-6],湿法脱碳工艺流程复杂,设备投资和电耗增加,维护和操作费用增加;而常规PSA运行温度不超过70 ℃,需将原料气降温,增加设备投资与流程复杂性,此外无法脱除中温变换气中含硫杂质、NH3、CO等杂质[7],无法一步到位提取高纯H2。
燃烧前碳捕集(正常运行温度在150~350 ℃)[8]为中温变压吸附(Elevated Temperature Pressure Swing Adsorption,ET-PSA)提供了类似煤制氢的工艺背景。针对煤气化后的H2净化,前期研究主要基于新型固体吸附剂改性开发,以满足中温下从含较多水蒸气、CO2等多组分中脱硫脱碳需求。美国Air Product and Chemicals,Inc.[9-10]以钾修饰的复合镁铝氧化物为吸附剂、400 ℃下通过吸附增强水气变换实现了IGCC中煤制合成气同时变换与CO2捕集;美国TDA Research Inc.[11]以改性椰壳活性炭吸附剂实现模拟煤制变换气或碳氢燃料重整气在100~300 ℃下分离CO2;美国MIT的GREEN课题组采用镁基活性炭在180~240 ℃下分离H2/CO2[12],在106 Pa和200 ℃时CO2吸附量为1.3 mmol/g。此外,氧化镁的改性衍生物[13-15]和氧化铝[16]也被用于中温吸附剂。
在相应示范领域,荷兰ECN研究所[17]于2011—2019年基于水滑石吸附剂,开发了吸附增强水气变换技术,在300~350 ℃实现了处理量800 m3/h(标况下)的高炉煤气中温脱除CO及CO2,是国际最早开展示范中温富氢气体脱碳示范的单位。美国TDA公司[11]后于2015—2018年合成了改性介孔碳吸附剂,并搭建了CO2捕集量0.2 kg/h的水气变换-变压吸附装置,在240 ℃实现了中温下变换气中含碳杂质的高效脱除。上述燃烧器碳捕集示范场景初步证明了中温直接脱碳的可行性以及初步经济性,但该技术尚未完全实现产业化,亟需通过现场更大规模中试进一步证明其可行性。
鉴于此,笔者研究改性煤基活性炭,并对其进行氮掺杂,使其更适用于中温高湿环境下H2/CO2分离净化; 搭建并运行中温变压吸附H2/CO2分离净化中试装置,实现关键吸附剂、中温变压吸附工艺突破,通过中试工程示范和验证证明该技术产业化的可行性。
1 试 验
1.1 氮基活性炭的合成与表征
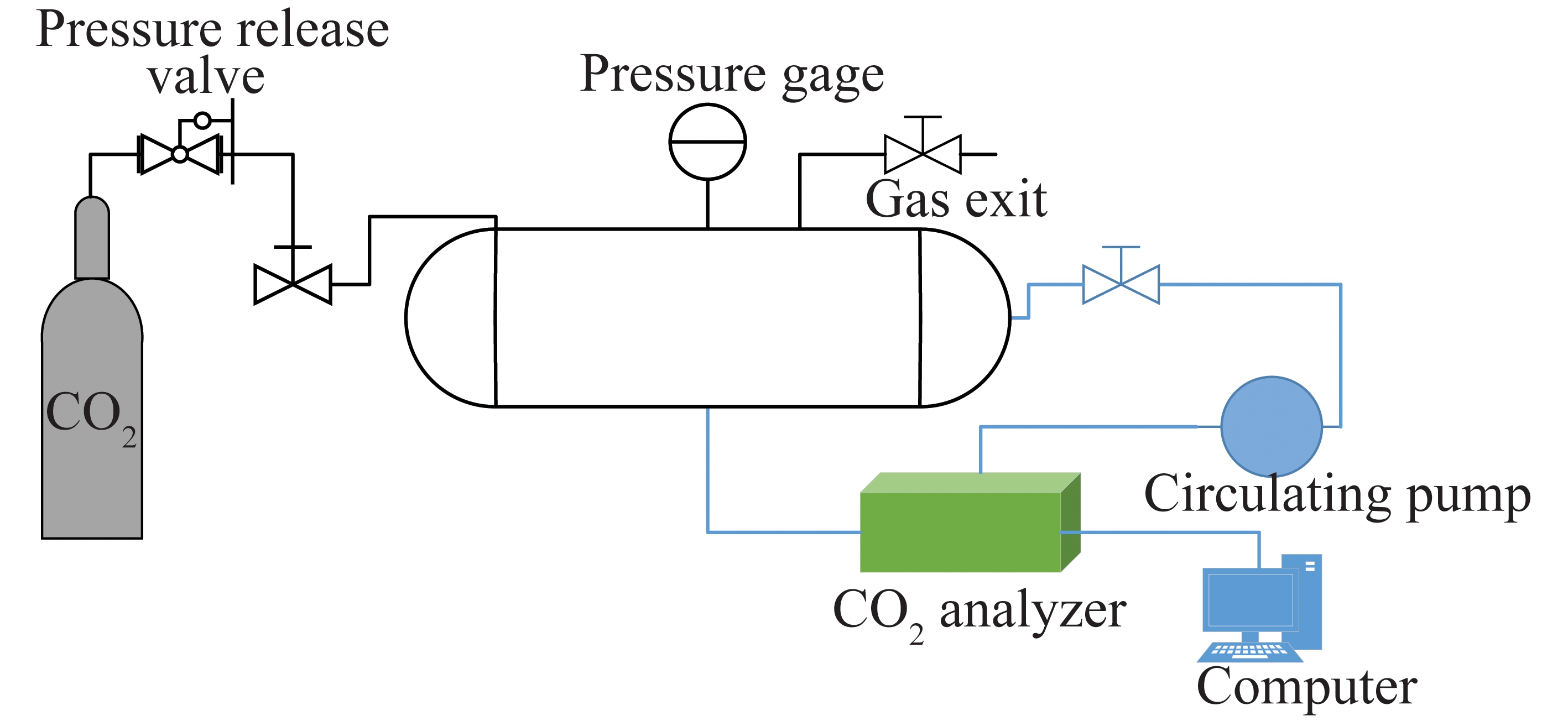
考虑到泉稷煤制气经过二次水气变换,来流温度为216 ℃,选用改性后煤基活性炭作为中温吸附剂。采用国家能源集团宁夏煤业有限责任公司洗选中心CTC-80活性炭产品,符合GB/T 213—2003《煤的发热量测定方法》,含碳量为90%;在尿素醇溶液中进行热浸渍,然后在N2气氛下550 ℃高温活化实现氮掺杂。掺杂后的吸附剂命名为U-80C-N-550。通过引入氮基官能团N-Q、N-5、N-6,增强吸附剂U-80C-N-550的疏水性及其对CO2选择性。使用Thermo SCIENTIFIC公司ESCALAB 250Xi的X射线光电子能谱仪表征材料表面元素分布以及氮掺杂类型、比例和官能团种类;使用北京恒久HCT-1型热重分析仪测试中温代表温度下(200 ℃)材料对CO2的吸附量;使用德国KRÜSS的DSA255型煤接触角测量仪对吸附剂进行疏水性能测试;使用实验室自主搭建的固定床反应器进行吸附剂中温高湿环境下CO2固定床突破试验。
1.2 中试示范装置
1.2.1 工艺原理
中温变压吸附H2/CO2分离技术是净化提纯合成气的关键技术,是常温变压吸附升温后的技术拓展延伸,符合干法净化低能耗低成本的发展方向,适用于各类化石燃料气化或重整气中CO2及少量CO、H2S的可逆脱除。其基本原理与常规常温PSA基本相同,即在特定温度不变的条件下,在加压情况下吸附,减压(抽真空)或常压条件下解吸。可见变压吸附是通过改变压力实现吸附和解吸,中温变压吸附是使温度提升至对应气体露点温度以上(150 ℃),其吸附机理从物理吸附向改性物理吸附甚至吸附热较低的弱化学吸附转变。煤制合成气变换后(原料气)不经大幅降温直接进入净化单元,借助固定床吸附塔内填充的弱化学吸附剂,按照特定中温变压吸附工艺,循环选择性吸附原料气中CO2及H2S分离得到高纯度H2。
1.2.2 工艺流程
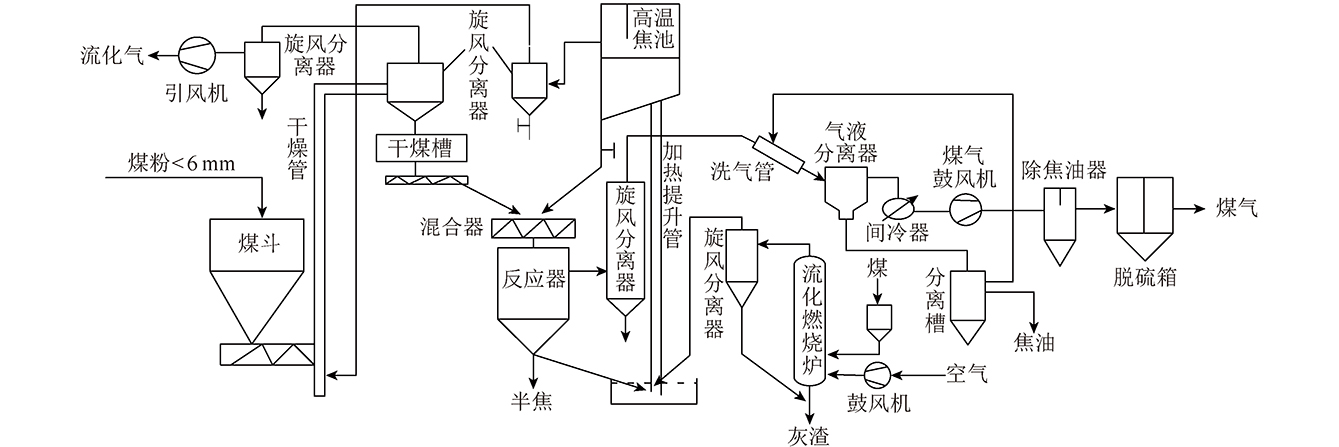
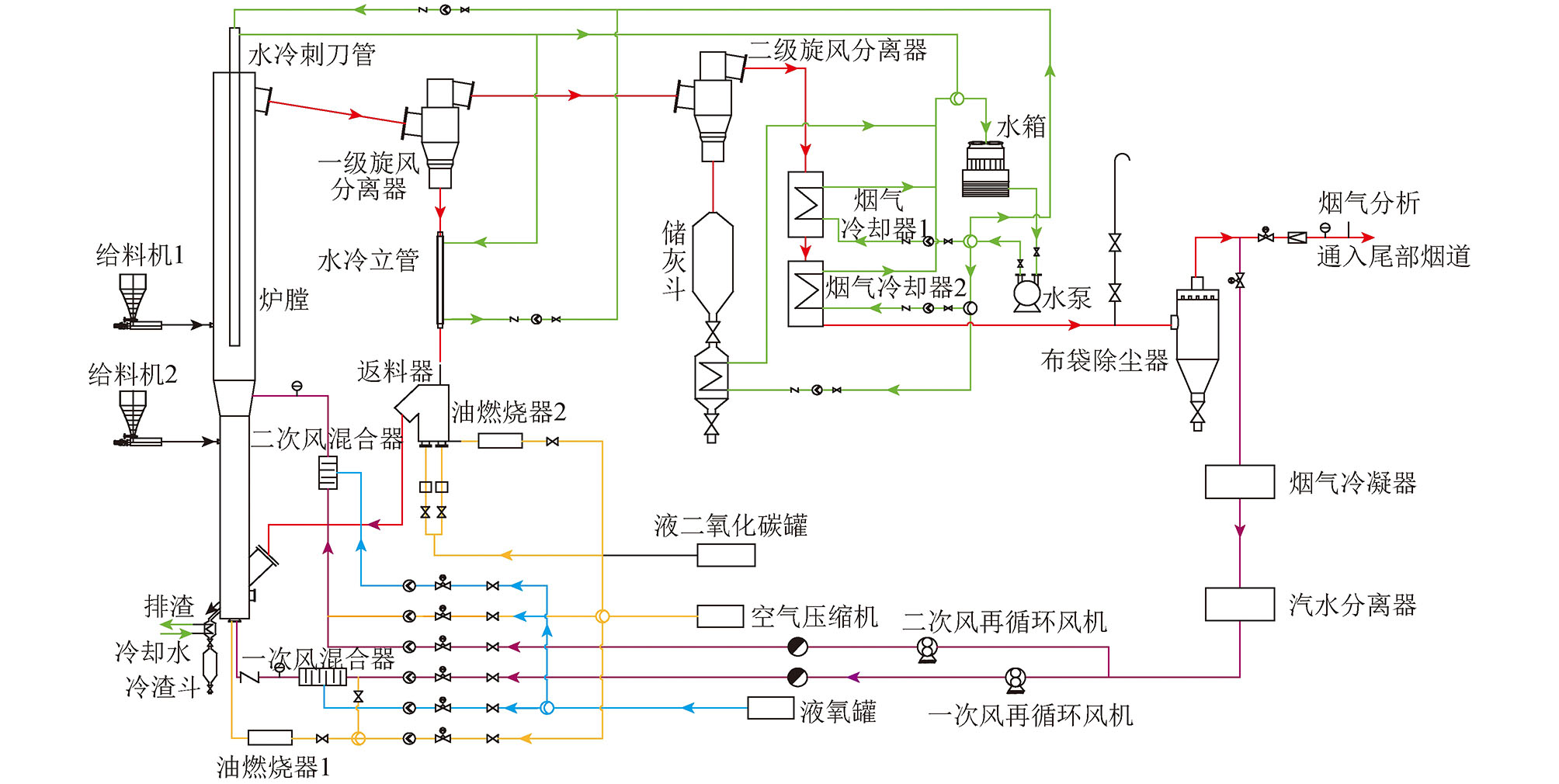
中温变压吸附H2/CO2分离中试示范装置于2020年8月在山西潞安丰喜泉稷能源有限公司建成投入使用,通过中温变压吸附工艺对送入界区的煤制合成气提取高纯H2。煤制合成气二次变换后气体组分约为40% H2,30% CO2,30%水蒸气,1 000×10-6 H2S,少量CO、CH4、N2;考虑到煤制气成分复杂,原料气中还有微量NH3、煤焦油蒸汽、碳酸氢铵蒸汽等。本装置由预处理、除氧、复温换热、中温变压吸附脱硫和中温变压吸附脱碳5个工序构成,对原料气中H2进行净化和提纯。装置的净化和提纯工艺流程如图1所示。

图1 中温变压吸附H2/CO2分离中试流程
Fig.1 Flow chart of ET-PSA H2/CO2 separation pilot test
原料气首先经过预处理、除氧及复温换热,除去原料气中夹带的油、尘和微量氧气等杂质,并使原料气温度降至178 ℃。预处理工序中气体由预处理过滤塔C0001底部进入,气体中油、尘等杂质被截留后从过滤塔顶部流出,进入除氧过滤塔C0002在催化剂作用下脱除原料气中微量O2。除氧后原料气经过复温调温器E0001、水冷器E0002除去原料气中过多水后进入中温变压吸附脱硫工序。从水冷器E0002出来的原料气进入粗脱硫塔C0003A/B和精脱硫塔C0004脱除原料气中微量H2S与微量NH3,脱硫后半成品气由精脱硫塔C0004底部排出,进入中温变压吸附脱碳工序。在中温变压吸附脱碳工序中,原料气从中温吸附塔C1001底部进入,从吸附塔顶部流出。CO2等气体被吸附剂选择性吸附,由于掺填部分变换催化剂,微量CO和H2O反应进一步生成H2,最终产品H2从塔顶流出,经过一段尾气缓冲罐V1001和产品气调温器E3001降温后流出界区。经过一系列均压过程后CO2等杂质气体通过逆放和抽真空方式排出吸附塔,吸附剂得到再生。
1.2.3 运行规程
结合来流温度并考虑侧线管道温度损失,本中试装置拟在180 ℃下运行;据小试结果[18],中温变压吸附工艺步序引入N2充洗、顺充和低压N2清洗、真空等步序提升H2收率及纯度。中温变压吸附脱硫工序可实现可逆脱除H2S,流程见表1。复温换热后的原料气经进口阀进入脱硫工序粗脱硫塔,粗脱硫后的原料气从粗脱硫塔顶部流出进入精脱硫塔,精脱后的原料气进入中温变压吸附脱碳工序。粗脱硫塔可除去绝大部分H2S和NH3,精脱硫进一步除去在粗脱硫中未除去的H2S气体,确保进入脱碳工序气体中无H2S和NH3气体。脱硫工序装置由2台粗脱硫塔、1台精脱硫塔、1台脱硫冷却器、1台脱硫真空泵及12台程序控制阀门和相应的调节阀组成。其中2台粗脱硫塔交替工作从而连续脱硫。1个周期中每个粗脱硫塔均经历吸附(AD)、逆放(BD)、冲洗(P)、抽真空冲洗(P V)、终充(FR)工艺过程。
表1 中温脱硫PSA工艺流程
Table 1 Flow chart of ET-PSA desulfurization

可逆脱除H2S后,原料气进入七塔中温变压吸附脱碳工序,脱除其中CO2及CO,具体流程见表2。中温变压吸附脱碳工序由7台吸附塔、1台解吸气冷却器、1台除水冷却器、1台产品气调温器、1台脱碳真空泵及56台程控阀门和相应调节阀组成。其中每台吸附塔与8排程序控制阀门相连,吸附塔的进气端有3排,出气端有5排。在一个周期中每个粗脱硫塔均经历吸附(AD)、吸附塔均压降压1(ED1)、吸附塔均压降压2(ED2)、吸附塔均压降压3(ED3)、吸附塔均压降压4(ED4)、吸附塔顺向降压(CD)、吸附塔N2顺向冲洗(R)、逆向放压(BD)、清洗(P)、抽空清洗(P V)、吸附塔均压升压4(EP4)、吸附塔均压升压3(EP3)、吸附塔均压升压2(EP2)、吸附塔均压升压1(EP1)、吸附尾气对吸附塔最终升压(FR)工艺过程。由于七塔做4次均压且每次吸附占用1塔,故简称7-4-1工艺。
表2 中温脱碳PSA工艺流程
Table 2 Flow chart of ET-PSA decarbonization

1.3 H2回收率及纯度计算
1.3.1 H2收率计算
H2纯度及收率是净化过程的重要参数。N2是合成氨的另一种重要产物,本文记作有效气体。H2S、氧气氩气合峰、N2、CH4、CO和CO2使用气相色谱仪和分析仪检测,H2使用分析仪检测。由于直接测量H2纯度不精确,因此H2纯度采用式(1)扣除法,用100%减去杂质组分计算得到H2(含有效气N2)纯度:
c(H2 N2)=100-∑ci,
(1)
式中,c(H2 N2)为H2(含有效气N2)纯度,%;ci为各类杂质气体体积分数,%。
1.3.2 H2回收率计算及误差
1)H2回收率计算。装置运行时,各工序的气体流量、温度和压力可被中控系统采集、存储,定时对各工序气体采样测试气体成分,用于检测装置系统运行情况和H2回收率y,具体为

(2)
其中,Fin为进入系统气体的流量,即原料气流量,m3/h;cin(H2)为进入系统气体H2体积分数,%;Fout为出系统气体的流量,出系统的气体包括产品气和顺放气,m3/h;cout(H2)为出系统气体(产品气和顺放气)H2体积分数,%。式(2)可表示为

(3)
式中,FP为进入系统气体的流量,即产品气流量,m3/h;cP(H2)为产品气H2体积分数,%;FCD为顺放气流量,m3/h;cCD(H2)为顺放气的H2体积分数,%。
2)H2回收率误差分析。函数误差关系见表3。
表3 函数误差关系
Table 3 Function error calculation table

注:m为函数,n1、n2为自变量;误差传递公式表示由于n1、n2误差而导致函数m的误差变化情况。
H2回收率为

(4)
式中,f1、f2、f3、c1、c2、c3分别为产品气流量、顺放气流量、原料气流量、产品气H2浓度、顺放气H2浓度和原料气H2浓度。
依据表3误差计算公式,H2回收率误差为

(5)
式中, Δ(f1c1)=±(f1Δc1 c1Δf1),Δ(f2c2)=±(f2Δc2 c2Δf2),Δ(f3c3)=c3Δf3。c3变化甚微,可作为常数处理。
Δ(f1c1)=±(f1Δc1 c1Δf1),Δ(f2c2)=±(f2Δc2 c2Δf2),Δ(f3c3)=c3Δf3。c3变化甚微,可作为常数处理。
2 结果与讨论
2.1 吸附剂疏水性及CO2选择性
活性炭中氮掺杂形式主要是吡咯型氮(N-5),吡啶型氮(N-6)和石墨型氮(N-Q)3类。其中N-6可作为活性位点捕获CO2,因为N-6的N有孤对电子,可贡献给酸性CO2分子的亲电位点形成氨基甲酸酯化合物[19]。原料和吸附剂XPS结果如图2所示。由图2可知,合成的U-80C-N-550的N含量明显高于原料CTC-80活性炭产品。总氮含量最多,N/O比最高可达1.22,氮基官能团取代酸性氧基官能团,使表面极性吸附位点减少,且与水分子生成氢键的氧元素含量降低[20],对水的吸附性减弱,其疏水性增强。

图2 原料和U-80C-N-550 N 1s能谱对比
Fig.2 Comparison of energy spectra of raw material and U-80C-N-550 N 1s
使用综合热重分析仪测试材料CO2吸附量,以材料质量变化测得吸附量。材料CO2吸附量的TGA测试结果如图3所示。原料在200 ℃下,CO2吸附量为1.040 mmol/g,最优样品U-80C-N-550的CO2吸附量可达1.197 mmol/g,对CO2吸附性能明显增强,主要是由于样品表面氮官能团含量不同,活性炭表面的N-5、N-6可作为活性位点捕获CO2。

图3 CO2的吸附量对比
Fig.3 Comparison of CO2 adsorption capacity
增强疏水性能可提升吸附剂在工业高湿气体中对CO2的吸附选择性,原料CTC-80活性炭产品与氮基活性炭U-80C-N-550的水接触角如图4所示。可知U-80C-N-550石墨化程度增加,N-Q的掺杂量和掺杂比例有利于提升材料的疏水性能,接触角拓展到132.3°,明显大于原料。疏水性能提高有利于增强高湿度富氢气氛中CO2的吸附选择性。按照泉稷公司二次变换出口工业气体成分比例,在200 °C、101 325 Pa高温高湿环境下,开展富氮活性炭对水蒸气耐受性及其对CO2吸附性能测试,测试结果如图5所示,可知与原料CTC-80活性炭相比,富氮活性炭对CO2的吸附性能明显较强,CO2穿透时间延长;对比不同条件合成的富氮活性炭,U-80C-N系列吸附剂对应CO2穿透时间最长且突破斜率最低,说明其在高湿环境中对CO2吸附性能最好。

图4 原料和U-80C-N-550水接触角对比
Fig.4 Comparison of contact angles between raw material and U-80C-N-550

图5 CO2穿透曲线
Fig.5 CO2 penetration curves
2.2 中温脱硫脱碳工序
装置最初设计时,预计先脱硫再脱碳;但现场试验发现实际来流原料气中含有NH3,中试研究改变为中温下先脱除NH3和H2S,再脱除碳。NH3使用氨气报警仪检测,H2S、O-Ar、N2、CH4使用气相色谱仪检测,CO和CO2使用气相色谱仪和气体分析仪检测,H2使用气体分析仪检测。
2.2.1 中温变压吸附脱硫脱氨
经测量,原料气中H2S体积分数为1 000×10-6~2 000×10-6,NH3体积分数为500×10-6~800×10-6(随时间波动)。
首先验证了NH3突破时间,设置粗脱过程脱硫脱氨周期为T1(逆放1):15 min,T2(逆放2):5 min,T3(N2清洗):15 min,T4(N2清洗 抽真空):3 min,T5(终充):35 min。在终充(T5)环节不同时间取样测试NH3及H2S含量,见表4。可知终充1 900 s 后,NH3实现突破。终充结束后切换B塔进行脱硫脱氨,B塔中终充700 s后取样测试NH3体积分数突增至131×10-6,说明NH3在B塔终充实现突破的时间为1~15 min。中试运行另一时间段采样测试的NH3及H2S体积分数见表5,可知通过AB塔多次循环切换,脱硫塔A终充剩余200 s时NH3为0,脱硫B塔终充全部为0(NH3)。证明多次循环后,装置在可逆脱硫的同时,实现了可逆脱氨且自净。以多次采样结果为依据,考虑实际操作中压力释放时间,最终确定脱硫时序为T1:16 min,T2:5 min,T3:17 min,T4:1 min,T5:36 min,半周期共75 min。
表4 NH3及H2S体积分数
Table 4 Volume fraction of NH3 and H2S

表5 另一时间段NH3及H2S体积分数
Table 5 Volume fraction of NH3 and H2S in another time

2.2.2 中温变压吸附脱碳
实现可逆脱除NH3和H2S后,研究了原料气进入七塔中温变压吸附脱碳工序,脱除其中CO2及CO。一个塔脱碳时序为T1:50 s,T2:50 s,T3:30 s,T4:25 s,共计155 s,全周期共1 086 s。中试某日,对原料气、产品H2、顺放、逆放等典型点位采样测试各组分含量,精细组分采用色谱重复测量,H2和CO2用实时气体流量计测试(分析仪均为0~100%量程,中间值组分测量误差较大),结果见表6、7。顺放气中H2含量高,后期压缩后接至原料气以提升H2收率;第1段脱硫逆放和第2段脱碳逆放均富含杂质气体,可考虑H2S、特别是CO2进一步富集与利用。2段后的产品气中,除N2、Ar2外各类杂质气体基本脱除,浓度处于色谱检测限下。
表6 各组分含量色谱仪测试结果
Table 6 Content of each component measured by chromatograph

表7 各组分含量分析仪测试结果
Table 7 Content of each component measured by analyzer

2.3 中试现场试验结果
2020年10月开始在泉稷现场开展中试试验。2022年初,该中试已经累计运行2 886 h,期间未更换吸附剂。
2.3.1 H2纯度计算结果
中试运行试验期间,对原料气和各工序出口气体成分进行定时点检,包括原料气、脱硫气(精脱出口气或粗脱出口气)和产品气成分检测,确保各控制点组分符合设计值,各工序正常运行。其中,变压吸附脱硫工序出口气体中无NH3且H2S需小于10×10-6,中温变压吸附脱碳工序入口无H2S检出。中试运行调试时,使用气袋采样并利用气体分析仪检测H2体积分数,均在99.9%左右。中试正式运行期间,为进一步确认产品气H2成分及其组分的准确性和可信度,现场采集产品气送至第三方检测,检测结果见表8。结果发现产品H2中总烃体积分数0.66 μmol/mol、O2体积分数<0.5 μmol/mol、He体积分数114 μmol/mol、Ar体积分数9.3 μmol/mol、N2体积分数2 553 μmol/mol、CO2体积分数<0.3 μmol/mol、CO体积分数<0.1 μmol/mol、H2S体积分数<0.000 5 μmol/mol、卤素体积分数<0.01 μmol/mol、NH3体积分数<0.03 μmol/mol。扣除法计算得到H2纯度为99.987 5%(含有效气N2),不仅满足合成氨,且满足GB/T 37244—2018《质子交换膜燃料电池汽车用燃料 氢气》燃料电池用氢标准。
表8 运行产品气检测结果
Table 8 Test result of product hydrogen

2.3.2 H2回收率计算结果
现以1 d优化顺放时间后工况为例,2021-10-10记录结果见表9,平均每4 h采样测试1次,取1 d中5次计算平均H2回收率为当天回收率,防止偶然性因素对结果的影响,可知H2收率超过99%。
表9 中试运行H2收率计算
Table 9 H2 yield calculation of pilot operation

2.3.3 H2回收率误差计算结果
计算H2回收率误差时,f1、 f2、 f3、c1、c2和c3取平均值分别为1 078.0、1 521.4、6 112.6 m3/h(标况下)和0.998、0.747和0.367。孔板流量计误差为1%,气体分析仪误差为2%,所以流量f误差为1%,浓度c误差为2%。于是Δf1、Δf2、Δf3、Δc1和Δc2分别为0.01f1、0.01f2、0.01f3、0.02c1和0.02c2。代入式(2)得到H2回收率误差为±4%。
2.3.4 中温变压吸附H2/CO2分离能耗分析
中试装置2021-08-26—2021-09-07运行期间(24 h连续不间断运行)公用工程相关数据见表10,每8 h记录公用工程消耗数值,以此为核算依据,平均每小时电耗64.3 kWh;中压蒸汽0.48 t;低压N2体积分数为149 m3(标况下);仪表空气33.5 m3(标况下)。
表10 中试公用工程能耗
Table 10 Utilities expenses of the pilot plant

仅折算电耗,中试净化H2净化运行成本约为0.051 kWh/m3(主要为真空泵消耗),相比丰喜泉穆厂内低温甲醇洗H2净化电耗0.079 kWh/m3(主要为输运液相工质及冷量电耗)可以节约净化运行成本约35%。
3 结 论
1)开发并合成了新型富氮活性炭吸附剂,通过表面氮官能团改性,所合成的U-80C-N-550在200 ℃下CO2吸附量可达1.197 mmol/g,并实现了高水蒸气含量下CO2的选择脱除。
2)提出了N2充洗、N2清洗等新工艺,提升中温变压吸附净化工段H2收率至99%。以丰喜泉稷煤制变换气为侧线原料气,搭建了原料气处理量5 000 m3/h(标况下)的中温变压吸附H2/CO2分离中试试验装置,实现了煤制气的H2净化连续示范,累计运行时间超2 800 h。经第三方检测,通过中温变压吸附中试,H2纯度达99.987 5%,主要CO2、CO、H2S、NH3等杂质残留均满足燃料电池氢气对杂质要求。
3)依据中试12 d连续运行结果,其制氢电耗比已有低温甲醇洗低35%,净化精度和收率均优于现有低温甲醇洗,验证了中温干法净化技术的工业可行性及经济性。
4)本技术拓宽了能源化工领域传统气体净化温度区间,使净化运行温区更贴近原料气制取温度(如煤气化、水气变换、碳氢燃料重整等),可改善净化工段冷热病、简化净化工艺流程、降低净化设备投资成本、节省净化运行成本。此外,中温变压吸附技术可定向脱除H2中碳、硫、氨等杂质,为燃料电池级H2净化提供新方案。中温变压吸附气体净化技术对煤化工富氢气体净化工艺革新及燃料H2规模净化技术的发展具有重要意义。
[1] NIKOLAIDIS P,POULLIKKAS A. A comparative overview of hydrogen production processes[J]. Renewable and Sustainable Energy Reviews,2017,67:597-611.
[2] 孙津生,李燕. 低温甲醇洗工艺流程模拟:甲醇洗涤塔的模拟[J]. 甘肃科学学报,2007,19(2):50-53.
SUN Jinsheng,LI Yan,Simulation of low temperature methanol washing process:Simulation of methanol scrubber tower[J]. Gansu Scientific Bulletin,2007,19 (2):50-53.
[3] QUINTELLA C M,HATIMONDI S A,MUSSE A P S,et al. CO2
capture technologies:An overview with technology assessment based on patents and articles[J]. Energy Procedia,2011,4:2050-2057.
[4] 朱兆友,李鑫,徐东芳,等. 低温甲醇洗中变换气脱硫脱碳过程的模拟优化[J]. 能源化工,2015,36(6):20-27.
ZHU Zhaoyou,LI Xin,XU Dongfang,et al. Simulation and optimization of desulphurization and decarbonization process of conversion gas in low temperature methanol washing[J]. Energy Chemical Industry,2015,36(6):20-27.
[5] 葛志颖. 煤基18/30装置变换气脱硫脱碳工艺技术的选择[J]. 气体净化,2009,9(2):13-16.
GE Zhiying. Selection of conversion gas desulfurization and decarbonization technology for coal-based 18/30 plant [J]. Gas Purification,2009,9(2):13-16.
[6] 李志娟. 活性MDEA溶液脱碳技术与变压吸附脱碳技术的比较[J]. 新疆化工,2003,3(3):10-14.
LI Zhijuan. Comparison of active MDEA solution decarburization technology and pressure swing adsorption decarburization technology [J]. Xinjiang Chemical Industry,2003,3(3):10-14.
[7] 管英富,武立新. 常温高效变压吸附提纯一氧化碳新技术[J]. 天然气化工:C1化学与化工,2007,32(1):61-63.
GUAN Yingfu,WU Lixin. New technology for purification of carbon monoxide by high efficiency pressure swing adsorption at normal temperature [J]. Natural Gas Chemical Industry:C1 Chemistry &Chemical Engineering,2007,32(1):61-63.
[8] JANSEN D,GAZZANI M,MANZOLINI G,et al. Pre-combustion CO2 capture[J].International Journal of Greenhouse Gas Control,2015,40:167-187.
[9] CARVILL B T,HUFTON J R,ANAND M,et al. Sorption-en-hanced reaction process[J]. AIChE Journal,1996,10:2762-2772.
[10] HUFTON J R,MAYORGA S,SIRCAR S. Sorption-enhanced reaction process for hydrogen production[J]. AIChE Journal,1999,45(2):248-256.
[11] ALPTEKIN G O,JAYARAMAN A,DIETZ S,et al. A low cost,high capacity regenerable sorbent for pre-combustion CO2 capture[R]. Wheat Ridge:TDA Research Inc.,2012.
[12] LIU Z,GREEN W H. Experimentalinvestigation of sorbent for wa-rm CO2 capture by pressure swing adsorption[J]. Industrial &Engineering Chemistry Research,2013,52(28):9665-9673.
[13] MEIXNER D L,ARTHUR D A,GEORGE S M . Kinetics of desorption,adsorption,and surface diffusion of CO2 on MgO(100)[J]. Surface Science,1992,261(3):141-154.
[14] BHAGIYALAKSHMI M,JI Y L,JANG H T. Synthesis of mesoporous magnesium oxide:Its application to CO2 chemisorption[J]. International Journal of Greenhouse Gas Control,2010,4(1):51-56.
[15] GAO W,ZHOU T,GAO Y,et al. Molten salts-modified MgO-based adsorbents for intermediate-temperature CO2 capture:A review[J]. Journal of Energy Chemistry,2017,3(26):830-838.
[16] STEPHANE W,PAUL D C,WIM G H,et al. In situ XRD detection of reversible dawsonite formation on alkali promoted alumina:A cheap sorbent for CO2 capture[J]. European Journal of Inorganic Chemistry,2010,2010(17):2461-2464.
[17] BOON J,COBDEN P D,VAN DIJK H A J,et al. High-temperature pressure swing adsorption cycle design for sorption-enhanced water-gas shift[J]. Chemical Engineering Science,2015,122:219-231.
[18] LI S,HAO P,ZHU X,et al. On-site demonstration of a two-stage deep desulfurization and decarbonization pressure and temperature swing adsorption unit at elevated temperature for hydrogen production[J]. Adsorption,2019,25:1683-1693.
[19] MANMUANPOM N,THUBSUANG U,DUBAS S T,et al. Enhanced CO2 capturing over ultra-microporous carbon with nitrogen-active species prepared using one-step carbonization of polybenzoxazine for a sustainable environment[J]. Journal of Environmental Management,2018,223:779-786.
[20] LI L,QUINLIVAN P A,KNAPPE D R U. Effects of activated carbon surface chemistry and pore structure on the adsorption of organic contaminants from aqueous solution[J]. Carbon,2002,40(12):2085-2100.
Study and demonstration of H2/CO2 separation of syngas from coal by elevated temperature pressure swing adsorption

LI Shuang,ZHANG Jing,WANG Dongdong,et al.Study and demonstration of H2/CO2 separation of syngas from coal by elevated temperature pressure swing adsorption[J].Clean Coal Technology,2023,29(3):92-101.