2种离子液体对水泥窑窑尾烟气CO2吸收特性试验研究
Experimental investigation on the absorption characteristics of two ionic liquids for CO2 in cement kiln tail gas
闫全英(1970—),女,河北宣化人,副教授,博士,主要从事相变材料储能、地板辐射供暖、热泵余热利用等方面的研究。E-mail:yanquan
ying@bucea.edu.cn。通讯作者:潘利生(1982—),男,副研究员,主要从事低品位余热高效回收利用关键技术研究。E-mail:panlisheng@imech.ac.cn
YAN Quanying,LYU Yifan,PAN Lisheng,et al.Experimental investigation on the absorption characteristics of two ionic liquids for CO2 in cement kiln tail gas[J].Clean Coal Technology,2020,26(5):147-152.
0 引 言
2019年我国能源消耗总量达486 000万t标准煤,比2018年增长4.7%[1]。工业领域能源消耗巨大,2017年占全国能源消耗总量的66%[2]。工业生产同步排放大量CO2,水泥行业的熟料生产工艺排放的CO2占全年人为CO2排放总量的11.7%[3]。水泥窑窑尾烟气中,CO2最高占比可达33%左右[4]。因此,水泥窑窑尾烟气的CO2捕集是工业领域碳减排的重要组成部分。
目前,CCS(Carbon capture and storage)技术在大规模减少CO2排放方面具有较大潜力,CO2捕集是关键环节之一[5]。CO2捕集可分为3种:燃烧前捕集、燃烧后捕集和富氧燃烧技术[6-7]。燃烧前捕集主要针对天然气联合循环(NGCC)和综合气化联合循环(IGCC)电站,将燃料转化成H2和CO2再进行分离[8];燃烧后捕集适用于水泥厂、火电厂等,对已建电站无需大范围改动,可在短期内有效降低CO2排放[9];富氧燃烧技术通过使用高浓度氧气参与燃烧获得高浓度CO2,但对已建电厂改造困难[10]。水泥窑窑尾烟气适合使用燃烧后捕集方式。常用的燃烧后捕集CO2方法主要有膜分离法、吸附分离法、低温分离法和吸收分离法[11]。本文研究的水泥窑窑尾烟气具有CO2浓度较高、分压较低的特点。对于吸收分离方法,常用的化学吸收法包括氨水吸收法、有机胺溶液吸收法、离子液体吸收法等,其中胺基吸收法被认为最具商业应用价值[12]。但烷醇胺吸收CO2后会产生较强的腐蚀性,影响设备的安全运行,降低系统的使用寿命[13]。氨水吸收法虽不存在腐蚀设备问题,但氨逃逸问题较严重[14]。由有机阳离子和阴离子组成的离子液体具有低熔点、高稳定性、溶解性能可调节、不易挥发、可再生等优点[15-17],在众多领域中具有应用潜力。Hospital-Benito等[18]通过分析6种离子液体的CO2吸收性能验证了离子液体捕集CO2的可行性。Lyu等[19]研究了氨基功能化离子液体双相溶剂[TETAH][Lys]乙醇水溶液的CO2捕集性能,研究表明该离子液体双相溶剂吸收CO2性能高效,且需要的能量较低。Liu等[20]为降低再生能耗和黏度,提出了一种新型功能化离子液体[TEPAH][2-MI],与有机溶剂混合来捕集CO2,通过试验得出其CO2吸收性能较好,且经过5次再生循环效率稳定。
前人研究常用纯CO2测试离子液体对CO2的吸收性能,但实际工程应用时需处理的气体为混合烟气,其中的N2、H2S、CH4等都可能对离子液体的CO2吸收性能产生影响。Wu等[21]指出,烟气中的SO2会明显降低离子液体对CO2的吸收性能,因为SO2更易与离子液体的活性中心发生反应。因此,在考察离子液体对CO2的捕集性能时,还需重点分析混合烟气中其他组分对CO2吸收性能的影响规律。Akhmetshina等[22]测定了离子液体二元混合物在不同分压和温度下对H2S和CO2的溶解度,研究表明基于2-羟乙基铵阳离子的离子液体对H2S吸收性能较高。Shaahmadi等[23]测定了在[Bmim][Ac]、[Bmim][BF4]及其二元混合物中CO2和CH4混合物的溶解度和选择性,结果表明,在CO2/CH4=25/75(摩尔比)时,离子液体可达到最高SCO2/CH4值。Handy等[24]研究了H2S在离子液体[BMIM][Br]中的溶解度和选择性吸收,证明[BMIM][Br]具有可脱除CO2/H2S混合物中H2S的潜在能力。Jalili等[25]测定了CO2、H2S和两者组成的混合气体在离子液体[Cnmim][Tf2N]中的溶解度,结果表明在离子液体中H2S的溶解度是CO2的2倍左右,且H2S在[Cnmim][Tf2N]中的溶解度随碳原子数n的增加而增大。本文以[M4Gu]Ac(四甲基胍醋酸盐)和[TMG][Lac](四甲基胍乳酸盐)为研究对象,分别考察其在30、50、70 ℃下对纯CO2和水泥窑窑尾模拟烟气中CO2的吸收特性,并对2种离子液体进行多次吸收和再生循环,研究离子液体重复使用次数对CO2吸收性能的影响。
1 试 验
1.1 试验系统
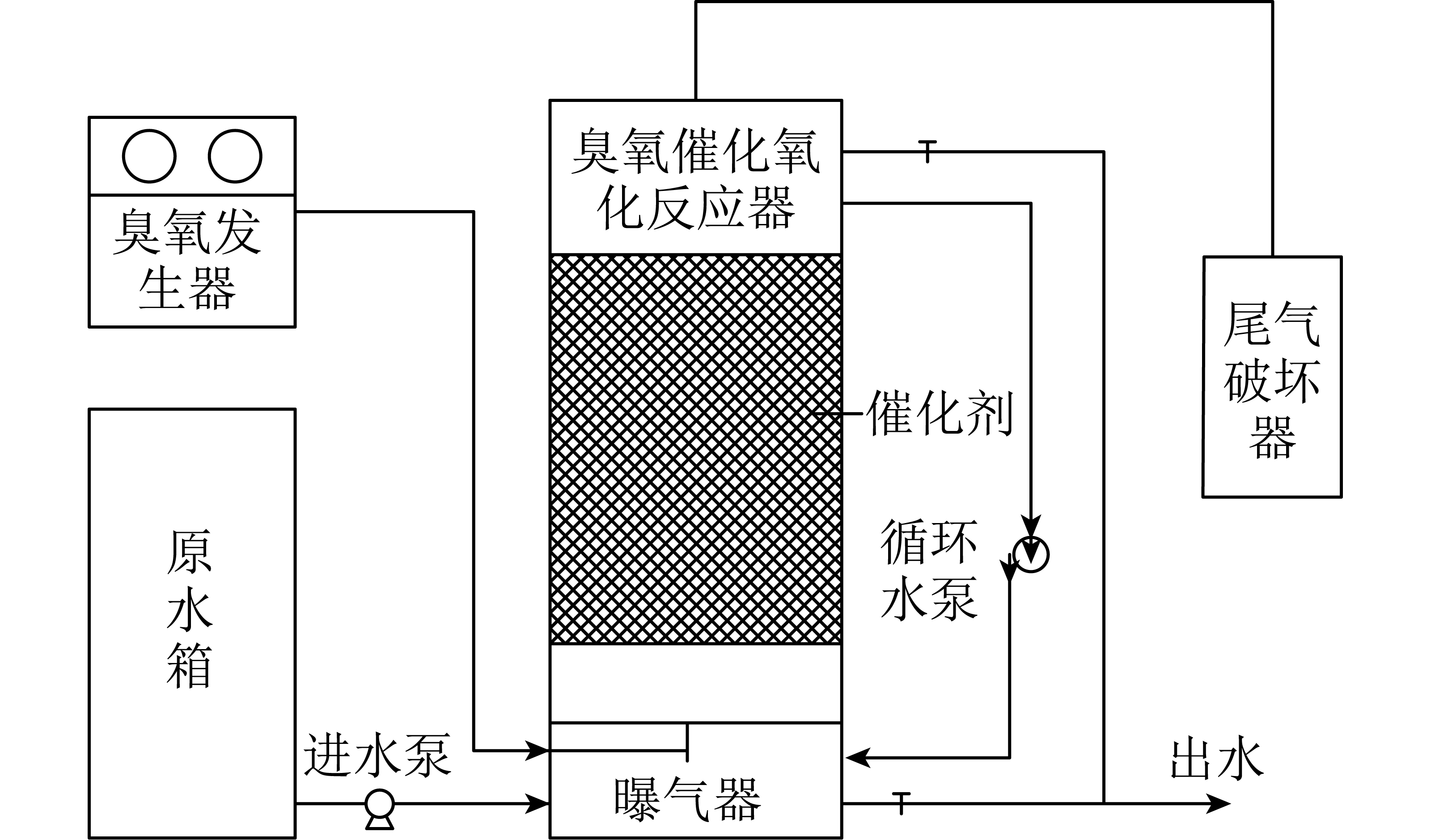
试验系统由真空干燥箱、滑片式真空泵、油浴锅、试管、CO2气瓶、O2气瓶、N2气瓶、气体质量流量控制器和分析天平构成,如图1所示。试验中使用的离子液体为纯度≥98%的[M4Gu]Ac(四甲基胍醋酸盐)和纯度≥98%的[TMG][Lac](四甲基胍乳酸盐)。试验仪器的具体规格参数和用途见表1。

图1 离子液体吸收CO2试验系统
Fig.1 Experimental system for CO2 absorption by ionic liquids
表1 仪器参数和用途
Table 1 Instrument parameters and usage

仪器参数用途真空干燥箱型号:DZF-6050控温范围:(室温+10)~250℃温度分辨率:0.1℃温度波动率:±1℃真空度:<133Pa工作环境温度:5~40℃试验前去除离子液体中的CO2和水滑片式真空泵型号:TWX最大流量:60L/min极限真空度:2Pa对真空干燥箱抽真空油浴锅最高温度:300℃精度:±1.0℃控制离子液体吸收和解吸CO2的工作温度气瓶纯度为99.99%的CO2、O2和N2为试验研究提供纯度为99.99%的CO2、O2和N2气体质量流量控制器型号:CS200A精度:±0.35%F.S.工作温度范围:5~45℃耐压:3MPa调节和控制模拟烟气中CO2、O2和N2的组成比例分析天平型号:FR224CN最大称量:220g分度值:0.0001g典型稳定时间:4s测量离子液体质量
1.2 试验方法
采用真空干燥箱对离子液体进行真空干燥,去除离子液体中可能含有的CO2和水分。在常压条件下(101.3 kPa),将盛有1.0 g离子液体的试管置于30 ℃油浴锅中,纯CO2以匀速通过离子液体,经一段时间后取出试管,停止纯CO2通入,待试管中离子液体平稳后,用分析天平测量离子液体质量后,将试管放回油浴锅内,继续通入纯CO2进行试验,重复多次,记录离子液体的质量变化规律。调节油浴锅温度50、70 ℃,同样方法测量离子液体对CO2的吸收特性。
由于混合气体组分对离子液体的CO2吸收性能具有较大影响,为提高测试精度,在模拟烟气中CO2吸收特性试验中,采用4.0 g离子液体,并使模拟烟气以100 mL/min的平均速度通过离子液体。模拟烟气由3个气瓶提供的高纯度气体混合而成,并通过气体质量流量控制器对3种气体比例进行调节和控制,模拟烟气中CO2/O2/N2=0.337/0.045/0.618。
在离子液体多次吸收和再生循环试验中,离子液体吸收CO2达到饱和时,将纯N2通入离子液体,降低离子液体中CO2分压,使CO2从离子液体中排出,此时离子液体发生CO2解吸反应。离子液体中的CO2被全部排出后,离子液体完成再生,再次进行CO2吸收试验。
根据试验中测得的离子液体质量,离子液体对CO2的吸收量由式(1)计算。

(1)
式中,qabs-des为离子液体对CO2的吸收量或解吸收量,mol/mol(CO2/IL);m(CO2)为吸收或解吸收CO2的质量,g;M(CO2)为CO2摩尔质量,g/mol;mIL为离子液体质量,g;MIL为离子液体摩尔质量,g/mol。
2 结果和讨论
2.1 工作温度的影响
工作温度对离子液体吸收CO2特性具有重要影响,在常压条件下,考察了离子液体[M4Gu]Ac和[TMG][Lac]在30、50和70 ℃对纯CO2的捕集效果,如图2所示。在相同工作温度下,2种离子液体对CO2的吸收量随时间的延长呈增加趋势,且增加速率逐步减小,吸收量最终稳定在极大值,即为离子液体在该工作温度下的CO2最大吸收量。工作温度为30 ℃时,离子液体[M4Gu]Ac和[TMG][Lac]在160 min后基本达到饱和,最大吸收量分别为0.148 和0.134 mol/mol(CO2/IL);50 ℃时,[M4Gu]Ac和[TMG][Lac]需18 min左右达到饱和状态,最大吸收量分别为0.120和0.109 mol/mol(CO2/IL);70 ℃时,[M4Gu]Ac和[TMG][Lac]仅用6 min左右即达到饱和状态,最大吸收量分别为0.073和0.056 mol/mol(CO2/IL)。可以看出,在相同工况下,[M4Gu]Ac对CO2的最大吸收量始终大于[TMG][Lac],表明[M4Gu]Ac对纯CO2的吸收能力强于[TMG][Lac]。
工作温度对[M4Gu]Ac和[TMG][Lac]的CO2吸收能力具有较大影响,比较图2可以得出,2种离子液体对CO2的最大吸收量随工作温度的升高呈下降趋势,70 ℃时[M4Gu]Ac和[TMG][Lac]的最大吸收量最小,仅为2种离子液体在30 ℃时最大吸收量的49.3%和41.7%、50 ℃时最大吸收量的60.8%和51.4%。因为随着温度升高,离子液体的黏度和表面张力等逐渐减小,增加了离子液体的活化能,导致其分子间作用力减少,从而降低了离子液体对CO2的吸收量。同时,随着温度升高,CO2的最大吸收量减少,吸收能力降低,离子液体更易达到饱和状态,所以达到饱和需要的时间变短。

图2 常压条件下[M4Gu]Ac和[TMG][Lac]对CO2吸收特性
Fig.2 CO2 absorption characteristics of [M4Gu]Ac and [TMG][Lac] under normal pressure
2.2 再生次数的影响
离子液体吸收CO2达到饱和时,将纯N2通入离子液体,降低离子液体内CO2分压,使CO2逐渐逸出。若将纯N2持续通入,离子液体内CO2含量会持续降至0,此时离子液体完成再生,再次用于CO2吸收。通过离子液体[M4Gu]Ac和[TMG][Lac]在常压、70 ℃条件下重复吸收和解吸试验,考察再生次数对离子液体最大吸收量的影响,如图3所示。2种离子液体[M4Gu]Ac、[TMG][Lac]在5次的吸收和解吸过程中,CO2在离子液体中的溶解量随时间的变化趋势完全相同,[M4Gu]Ac的5次吸收极大值分别为0.072 7、0.071 6、0.072 7、0.072 7和0.072 8 mol/mol(CO2/IL),[TMG][Lac]的5次吸收极大值分别为0.055 7、0.058 3、0.057 8、0.057 4和0.057 4 mol/mol(CO2/IL),可见最大吸收量基本保持不变,表明离子液体重复使用对吸收速率、最大吸收量、解吸速率等几乎无影响。

图3 离子液体在70 ℃下重复吸收/解吸收CO2特性
Fig.3 Repeated CO2 absorption/desorption characteristics of ionic liquids at 70 ℃
2.3 水泥窑窑尾模拟烟气的影响
混合气体中的其他成分会降低混合气体和离子液体内的CO2分压,从而制造更有利于CO2解吸的环境。在常压条件下,采用转炉模拟烟气,分别考察2种离子液体[M4Gu]Ac和[TMG][Lac]在30、50、70 ℃对模拟烟气中CO2的吸收性能(图4),间接反映了混合气体组分对CO2吸收性能的影响。
由图4可知,2种离子液体对模拟烟气中CO2的吸收性能远低于其对纯CO2的吸收性能。工作温度为30 ℃时,[M4Gu]Ac、[TMG][Lac]对模拟烟气中CO2的最大吸收量仅为0.033、0.028 mol/mol(CO2/IL),相当于其对纯CO2最大吸收量的22.3%和20.9%;50 ℃时,[M4Gu]Ac、[TMG][Lac]对模拟烟气中CO2的最大吸收量为0.008、0.014 mol/mol(CO2/IL),约为其对纯CO2最大吸收量的6.7%和12.8%;70 ℃时,[M4Gu]Ac和[TMG][Lac]对模拟烟气中CO2的最大吸收量为0.006和0.011 mol/mol(CO2/IL),约为其对纯CO2最大吸收量的8.2%和19.6%。图4(a)中,2种离子液体的CO2吸收量曲线相交,说明该工况下,开始阶段[TMG][Lac]对模拟烟气中CO2的吸收速率较大,但后期[M4Gu]Ac对模拟烟气中CO2的吸收速率较大,达到饱和时,[M4Gu]Ac的CO2最大吸收量高于[TMG][Lac]。在50、70 ℃下,2种离子液体对模拟烟气中CO2的吸收量曲线没有明显交叉点,说明[TMG][Lac]对模拟烟气中CO2的吸收速率始终大于[M4Gu]Ac,达到饱和时,[TMG][Lac]的CO2最大吸收量高于[M4Gu]Ac的最大吸收量,与30 ℃时的结论相反。

图4 常压条件下[M4Gu]Ac和[TMG][Lac]对水泥窑窑尾烟气中CO2吸收特性
Fig.4 Absorption characteristics of [M4Gu]Ac and [TMG] [lac] for CO2 in tail gas of cement rotary kiln under normal pressure
综上,[M4Gu]Ac和[TMG][Lac]对水泥窑窑尾模拟烟气(混合气体)中CO2的吸收性能远劣于其对纯CO2的吸收性能。
3 结 论
1)在定压、定温条件下,离子液体的CO2吸收量随时间的延长逐步增大,且增速不断降低,最终达到CO2吸收量的极大值。在定压、变温条件下,2种离子液体的CO2最大吸收量随温度的升高大幅下降。70 ℃时,[M4Gu]Ac和[TMG][Lac]的最大吸收量仅为2种离子液体在30 ℃时最大吸收量的49.3%和41.7%、50 ℃时最大吸收量的60.8%和51.4%。
2)在5个吸收和再生循环试验中,离子液体[M4Gu]Ac和[TMG][Lac]的CO2最大吸收量近似相等,吸收性能基本维持稳定,吸收和解吸次数对考察离子液体的CO2吸收性能影响不大。
3)[M4Gu]Ac和[TMG][Lac]对水泥窑窑尾模拟烟气(混合气体)中CO2的吸收性能远劣于其对纯CO2的吸收性能。对于纯CO2吸收,离子液体[M4Gu]Ac的吸收性能略优于[TMG][Lac];对于水泥窑窑尾模拟烟气中CO2的吸收,30 ℃时,[M4Gu]Ac的吸收性能优于[TMG][Lac],50、70 ℃下,[M4Gu]Ac的吸收性能劣于[TMG][Lac]。
[1] 国家统计局. 中国统计年鉴 [J]. 北京:中国统计出版社,2019.
State Statistical Bureau. China statistical yearbook [J]. Beijing:China Statistics Press,2019.
[2] 国家统计局. 中国统计年鉴 [J]. 北京:中国统计出版社,2017.
State Statistical Bureau. China statistical yearbook [J]. Beijing:China Statistics Press,2017.
[3] 高长明. 水泥工业低碳转型刻不容缓 [J]. 新世纪水泥导报,2019(6):1-4.
GAO Changming.No time to delay for low carbon transformation of cement industry to the world especially China [J]. Cement Guide for New Epoch,2019(6):1-4.
[4] ALI M B,SAIDUR R,HOSSAIN M S. A review on emission analysis in cement industries [J]. Renewable and Sustainable Energy Reviews,2011,15(5):2252-2261.
[5] 步学朋. 二氧化碳捕集技术及应用分析 [J]. 洁净煤技术,2014,20(5):9-13.
BU Xupeng. CO2 capture technologies and application [J]. Clean Coal Technology,2014,20(5):9-13.
[6] 池渊.CO2捕集与封存中气体吸附特性研究 [D]. 大连:大连理工大学,2018.
CHI Yuan.Study on gas adsorption characteristics in CO2 capture and storage abstract [D]. Dalian:Dalian University of Technology,2018.
[7] 余景文. 氨水溶液脱除燃煤电站烟气中二氧化碳能耗研究 [D]. 北京:清华大学,2016.
YU Jingwen.Study on energy requirement for CO2 capture with aqueous ammonia solution [D]. Beijing:Tsinghua University,2016.
[8] JANSEN D,GAZZANI M,MANZOLINI G,et al. Pre-combustion CO2 capture [J]. International Journal of Greenhouse Gas Control,2015,40:167-187.
[9] 杨楠. 改良氨法捕集烟气中CO2技术的研究 [D]. 北京:中国矿业大学(北京),2015.
YANG Nan.Post-combustion capture of CO2 using advanced aqueous ammonia. Beijing:China University of Mining & Technology(Beijing),2015.
[10] STADLER H,CHRIST D,HABERMEHL M,et al. Experimental investigation of NOx emissions in oxycoal combustion [J].Fuel,2011,90:1604-1611.
[11] 周小斌. 新型两相胺吸收剂捕集二氧化碳研究 [D]. 厦门:华侨大学,2019.
ZHOU Xiaobin. Study on carbon dioxide capture using a novel biphasic solvent [D]. Xiamen:Huaqiao University,2019.
[12] WANG Y M,CHEN Y S. Capture of CO2 by highly concentrated alkanolamine solutions in a rotating packed bed [J]. Environmental Progress & Sustainable Energy,2019,38(6):115-122.
[13] 冯绪文,郭兴蓬. 烷醇胺水溶液的CO2吸收机理及其腐蚀行为的相关性研究 [J]. 中国腐蚀与防护学报,2003,23(2):79-83.
FENG Xuwen,GUO Xingpeng. Study on the correlation between CO2 absorption mechanisms and corrosion behavior of alkanolamine solutions [J]. Journal of Chinese Society for Corrosion and Protection,2003,23(2):79-83.
[14] 吴彬,黄坤荣,刘子健. 化学吸收法捕集二氧化碳研究进展 [J]. 广州化工,2017,45(11):11-13.
WU Bin,HUANG Kunrong,LIU Zijian. Research progress on carbon dioxide capture by chemical absorption [J]. Guangzhou Chemical Industry,2017,45(11):11-13.
[15] 袁晓亮,张延强,兰玲,等. 离子液体固定CO2及其转化利用的研究进展 [J]. 过程工程学报,2008,8(2):409-416.
YUAN Xiaoliang,ZHANG Yanqiang,LAN Ling,et al. Research progress in fixation and transformation of CO2 using ionic liquids [J]. The Chinese Journal of Process Engineering,2008,8(2):409-416.
[16] 王斌,周瀚成,郭新风. 离子液体固定和转化CO2研究 [J]. 化工设计通讯,2018,44(12):151-152.
WANG Bin,ZHOU Hancheng,GUO Xinfeng. Study on ionic liquid fixation and conversion of CO2 [J]. Chemical Engineering Design Communications,2018,44(12):151-152.
[17] MAKINO T,KANAKUBO M. CO2 absorption property of ionic liquid and CO2permselectivity for ionic liquid membrane [J]. Journal of the Japan Petroleum Institute,2016,59(4):109-117.
[18] HOSPITAL-BENITO D,LEMUS J,MOYA C,et al. Process analysis overview of ionic liquids on CO2 chemical capture [J]. Chemical Engineering Journal,2020,390:124509.
[19] LYU B,HUANG Q,ZHOU Z,et al. Novel biphasic amino-functionalized ionic liquid solvent for CO2 capture:Kinetics and regeneration heat duty [J]. Environmental Science and Pollution Research,2020,27:26965-26973.
[20] LIU F,SHEN Y,SHEN L,et al. A novel amino functionalized ionic liquid/ organic solvent with low viscosity for CO2 capture [J]. Environmental Science & Technology,2020,54(6):3520-3529.
[21] WU G,LIU Y,LIU G,et al. The CO2 absorption in flue gas using mixed ionic liquids [J]. Molecules,2020,25(5):1034.
[22] AKHMETSHINA A I,PETUKHOV A N,VOROTYNTSEV A V,et al. Absorption behavior of acid gases in protic ionic liquid/alkanolamine binary mixtures [J]. ACS Sustainable Chemistry & Engineering,2017,5(4):3429-3437.
[23] SHAAHMADI F,SHAHRAKI B H,FARHADI A. The CO2/CH4 gas mixture solubility in ionic liquids [Bmim][Ac],[Bmim][BF4] and their binary mixtures [J]. Journal of Chemical Thermodynamics,2020,141:105922.
[24] HANDY H,SANTOSO A,WIDODO A,et al. H2S-CO2 separation using room temperature ionic liquid [BMIM][Br] [J]. Separation Science and Technology,2014,49(13):2079-2084.
[25] JALILI A H,SAFAVI M,GHOTBi C,et al. Solubility of CO2,H2S,and their mixture in the ionic liquid 1-Octyl-3-methylimidazolium bis(trifluoromethyl) sulfonylimide [J]. Journal of Physical Chemistry B,2012,116:2758-2774.